2,6-Diaminopurina - 2,6-Diaminopurine
|
|
| Nomes | |
|---|---|
|
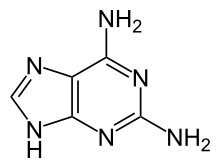
Nome IUPAC
7 H -purina-2,6-diamina
|
|
| Outros nomes
2-aminoadenina; 2,6-DAP
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.016.006 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 5 H 6 N 6 | |
| Massa molar | 150,145 g · mol −1 |
| Aparência | Pó cristalino branco a amarelo |
| Densidade | 1,743 g / cm 3 |
| Ponto de fusão | 117 a 122 ° C (243 a 252 ° F; 390 a 395 K) |
| 2,38 g / L a 20 ° C | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
2,6-diaminopurina ( 2,6-DAP , também conhecido como 2-aminoadenina ) é um composto usado uma vez no tratamento da leucemia . Como base Z, é encontrada no lugar da adenina (A) no material genético de alguns vírus bacteriófagos .
Em agosto de 2011, um relatório, baseado em estudos da NASA com meteoritos encontrados na Terra , foi publicado sugerindo que a 2,6-diaminopurina e moléculas orgânicas relacionadas , incluindo os componentes de DNA e RNA adenina e guanina , podem ter sido formadas extraterrestre no espaço sideral .
Em vírus
No cianófago S-2L ( Siphoviridae ), a diaminopurina é usada em vez da adenina ( evasão do hospedeiro ). A base de diaminopurina (Z) combina perfeitamente com a timina (T), pois é idêntica à adenina (A), mas tem um grupo amina na posição 2 formando 3 ligações de hidrogênio intermoleculares, eliminando a principal diferença entre os dois tipos de pares de bases (fraco: AT e forte: CG). Esta estabilidade melhorada afeta as interações de ligação de proteínas que dependem dessas diferenças.
Quatro artigos publicados em abril de 2021 descrevem com mais detalhes o uso e a produção da Z-base. Agora sabe-se que:
- O fago S-2L evita a incorporação de bases A no genoma hidrolisando dATP (enzima DatZ);
- A base Z é produzida por uma via envolvendo DUF550 (MazZ) e PurZ em S-2L e Vibrio fago PhiVC8;
- A DNA polimerase PrimPol / AEP responsável pelo manuseio da base Z ocorre no mesmo agrupamento de genes que as três enzimas mencionadas;
- A base Z é bastante difundida tanto em Siphoviridae quanto em Podoviridae , com base na ocorrência do referido agrupamento de genes.
Em agosto de 2021, foi demonstrado que DatZ, MazZ e PurZ são suficientes para substituir alguma ocorrência de A por Z no genoma bacteriano de E. coli ; a expressão desse sistema é tóxica para a célula. As estruturas de MAZZ (subtipo 2) e PurZ são também determinadas, que mostra uma possível ligação entre PurZ e de arqueobactia verions de purA.
Biossíntese
A 2-aminoadenina é produzida em duas etapas. A enzima MazZ (homóloga a MazG, EC 3.6.1.8 ) executa primeiro:
- dGTP + H 2 O = dGMP + difosfato
A enzima PurZ (homóloga a PurA, EC 6.3.4.4 ) então realiza:
- (d) ATP + dGMP + L-aspartato = (d) ADP + fosfato + 2-aminodesoxiadenilossuccinato (dSMP)
O dSMP resultante é processado por enzimas hospedeiras analogamente ao adenilossuccinato para produzir dZTP.
Na vida celular
2,6-DAP foi usado para tratar a leucemia desde 1951. É conhecido por interromper a progressão do ciclo celular em células de leucemia de camundongo em 1989. As células cancerosas são conhecidas por se tornarem resistentes ao DAP ao perder sua função de adenina fosforibosiltransferase (APRT) , um processo compartilhado com E. coli .
Os derivados de DAP são antivirais in vitro úteis contra o vírus da pseudo-raiva , uma doença pecuária economicamente importante. Essa base, em sua forma livre, é capaz de corrigir mutações sem sentido UGA por meio do incentivo à leitura translacional , por meio da inibição de FTSJ1 .
Bioengenharia
Na bioengenharia, os oligonucleotídeos anti-miRNA (especificamente, o tipo de ácido nucléico de serinol [SNA]) incorporando a base Z em vez de A mostram ligação aumentada ao RNA.
O DAP é usado de maneira semelhante a outros análogos do ácido nuclear na investigação de estruturas e mecanismos enzimáticos.

