Dirênio decacarbonil - Dirhenium decacarbonyl

|
|
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
bis (pentacarbonilrênio) ( Re - Re )
|
|
| Outros nomes
Carbonil de rênio; rênio pentacarbonil
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.034.714 |
|
PubChem CID
|
|
|
|
|
|
| Propriedades | |
| Re 2 (CO) 10 | |
| Massa molar | 652,52 g / mol |
| Ponto de fusão | 170 ° C (338 ° F; 443 K) (decompõe-se) |
| Perigos | |
| Nocivo ( Xn ) | |
| Frases R (desatualizado) | R20 |
| Frases S (desatualizado) | S36 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
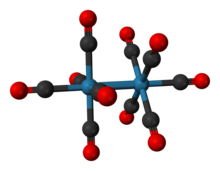
O dirênio decacarbonil é o composto inorgânico com a fórmula química Re 2 (CO) 10 . Disponível comercialmente, é usado como ponto de partida para a síntese de muitos complexos de rênio- carbonila . Foi relatado pela primeira vez em 1941 por Walter Hieber , que o preparou por carbonilação redutiva de rênio. O composto consiste em um par de unidades Re (CO) 5 piramidais quadradas unidas por uma ligação Re-Re, que produz um complexo carbonil homoléptico.
História
Na década de 1930, Robert Mond desenvolveu métodos que usavam o aumento da pressão e da temperatura para produzir várias formas de carbonil metálico . Um proeminente cientista do século XX, Walter Hieber foi crucial para o desenvolvimento posterior do dirênio decacarbonil. Os esforços iniciais produziram complexos de metal mononuclear, mas após avaliação adicional, Hieber descobriu que usando Re 2 O 7 como um material de partida sem solvente, um complexo de dirênio poderia ser alcançado produzindo uma interação Re-Re.
Estrutura e propriedades
A estrutura cristalina do Re 2 (CO) 10 é relativamente bem conhecida. O composto consiste em um par de unidades Re (CO) 5 piramidais quadradas ligadas por uma ligação Re-Re. Existem duas conformações diferentes que podem ocorrer: escalonada e eclipsada. A conformação eclipsada ocorre cerca de 30% das vezes, produzindo um grupo de pontos D 4h , mas a forma escalonada, com grupo de pontos D 4d , é mais estável. O comprimento da ligação Re-Re foi experimentalmente determinado como sendo 3,04Å.
O átomo Re existe em uma configuração octaédrica ligeiramente distorcida com o ângulo C axial-Re-C equatorial igual a 88 °. O comprimento médio da ligação Re-C de 2,01 Å é o mesmo para as posições axial e equatorial . A distância média de CO é 1,16 Å.
Este composto tem uma ampla banda de absorção de IV em 1800 cm −1 e a região pode ser atribuída a dois componentes centrados em 1780 e 1830 cm −1 , resultantes da adsorção de CO. Os nove grupos CO restantes em Re 2 (CO) 10 fornecem a absorção de IV complexa na região 1950–2150 cm −1 . Livre Re 2 (CO) 10 ( simetria de ponto D 4d ) tem uma representação de estiramento de CO de 2A 1 + E 2 + E 3 + 2B 2 + E 1 , onde 2B 2 + E 1 são IR ativos. Para uma molécula (C 4v ) Re 2 (CO) 10 axialmente perturbada , a representação do trecho de CO foi encontrada como sendo 2E + B 1 + B 2 + 3A 1 , onde os modos ativos de IR são 2E + 3A 1 .
Sua identidade também pode ser confirmada por espectrometria de massa, usando o padrão isotópico de rênio ( 185 Re e 187 Re).
Síntese
O decacarbonil de dirênio pode ser obtido por carbonilação redutiva de óxido de rênio (VII) (Re 2 O 7 ) a 350 atm e 250 ° C.
- Re 2 O 7 + 17 CO → Re 2 (CO) 10 + 7 CO 2
Reações
Os ligantes de carbonila podem ser substituídos por outros ligantes, como fosfinas e fosfitos (denotados por L).
- Re 2 (CO) 10 + 2 L → Re 2 (CO) 8 L 2
Este composto também pode ser "craqueado" em complexos Re (I) carbonil mononucleares por halogenação :
- Re 2 (CO) 10 + X 2 → 2 Re (CO) 5 X (X = Cl, Br, I)
Quando o bromo é usado, o bromopentacarbonilrênio (I) é formado, que é um intermediário para muitos mais complexos de rênio. Este composto também pode ser hidrogenado para formar vários complexos de polirrênio, eventualmente dando rênio elementar.
- Re 2 (CO) 10 → H 3 Re 3 (CO) 12 → H 5 Re 4 (CO) 12 → Re (metal)
Na presença de água, a fotólise de Re 2 (CO) 10 produz um complexo de hidróxido:
- Re 2 (CO) 10 → HRe (CO) 5 + Re 4 (CO) 12 (OH) 4
Esta reação inclui a clivagem da ligação Re-Re e a síntese de HRe (CO) 5 , que pode ser usada para preparar estruturas de superfície projetadas para incorporar complexos Re carbonil ligados à superfície isolados.
A perda de um ligante de carbonila por fotólise gera um complexo coordenadamente insaturado que sofre adição oxidativa de ligações Si-H, por exemplo:
- Re 2 (CO) 10 + HSiCl 3 * → (CO) 5 ReHRe (CO) 4 SiCl 3 + CO
Formulários
A catálise à base de rênio tem sido usada em metátese , reforma, hidrogenação e vários processos de hidrotratamento, como hidrodessulfurização . Re 2 (CO) 10 pode ser usado para promover a silação de álcoois e preparar os éteres silílicos , e sua reação:
- RSiH 3 + R'OH → RH 2 SiOR '+ H 2
