Ferredoxina - Ferredoxin
As ferredoxinas (do latim ferrum : ferro + redox , frequentemente abreviado como "fd") são proteínas ferro-enxofre que medeiam a transferência de elétrons em uma variedade de reações metabólicas. O termo "ferredoxina" foi cunhado por DC Wharton da DuPont Co. e aplicado à "proteína de ferro" purificada pela primeira vez em 1962 por Mortenson, Valentine e Carnahan da bactéria anaeróbica Clostridium pasteurianum .
Outra proteína redox, isolada dos cloroplastos do espinafre , foi denominada "ferredoxina do cloroplasto". A ferredoxina do cloroplasto está envolvida nas reações de fotofosforilação cíclicas e não cíclicas da fotossíntese . Na fotofosforilação não cíclica, a ferredoxina é o último aceptor de elétrons, reduzindo assim a enzima NADP + redutase. Aceita elétrons produzidos a partir da clorofila excitada pela luz solar e os transfere para a enzima ferredoxina: NADP + oxidorredutase EC 1.18.1.2 .
As ferredoxinas são pequenas proteínas que contêm átomos de ferro e enxofre organizados como aglomerados de ferro-enxofre . Esses " capacitores " biológicos podem aceitar ou descarregar elétrons, com o efeito de uma mudança no estado de oxidação dos átomos de ferro entre +2 e +3. Dessa forma, a ferredoxina atua como um agente de transferência de elétrons em reações redox biológicas .
Outros sistemas de transporte de elétrons bioinorgânicos incluem rubredoxinas , citocromos , proteínas de cobre azul e as proteínas de Rieske estruturalmente relacionadas .
As ferredoxinas podem ser classificadas de acordo com a natureza de seus clusters ferro-enxofre e por similaridade de sequência.
Bioenergética de ferredoxinas
As ferredoxinas normalmente realizam uma única transferência de elétrons.
Fd0
boi+ e - Fd -
vermelho
No entanto, algumas ferredoxinas bacterianas (do tipo 2 [4Fe4S]) têm dois aglomerados de enxofre de ferro e podem realizar duas reações de transferência de elétrons. Dependendo da sequência da proteína, as duas transferências podem ter potenciais de redução quase idênticos ou podem ser significativamente diferentes.
Fd0
boi+ e - Fd -
vermelho
Fd-
vermelho+ e - Fd 2 -
vermelho
As ferredoxinas são um dos portadores de elétrons biológicos mais redutores. Eles normalmente têm um potencial de ponto médio de -420 mV. O potencial de redução de uma substância na célula será diferente de seu potencial de ponto médio, dependendo das concentrações de suas formas reduzida e oxidada. Para uma reação de um elétron, o potencial muda em cerca de 60 mV para cada potência de dez na proporção da concentração. Por exemplo, se o pool de ferredoxina for cerca de 95% reduzido, o potencial de redução será em torno de -500 mV. Em comparação, outras reações biológicas geralmente têm menos potenciais de redução: por exemplo, o redutor biossintético primário da célula, NADPH tem um potencial redox celular de -370 mV ( E
0 = -320 mV).
Dependendo da sequência da proteína de suporte, as ferredoxinas têm potencial de redução de cerca de -500mv a -340 mV. Uma única célula pode ter vários tipos de ferredoxinas, onde cada tipo é ajustado para realizar diferentes reações de maneira ideal.
Redução de ferredoxina
As ferredoxinas altamente redutoras são reduzidas usando outro agente redutor forte, ou usando alguma fonte de energia para "impulsionar" elétrons de fontes menos redutoras para a ferredoxina.
Redução direta
As reações que reduzem Fd incluem a oxidação de aldeídos em ácidos como a reação de gliceraldeído em glicerato (-580 mV), a reação de monóxido de carbono desidrogenase (-520 mV) e as reações de 2-oxoácido: Fd Oxidoredutase (-500 mV) como a reação realizada por piruvato sintase .
Redução acoplada do potencial da membrana
A ferredoxina também pode ser reduzida usando NADH (-320 mV) ou H
2(-414 mV), mas esses processos são acoplados ao consumo do potencial de membrana para alimentar o "impulso" de elétrons para o estado de energia superior. O complexo Rnf é uma proteína de membrana difundida em bactérias que transfere elétrons entre NADH e ferredoxina enquanto bombeia Na+
ou H+
íons através da membrana. O potencial quimiosmótico da membrana é consumido para alimentar a redução desfavorável de Fd
boipor NADH. Esta reação é uma fonte essencial de Fd-
vermelhoem muitos organismos autotróficos. Se a célula está crescendo em substratos que fornecem Fd em excesso-
vermelho, o complexo Rnf pode transferir esses elétrons para NAD+
e armazenar a energia resultante no potencial de membrana. As hidrogenases de conversão de energia (Ech) são uma família de enzimas que acoplam reversivelmente a transferência de elétrons entre Fd e H
2enquanto bombeia H+
íons através da membrana para equilibrar a diferença de energia.
Fd0
boi+ NADH + Na+
fora Fd2 -
vermelho+ NAD+
+ Na+
dentro
Fd0
boi+ H
2+ H+
fora Fd2 -
vermelho+ H+
+ H+
dentro
Bifurcação de elétrons
A redução desfavorável de Fd de um doador de elétrons menos redutor pode ser acoplada simultaneamente com a redução favorável de um agente oxidante por meio de uma reação de bifurcação de elétrons . Um exemplo da reação de bifurcação de elétrons é a geração de Fd-
vermelhopara fixação de nitrogênio em certos diazotróficos aeróbios . Normalmente, na fosforilação oxidativa, a transferência de elétrons do NADH para a Ubiquinona (Q) é acoplada ao carregamento da força motriz do próton. No Azotobacter, a energia liberada pela transferência de um elétron de NADH para Q é usada para aumentar simultaneamente a transferência de um elétron de NADH para Fd.
Redução direta de ferredoxinas de alto potencial
Algumas ferredoxinas têm um potencial redox suficientemente alto que podem ser reduzidas diretamente pelo NADPH. Uma dessas ferredoxinas é a adrenoxina (-274mV), que participa da biossíntese de muitos esteróides de mamíferos. A ferredoxina Fd3 nas raízes das plantas, que reduz o nitrato e o sulfito, tem um potencial de ponto médio de -337mV e também é reduzida pelo NADPH.
Fe 2 S 2 ferredoxinas
| Domínio de ligação do cluster ferro-enxofre 2Fe-2S | |||||||||
|---|---|---|---|---|---|---|---|---|---|
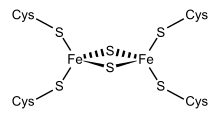 Representação estrutural de uma ferredoxina Fe 2 S 2 .
| |||||||||
| Identificadores | |||||||||
| Símbolo | Fer2 | ||||||||
| Pfam | PF00111 | ||||||||
| Clã Pfam | CL0486 | ||||||||
| InterPro | IPR001041 | ||||||||
| PRÓSITO | PDOC00642 | ||||||||
| SCOP2 | 3fxc / SCOPe / SUPFAM | ||||||||
| Proteína OPM | 1kf6 | ||||||||
| |||||||||
Os membros da superfamília das ferredoxinas 2Fe – 2S ( InterPro : IPR036010 ) têm uma estrutura central geral que consiste em beta (2) -alfa-beta (2), que inclui putidaredoxina, terpredoxina e adrenodoxina. Eles são proteínas de cerca de cem aminoácidos com quatro resíduos de cisteína conservados aos quais o cluster 2Fe – 2S está ligado. Esta região conservada também é encontrada como um domínio em várias enzimas metabólicas e em proteínas de múltiplos domínios, como aldeído oxidoredutase ( N- terminal), xantina oxidase ( N- terminal), ftalato dioxigenase redutase ( C- terminal), succinato desidrogenase ferro-enxofre proteína ( N- terminal) e metano monooxigenase redutase ( N- terminal).
Ferredoxinas de tipo vegetal
Um grupo de ferredoxinas, originalmente encontrado nas membranas do cloroplasto , foi denominado "tipo cloroplástico" ou "tipo planta" ( InterPro : IPR010241 ). Seu centro ativo é um aglomerado [Fe 2 S 2 ], onde os átomos de ferro são tetraedricamente coordenados por átomos de enxofre inorgânicos e por enxofre de quatro resíduos de cisteína (Cys) conservados.
Nos cloroplastos, as ferredoxinas Fe 2 S 2 funcionam como transportadores de elétrons na cadeia de transporte de elétrons fotossintética e como doadores de elétrons para várias proteínas celulares, como glutamato sintase, nitrito redutase, sulfito redutase e a ciclase da biossíntese de clorofila . Uma vez que a ciclase é uma enzima dependente da ferredoxina, isso pode fornecer um mecanismo para a coordenação entre a fotossíntese e a necessidade dos cloroplastos de clorofila, ligando a biossíntese da clorofila à cadeia fotossintética de transporte de elétrons. Na hidroxilação de sistemas de dioxigenases bacterianas, eles atuam como transportadores intermediários de transferência de elétrons entre as flavoproteínas redutase e a oxigenase.
Ferredoxinas semelhantes à tioredoxina
A ferredoxina Fe 2 S 2 de Clostridium pasteurianum ( Cp 2FeFd; P07324 ) foi reconhecida como uma família de proteínas distinta com base em sua sequência de aminoácidos, propriedades espectroscópicas de seu cluster ferro-enxofre e a capacidade única de troca de ligante de dois ligantes de cisteína para o cluster [Fe 2 S 2 ]. Embora o papel fisiológico desta ferredoxina permaneça obscuro, uma interação forte e específica de Cp 2FeFd com a proteína molibdênio-ferro da nitrogenase foi revelada. Ferredoxinas homólogas de Azotobacter vinelandii ( Av 2FeFdI; P82802 ) e Aquifex aeolicus ( Aa Fd; O66511 ) foram caracterizadas. A estrutura cristalina de Aa Fd foi resolvida. Aa Fd existe como um dímero. A estrutura do monômero Aa Fd é diferente de outras ferredoxinas Fe 2 S 2 . A dobra pertence à classe α + β, com as primeiras quatro cadeias β e duas α-hélices adotando uma variante da dobra da tioredoxina . O UniProt os categoriza como a família "ferredoxina do tipo 2Fe2S Shethna".
Ferredoxinas do tipo adrenodoxina
| ferredoxina 1 | |||||||
|---|---|---|---|---|---|---|---|
 Estrutura cristalina da ferredoxina-1 humana (FDX1).
| |||||||
| Identificadores | |||||||
| Símbolo | FDX1 | ||||||
| Alt. símbolos | FDX | ||||||
| Gene NCBI | 2230 | ||||||
| HGNC | 3638 | ||||||
| OMIM | 103260 | ||||||
| RefSeq | NM_004109 | ||||||
| UniProt | P10109 | ||||||
| Outros dados | |||||||
| Locus | Chr. 11 q22.3 | ||||||
| |||||||
A adrenodoxina (ferredoxina adrenal; InterPro : IPR001055 ), a putidaredoxina e a terpredoxina constituem uma família de proteínas Fe 2 S 2 solúveis que atuam como transportadores de um único elétron, encontradas principalmente em mitocôndrias e proteobactérias eucarióticas . A variante humana da adrenodoxina é referida como ferredoxina-1 e ferredoxina-2 . Nos sistemas de monooxigenase mitocondrial, a adrenodoxina transfere um elétron do NADPH: adrenodoxina redutase para o citocromo P450 ligado à membrana . Em bactérias, a putidaredoxina e a terpredoxina transferem elétrons entre as redutases de ferredoxina dependentes de NADH correspondentes e os P450s solúveis. As funções exatas de outros membros desta família não são conhecidas, embora Escherichia coli Fdx esteja envolvida na biogênese de aglomerados de Fe-S. Apesar da baixa similaridade de sequência entre as ferredoxinas do tipo adrenodoxina e do tipo vegetal, as duas classes têm uma topologia de dobramento semelhante.
A ferredoxina-1 em humanos participa da síntese dos hormônios tireoidianos. Ele também transfere elétrons da adrenodoxina redutase para o CYP11A1 , uma enzima CYP450 responsável pela clivagem da cadeia lateral do colesterol. O FDX-1 tem a capacidade de se ligar a metais e proteínas. A ferredoxina-2 participa da síntese de proteínas heme A e ferro-enxofre.
Fe 4 S 4 e Fe 3 S 4 ferredoxinas
As ferredoxinas [Fe 4 S 4 ] podem ser subdivididas em ferredoxinas de baixo potencial (tipo bacteriano) e alto potencial (HiPIP) .
As ferredoxinas de baixo e alto potencial estão relacionadas pelo seguinte esquema redox:
Os números de oxidação formal dos íons de ferro podem ser [2Fe 3+ , 2Fe 2+ ] ou [1Fe 3+ , 3Fe 2+ ] em ferredoxinas de baixo potencial. Os números de oxidação dos íons de ferro em ferredoxinas de alto potencial podem ser [3Fe 3+ , 1Fe 2+ ] ou [2Fe 3+ , 2Fe 2+ ].
Ferredoxinas do tipo bacteriano
| Domínio de ligação 3Fe-4S | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 Representação estrutural de uma ferredoxina Fe 3 S 4 .
| |||||||||||
| Identificadores | |||||||||||
| Símbolo | Fer4 | ||||||||||
| Pfam | PF00037 | ||||||||||
| InterPro | IPR001450 | ||||||||||
| PRÓSITO | PDOC00176 | ||||||||||
| SCOP2 | 5fd1 / SCOPe / SUPFAM | ||||||||||
| Proteína OPM | 1kqf | ||||||||||
| |||||||||||
Um grupo de ferredoxinas Fe 4 S 4 , originalmente encontrado em bactérias, foi denominado "tipo bacteriano". As ferredoxinas do tipo bacteriano podem, por sua vez, ser subdivididas em outros grupos, com base em suas propriedades de sequência. A maioria contém pelo menos um domínio conservado, incluindo quatro resíduos de cisteína que se ligam a um cluster [Fe 4 S 4 ]. Na ferredoxina Pyrococcus furiosus Fe 4 S 4 , um dos resíduos Cys conservados é substituído por ácido aspártico.
Durante a evolução das ferredoxinas do tipo bacteriano, ocorreram eventos de duplicação, transposição e fusão de genes intra-sequência, resultando no aparecimento de proteínas com múltiplos centros de ferro-enxofre. Em algumas ferredoxinas bacterianas, um dos domínios duplicados perdeu um ou mais dos quatro resíduos Cys conservados. Esses domínios perderam sua propriedade de ligação ferro-enxofre ou se ligaram a um aglomerado [Fe 3 S 4 ] em vez de um aglomerado [Fe 4 S 4 ] e do tipo aglomerado.
As estruturas 3-D são conhecidas por uma série de ferredoxinas do tipo bacteriano monocluster e dicluster. A dobra pertence à classe α + β, com 2-7 α-hélices e quatro β-fitas formando uma estrutura semelhante a um barril, e uma alça extrudada contendo três ligantes Cys "proximais" do aglomerado ferro-enxofre.
Proteínas de alto potencial ferro-enxofre
As proteínas de alto potencial ferro-enxofre (HiPIPs) formam uma família única de ferredoxinas Fe 4 S 4 que funcionam em cadeias de transporte de elétrons anaeróbicas. Alguns HiPIPs têm um potencial redox mais alto do que qualquer outra proteína ferro-enxofre conhecida (por exemplo, HiPIP de Rhodopila globiformis tem um potencial redox de cerca de 450 mV). Vários HiPIPs foram caracterizados estruturalmente até agora, suas dobras pertencentes à classe α + β. Como em outras ferredoxinas bacterianas, a unidade [Fe 4 S 4 ] forma um agrupamento do tipo cubano e é ligada à proteína por meio de quatro resíduos Cys.
Proteínas humanas da família das ferredoxinas
Evolução das ferredoxinas
Referências
Leitura adicional
- Bruschi M, Guerlesquin F (1988). "Estrutura, função e evolução das ferredoxinas bacterianas" . Revisões de Microbiologia da FEMS . 4 (2): 155–75. doi : 10.1111 / j.1574-6968.1988.tb02741.x . PMID 3078742 .
- Ciurli S, Musiani F (2005). "Proteínas de alto potencial ferro-enxofre e seu papel como transportadores de elétrons solúveis na fotossíntese bacteriana: conto de uma descoberta". Pesquisa de fotossíntese . 85 (1): 115–31. doi : 10.1007 / s11120-004-6556-4 . PMID 15977063 . S2CID 27768048 .
- Fukuyama K (2004). "Estrutura e função das ferredoxinas do tipo vegetal". Pesquisa de fotossíntese . 81 (3): 289–301. doi : 10.1023 / B: PRES.0000036882.19322.0a . PMID 16034533 . S2CID 24574958 .
- Grinberg AV, Hannemann F, Schiffler B, Müller J, Heinemann U, Bernhardt R (setembro de 2000). "Adrenodoxina: estrutura, estabilidade e propriedades de transferência de elétrons". Proteínas . 40 (4): 590–612. doi : 10.1002 / 1097-0134 (20000901) 40: 4 <590 :: AID-PROT50> 3.0.CO; 2-P . PMID 10899784 .
- Holden HM, Jacobson BL, Hurley JK, Tollin G, Oh BH, Skjeldal L, et al. (Fevereiro de 1994). "Structure-function studies of [2Fe-2S] ferredoxins". Journal of Bioenergetics and Biomembranes . 26 (1): 67–88. doi : 10.1007 / BF00763220 . PMID 8027024 . S2CID 12560221 .
- Meyer J (novembro de 2001). "Ferredoxinas de terceiro tipo" . FEBS Letters . 509 (1): 1–5. doi : 10.1016 / S0014-5793 (01) 03049-6 . PMID 11734195 . S2CID 8101608 .
links externos
- InterPro : IPR006057 - subdomínio de ferredoxina 2Fe – 2S
- InterPro : IPR001055 - Adrenodoxina
- InterPro : IPR001450 - ferredoxina 4Fe-4S, ligação ferro-enxofre
- InterPro : IPR000170 - Proteína ferro-enxofre de alto potencial
- PDB : 1F37 - Estrutura de raios-X da ferredoxina semelhante à tiorredoxina de Aquifex aeolicus ( Aa Fd)


