Ânion oxocarbono - Oxocarbon anion

12O6 a
12, um dos ânions de oxocarbono. Os círculos pretos são átomos de carbono, os círculos vermelhos são átomos de oxigênio. Cada halo azul representa metade de uma carga negativa.
Em química, um ânion oxocarbono é um íon negativo que consiste unicamente em átomos de carbono e oxigênio e, portanto, tem a fórmula geral C
xOn -
ypara alguns inteiros x , y e n .
Os ânions de oxocarbono mais comuns são carbonato , CO2−
3e oxalato , C
2O2−
4. No entanto, há um grande número de ânions estáveis nesta classe, incluindo vários que têm uso industrial ou em pesquisa. Existem também muitos ânions instáveis, como CO-
2e CO-
4, que têm uma existência fugaz durante algumas reações químicas; e muitas espécies hipotéticas, como CO4−
4, que foram objeto de estudos teóricos, mas ainda não foram observados.
Os ânions de oxocarbono estáveis formam sais com uma grande variedade de cátions . Os ânions instáveis podem persistir em um estado gasoso muito rarefeito, como nas nuvens interestelares . A maioria dos ânions oxocarbono tem porções correspondentes na química orgânica , cujos compostos são geralmente ésteres . Assim, por exemplo, a porção oxalato [–O– (C = O) 2 –O–] ocorre no éster dimetil oxalato H 3 C – O– (C = O) 2 –O – CH 3 .
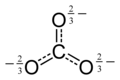
Estrutura eletrônica do íon carbonato
O íon carbonato tem uma estrutura trigonal planar, grupo de pontos D 3h . As três ligações CO têm o mesmo comprimento de 136 pm e os 3 ângulos OCO são 120 °. O átomo de carbono tem 4 pares de elétrons de valência, o que mostra que a molécula obedece à regra do octeto . Esse é um fator que contribui para a alta estabilidade do íon, que ocorre em rochas como o calcário . A estrutura eletrônica é descrita por duas teorias principais que são utilizadas para mostrar como os 4 pares de elétrons são distribuídos em uma molécula que possui apenas 3 ligações CO.
Com a teoria das ligações de valência, a estrutura eletrônica do íon carbonato é um híbrido de ressonância de 3 formas canônicas.
Em cada forma canônica, existem duas ligações simples, uma ligação dupla. As três formas canônicas contribuem igualmente para o híbrido de ressonância, portanto, as três ligações CO têm o mesmo comprimento.
Com a teoria orbital molecular, o eixo triplo é designado como o eixo z da molécula. Três ligações σ são formadas sobrepostas dos orbitais s, p x e p y no átomo de carbono com um orbital ap em cada átomo de oxigênio. Além disso, uma ligação π deslocalizada é feita pela sobreposição do orbital p z no átomo de carbono com o orbital p z em cada átomo de oxigênio que é perpendicular ao plano da molécula.
Observe que os mesmos esquemas de ligação podem ser aplicados ao íon nitrato , NO 3 - , que é isoeletrônico com o íon carbonato.
Da mesma forma, a estrutura simétrica dupla de um grupo carboxilato , CO-
2, pode ser descrito como um híbrido de ressonância de duas formas canônicas na teoria de ligações de valência, ou com 2 ligações σ e uma ligação π deslocalizada na teoria orbital molecular.
Compostos relacionados
Ácidos de oxocarbono
Um ânion oxocarbono C
xOn -
ypode ser visto como o resultado da remoção de todos os prótons de um ácido correspondente C x H n O y . Carbonato CO2−
3, por exemplo, pode ser visto como o ânion de ácido carbônico H 2 CO 3 . Às vezes, o "ácido" é na verdade um álcool ou outra espécie; este é o caso, por exemplo, do acetilenodiolato C
2O2−
2que produziria acetylenediol C 2 H 2 O 2 . No entanto, o ânion é frequentemente mais estável do que o ácido (como é o caso do carbonato); e às vezes o ácido é desconhecido ou espera-se que seja extremamente instável (como é o caso do metanotetracarboxilato C (COO - ) 4 ).
Espécies neutralizadas
Cada ânion oxocarbono C
xOn -
ypode ser combinado em princípio com a variante eletricamente neutra (ou oxidada ) C x O y , um oxocarbono ( óxido de carbono) com a mesma composição e estrutura, exceto para a carga negativa. Como regra, entretanto, esses oxocarbonos neutros são menos estáveis do que os ânions correspondentes. Assim, por exemplo, o ânion carbonato estável corresponde ao trióxido de carbono neutro extremamente instável CO 3 ; oxalato C
2O2−
4correspondem à ainda menos estável 1,2-dioxetanodiona C 2 O 4 ; e o ânion C croconato estável
5O2−
5corresponde à ciclopentanepentona C 5 O 5 neutra , que foi detectada apenas em pequenas quantidades.
Variantes reduzidas
Por outro lado, alguns ânions de oxocarbono podem ser reduzidos para produzir outros ânions com a mesma fórmula estrutural, mas com carga negativa maior. Assim, rodizonato C
6O2−
6pode ser reduzido ao ânion C tetrahidroxibenzoquinona (THBQ)
6O4−
6e então para benzenohexolato C
6O6−
6.
Anidridos ácidos
Um ânion oxocarbono C
xOn -
ytambém pode ser associado ao anidrido do ácido correspondente. Este último seria outro oxocarbon com a fórmula C x O y - n / 2 ; ou seja, a menos ácido n / 2 moléculas de água H 2 O. O exemplo padrão é a ligação entre carbonato de CO2−
3e dióxido de carbono CO 2 . A correspondência nem sempre é bem definida, pois pode haver várias maneiras de realizar essa desidratação formal, incluindo a junção de dois ou mais ânions para formar um oligômero ou polímero . Ao contrário da neutralização, esta desidratação formal às vezes rende oxocarbonos razoavelmente estáveis, como o anidrido melítico C 12 O 9 do melitado C
12O6 a
12via ácido melítico C 12 H 6 O 12
Ânions hidrogenados
Para cada ânion oxocarbono C
xOn -
yexistem em princípio n -1 ânions parcialmente hidrogenados com a fórmula H
kC
xO( n - k ) -
y, onde k varia de 1 a n −1. Esses ânions são geralmente indicados pelos prefixos "hidrogênio" -, "dihidrogênio" -, "trihidrogênio" -, etc. Alguns deles, entretanto, têm nomes especiais: hidrogenocarbonato HCO-
3é comumente chamado de bicarbonato , e hidrogenoxalato HC
2O-
4é conhecido como binoxalato .
Os ânions hidrogenados podem ser estáveis mesmo que o ácido totalmente protonado não seja (como é o caso do bicarbonato).
Lista de ânions oxocarbono
Aqui está uma lista incompleta dos ânions de oxocarbono conhecidos ou conjecturados
Vários outros ânions de oxocarbono foram detectados em quantidades residuais, como C
6O-
6, uma versão ionizada isoladamente do rodizonato.
Veja também
- Oxocarbono
- Silicato
- Percarbonato de sódio (na verdade, um peridrato de carbonato )