Analógico de estado de transição - Transition state analog
Análogos de estado de transição ( análogos de estado de transição ) são compostos químicos com uma estrutura química que se assemelha ao estado de transição de uma molécula de substrato em uma reação química catalisada por enzima . As enzimas interagem com um substrato por meio de deformações ou distorções, movendo o substrato em direção ao estado de transição. Os análogos do estado de transição podem ser usados como inibidores em reações catalisadas por enzimas, bloqueando o sítio ativo da enzima. A teoria sugere que os inibidores da enzima que se assemelham à estrutura do estado de transição se ligariam mais fortemente à enzima do que o substrato real. Exemplos de drogas que são inibidores de análogos do estado de transição incluem medicamentos contra a gripe, como o inibidor da neuraminidase oseltamivir e os inibidores da protease do HIV saquinavir no tratamento da AIDS.
Analógico de estado de transição
O estado de transição de uma estrutura pode ser melhor descrito em relação à mecânica estatística, onde as energias das ligações quebrando e formando têm uma probabilidade igual de se mover do estado de transição para trás para os reagentes ou para a frente para os produtos. Em reações catalisadas por enzimas, a energia de ativação geral da reação é reduzida quando uma enzima estabiliza um intermediário de estado de transição de alta energia . Os análogos do estado de transição imitam este intermediário de alta energia, mas não sofrem uma reação química catalisada e podem, portanto, ligar-se muito mais forte a uma enzima do que o substrato simples ou análogos do produto.
Projetando um estado de transição analógico
Para projetar um análogo do estado de transição, a etapa principal é a determinação da estrutura do estado de transição do substrato na enzima específica de interesse com método experimental, por exemplo, efeito de isótopo cinético . Além disso, a estrutura do estado de transição também pode ser prevista com abordagens computacionais como um complemento ao KIE. Explicaremos esses dois métodos resumidamente.
Efeito de isótopo cinético
O efeito isotópico cinético (KIE) é uma medida da taxa de reação de reagentes marcados com isótopos contra o substrato natural mais comum. Os valores do efeito do isótopo cinético são uma proporção do número de turnover e incluem todas as etapas da reação. Os valores de isótopos cinéticos intrínsecos derivam da diferença no ambiente vibracional da ligação de um átomo nos reagentes no estado fundamental para o ambiente no estado de transição do átomo. Por meio do efeito do isótopo cinético, muitos insights podem ser obtidos sobre como é o estado de transição de uma reação catalisada por enzima e orientar o desenvolvimento de análogos do estado de transição.
Simulação computacional
Abordagens computacionais têm sido consideradas uma ferramenta útil para elucidar o mecanismo de ação de enzimas. A mecânica molecular em si não pode prever a transferência de elétrons, que é a base da reação orgânica, mas a simulação da dinâmica molecular fornece informações suficientes considerando a flexibilidade da proteína durante a reação catalítica. O método complementar seria a combinação de métodos de simulação de mecânica molecular / mecânica quântica ( QM / MM ). Com essa abordagem, apenas os átomos responsáveis pela reação enzimática na região catalítica serão criados com a mecânica quântica e o restante dos átomos serão tratados com a mecânica molecular .
Exemplos de design analógico de estado de transição
Depois de determinar as estruturas de estado de transição usando KIE ou simulações de computação, o inibidor pode ser projetado de acordo com as estruturas de estado de transição ou intermediários determinados. Os três exemplos a seguir ilustram como os inibidores imitam a estrutura do estado de transição, alterando grupos funcionais que correspondem à geometria e distribuição eletrostática das estruturas do estado de transição.
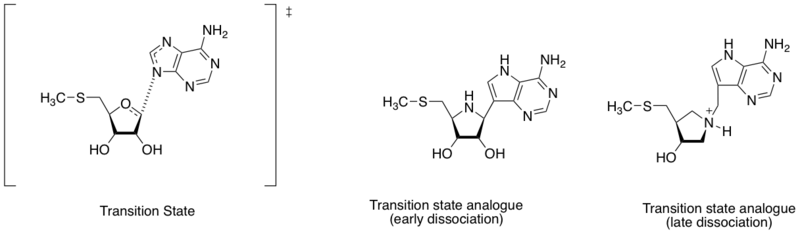
Inibidor de metiltioadenosina nucleosidase
Metiltioadenosina nucleosidase são enzimas que catalisam a reação de deadenilação hidrolítica de 5'-metiltioadenosina e S-adenosilhomocisteína. É também considerado um alvo importante para a descoberta de medicamentos antibacterianos porque é importante no sistema metabólico das bactérias e apenas produzido por bactérias. Dada a distância diferente entre o átomo de nitrogênio da adenina e o carbono anomérico ribose (veja o diagrama nesta seção), a estrutura do estado de transição pode ser definida pelo estágio inicial ou tardio de dissociação. Com base na descoberta de diferentes estruturas de estado de transição, Schramm e colaboradores projetaram dois análogos de estado de transição que imitam o estado de transição dissociativa inicial e tardia. O análogo de estado de transição precoce e tardio mostrou afinidade de ligação (Kd) de 360 e 140 pM, respectivamente.
Inibidor de termolisina
A termolisina é uma enzima produzida pelo Bacillus thermoproteolyticus que catalisa a hidrólise de peptídeos contendo aminoácidos hidrofóbicos. Portanto, também é um alvo para agentes antibacterianos. O mecanismo de reação enzimática começa a formar a pequena molécula de peptídeo e substitui a molécula de água de ligação de zinco para Glu143 de termolisina. A molécula de água é então ativada tanto pelo íon zinco quanto pelo resíduo Glu143 e ataca o carbono carbonil para formar um estado de transição tetraédrico (veja a figura). Holden e colegas de trabalho então imitaram esse estado de transição tetraédrico para projetar uma série de análogos de peptídeo fosfonamidato. Entre os análogos sintetizados, R = L- Leu possui a atividade inibitória mais potente ( K i = 9,1 nM).
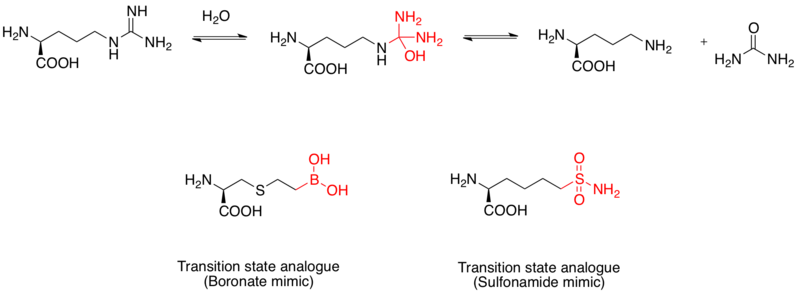
Inibidor de arginase
A arginase é uma metaloproteína binuclear de manganês que catalisa a hidrólise da L- arginina em L- ornitina e ureia . Também é considerado um alvo de drogas para o tratamento da asma . O mecanismo de hidrólise da L-arginina é realizado via ataque nucleofílico ao grupo guanidino pela água, formando um intermediário tetraédrico. Estudos mostraram que uma porção de ácido borônico adota uma configuração tetraédrica e atua como um inibidor. Além disso, o grupo funcional sulfonamida também pode imitar a estrutura do estado de transição. Evidências de mímicos de ácido borônico como inibidores análogos do estado de transição da arginase I humana foram elucidadas por estruturas de cristal de raios-X.
Veja também
- Enzima
- Análogo estrutural , compostos com estrutura química semelhante
- Inibidor de enzima
- Análogo de substrato
- Inibidor de suicídio
- Substrato