Alótropos de boro - Allotropes of boron
O boro pode ser preparado em várias formas cristalinas e amorfas . As formas cristalinas bem conhecidas são α-romboédrica (α-R), β-romboédrica (β-R) e β-tetragonal (β-T). Em circunstâncias especiais, o boro também pode ser sintetizado na forma de seus alótropos α-tetragonal (α-T) e γ-ortorrômbico (γ) . Duas formas amorfas, uma em pó finamente dividido e a outra em um sólido vítreo, também são conhecidas. Embora pelo menos mais 14 alótropos tenham sido relatados, essas outras formas são baseadas em evidências tênues ou não foram confirmadas experimentalmente, ou são pensadas para representar alótropos mistos, ou estruturas de boro estabilizadas por impurezas. Enquanto a fase β-romboédrica é a mais estável e as outras são metaestáveis, a taxa de transformação é desprezível à temperatura ambiente e, portanto, todas as cinco fases podem existir em condições ambientais. Boro pó amorfo e policristalino boro β-romboédrica são as formas mais comuns. O último alótropo é um material cinza muito duro, cerca de dez por cento mais leve que o alumínio e com um ponto de fusão (2080 ° C) várias centenas de graus mais alto que o do aço.
O boro elementar foi encontrado na poeira estelar e meteoritos, mas não existe no ambiente de alto oxigênio da Terra. É difícil extrair de seus compostos. Os métodos mais antigos envolviam a redução do óxido bórico com metais como magnésio ou alumínio . No entanto, o produto está quase sempre contaminado com boretos metálicos . O boro puro pode ser preparado reduzindo halogenetos de boro voláteis com hidrogênio em altas temperaturas. O boro muito puro, para uso na indústria de semicondutores, é produzido pela decomposição do diborano em altas temperaturas, seguida pela purificação por fusão por zona ou pelo processo de Czochralski . Ainda mais difíceis de preparar são os monocristais de fases puras de boro, devido ao polimorfismo e à tendência do boro em reagir com impurezas; o tamanho típico do cristal é ~ 0,1 mm.
Resumo das propriedades
| Fase de boro | α-R | α-T | β-R | β-T | γ | Amorfo | |
|---|---|---|---|---|---|---|---|
|
|
|
||||||
| Simetria | Romboédrico | Tetragonal | Romboédrico | Tetragonal | Ortorrômbico | Semi-aleatório | Semi-aleatório |
| Ocorrência | comum | especial | comum | comum | especial | ||
| Átomos / célula unitária | 12 | 50 | 105‒108 | 192 | 28 | ||
| Densidade (g / cm 3 ) | 2,46 | 2,29‒2,39 | 2,35 | 2,36 | 2,52 | 1,73 | 2,34-35 |
| Dureza Vickers (GPa) | 42 | 45 | 50–58 | ||||
| Módulo de massa (GPa) | 224 | 184 | 227 | ||||
| Lacuna de banda (eV) | 2 | 1,6 | ~ 2,6 | 2,1 | 0,56-0,71 | ||
| Cor | Cristais são vermelhos claros | Preto e opaco, com brilho metálico | Escuro a cinza prateado brilhante | Preto / vermelho | Cinza escuro | Preto para marrom | Preto opaco |
| Primeiro ano relatado | 1958 | 1943/1973 | 1957 | 1960 | 2009 | 1808 | 1911 |
boro α-romboédrico
O boro α-romboédrico possui uma célula unitária de doze átomos de boro. A estrutura consiste em B
12icosaedra em que cada átomo de boro tem cinco vizinhos mais próximos dentro do icosaedro. Se a ligação fosse do tipo covalente convencional , cada boro teria doado cinco elétrons. No entanto, o boro tem apenas três elétrons de valência, e acredita-se que a ligação no B
12 A icosaedra é obtida pelas chamadas ligações deficientes de elétrons de 3 centros, onde a carga do elétron é acumulada no centro de um triângulo formado por três átomos adjacentes.
O isolado B
12os icosaedros não são estáveis, devido à não uniformidade do favo de mel ; assim, o boro não é um sólido molecular, mas os icosaedros nele são conectados por fortes ligações covalentes.
boro α-tetragonal
O α-tetragonal puro só pode ser sintetizado como camadas finas depositadas em um substrato subjacente de carboneto de boro isotrópico (B 50 C 2 ) ou nitreto (B 50 N 2 ). A maioria dos exemplos de boro α-tetragonal são de fato carbonetos ou nitretos ricos em boro .
boro β-romboédrico
O boro β-romboédrico tem uma célula unitária contendo 105–108 (idealmente exatamente 105) átomos. A maioria dos átomos forma um icosaedra discreto B 12 ; alguns formam icosaedros parcialmente interpenetrantes, e há duas unidades deltaédricas B 10 e um único átomo B central. Por muito tempo, não estava claro se a fase α ou β é mais estável em condições ambientais; entretanto, gradualmente foi alcançado um consenso de que a fase β é o alótropo mais termodinamicamente estável.
boro β-tetragonal
A fase β foi produzida em 1960 por redução de hidrogênio de BBr 3 em filamentos quentes de tungstênio , rênio ou tântalo a temperaturas 1270-1550 ° C (ou seja, deposição química de vapor ). Outros estudos reproduziram a síntese e confirmaram a ausência de impurezas nesta fase.
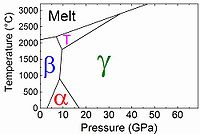
γ-boro
A fase γ pode ser descrita como um arranjo do tipo NaCl de dois tipos de aglomerados, pares B 12 icosaedra e B 2 . Pode ser produzido comprimindo outras fases de boro a 12–20 GPa e aquecendo a 1500–1800 ° C, e permanece estável nas condições ambientais. Há evidências de transferência de carga significativa dos pares B 2 para o icosaedra B 12 nesta estrutura; em particular, a dinâmica da rede sugere a presença de interações eletrostáticas significativas de longo alcance.
Esta fase foi relatada por Wentorf em 1965; no entanto, nem a estrutura nem a composição química foram estabelecidas. A estrutura foi resolvida usando cálculos de predição de estrutura de cristal ab initio e confirmada usando difração de raios-X de cristal único .
Boro cúbico
Sullenger et al. (1969) e McConville et al. (1976) relataram um alótropo cúbico de boro, obtido em experimentos de plasma de argônio, com uma célula unitária de 1705 ± 3 átomos e uma densidade de 2,367 g / cm 3 . Embora este alótropo seja ocasionalmente mencionado na literatura, nenhum trabalho subsequente parece ter sido publicado confirmando ou desacreditando sua existência. Donohue (1982) comentou que o número de átomos na célula unitária não parecia ser icosaedricamente relacionado (o icosaedro sendo um motivo comum às estruturas de boro).
Fase supercondutora de alta pressão
A compressão do boro acima de 160 GPa produz uma fase de boro com uma estrutura ainda desconhecida. Ao contrário de outras fases, que são semicondutores , esta fase é um metal e se torna um supercondutor com uma temperatura crítica aumentando de 6 K a 160 GPa para 11 K a 250 GPa. Essa transformação estrutural ocorre em pressões nas quais a teoria prevê que a icosaedra se dissociará. A especulação quanto à estrutura desta fase incluiu a cúbica centrada na face (análoga ao Al); α-Ga e tetragonal centrado no corpo (análogo a In). Também foi sugerido que a transição não metal-metal é simplesmente o resultado de um fechamento de gap , como ocorre com o iodo, ao invés de uma transição estrutural.
Borofeno
Existem várias formas bidimensionais de boro (juntas chamadas de borofenos ), e ainda mais são previstas teoricamente.
Borosfereno
A descoberta da molécula alotrópica quasisférica borosfereno (B 40 ) foi anunciada em julho de 2014.
Boro amorfo
O boro amorfo contém icosaedras regulares B 12 que são ligadas aleatoriamente entre si sem ordem de longo alcance. O boro amorfo puro pode ser produzido por decomposição térmica do diborano a temperaturas abaixo de 1000 ° C. O recozimento a 1000 ° C converte o boro amorfo em boro β-romboédrico. Nanofios amorfos de boro (30-60 nm de espessura) ou fibras podem ser produzidos por pulverização catódica de magnetron e deposição química de vapor assistida por laser , respectivamente; e também se convertem em nanofios de boro β-romboédrico após recozimento a 1000 ° C.
Notas
Referências
Bibliografia
- Amberger, E. (1981). "Boro elementar". Em Buschbeck, KC (ed.). Manual de Gmelin de química inorgânica e organometálica: B Boron, Supplement 2 (8th ed.). Berlim: Springer-Verlag. pp. 1–112. ISBN 3-540-93448-0.
- Donohue, J. (1982). As estruturas dos elementos . Malabar, Flórida: Robert E. Krieger. ISBN 0-89874-230-7.
- Housecroft, CE; Sharpe, AG (2008). Química Inorgânica (3ª ed.). Harlow: Pearson Education. ISBN 978-0-13-175553-6.
- Madelung, O. (1983). Dados numéricos de Landolt-Bornstein e relações funcionais em ciência e tecnologia. Nova série. Grupo III. Volume 17: Semicondutores. Subvolume e: elementos Física de não-tetrahedrally ligados e compostos binários I . Springer-Verlag: New York. ISBN 0-387-11780-6.
- Nelmes, RJ; Loveday, JS; Allan, DR; Besson, JM; Hamel, G .; Grima, P .; Hull, S. (1993). "Medições de difração de raios-x e nêutrons do módulo de volume do boro". Physical Review B . 47 (13): 7668–7673. Bibcode : 1993PhRvB..47.7668N . doi : 10.1103 / PhysRevB.47.7668 . PMID 10004773 .
- Oganov, AR; Chen, J .; Poderia.; Glass, CW; Yu, Z .; Kurakevych, OO; Solozhenko, VL (12 de fevereiro de 2009). "Forma iônica de alta pressão do boro elementar". Nature . 457 (7027): 863–868. arXiv : 0911.3192 . Bibcode : 2009Natur.457..863O . doi : 10.1038 / nature07736 . PMID 19182772 .
- Sullenger, DB; Phipps, KD; Seabaugh, PW; Hudgens, CR; Sands, DE; Cantrell, JS (1969). "Modificações de boro produzidas em um plasma de argônio acoplado por indução". Ciência . 163 (3870): 935‒937. Bibcode : 1969Sci ... 163..935S . doi : 10.1126 / science.163.3870.935 . PMID 17737317 .
- Talley, CP; La Plaça, S .; Post, B. (1960). “Um novo polimorfo do boro” . Acta Crystallographica . 13 (3): 271‒2. doi : 10.1107 / S0365110X60000613 .
- Wang, YQ; Duan, XF (2003). "Nanofios de boro cristalinos". Letras de Física Aplicada . 82 (2): 272. bibcode : 2003ApPhL..82..272W . doi : 10.1063 / 1.1536269 . S2CID 122278136 .
- Wentorf, RH (1965). "Boro: Outra forma". Ciência . 147 (3653): 49–50. Bibcode : 1965Sci ... 147 ... 49W . doi : 10.1126 / science.147.3653.49 . PMID 17799779 .
- Wiberg, N. (2001). Química inorgânica . San Diego: Academic Press. ISBN 0-12-352651-5.
- Will, G .; Kiefer, B. (2001). "Densidade de deformação de elétrons em α-boro romboédrico". Zeitschrift für anorganische und allgemeine Chemie . 627 (9): 2100‒104. doi : 10.1002 / 1521-3749 (200109) 627: 9 <2100 :: AID-ZAAC2100> 3.0.CO; 2-G .
- Zarechnaya, EY; Dubrovinsky, L .; Dubrovinskaia, N .; Filinchuk, Y .; Chernyshov, D .; Dmitriev, V .; Miyajima, N .; El Goresy, A .; et al. (2009). "Superhard semicondutor opticamente transparente fase de alta pressão de boro". Cartas de revisão física . 102 (18): 185501‒4. Bibcode : 2009PhRvL.102r5501Z . doi : 10.1103 / PhysRevLett.102.185501 . PMID 19518885 . S2CID 14942345 .
links externos
-
 Mídia relacionada a alótropos de boro no Wikimedia Commons
Mídia relacionada a alótropos de boro no Wikimedia Commons