Síndrome de Hurler - Hurler syndrome
| Síndrome de Hurler | |
|---|---|
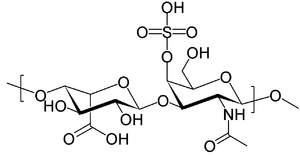 | |
| Estrutura do sulfato de dermatana , uma das moléculas que se acumulam nos lisossomos de pacientes com síndrome de Hurler | |
| Causas | Deficiência da enzima alfa-L iduronidase |
| Diagnóstico diferencial | Síndrome de Hurler-Scheie ; Síndrome de Scheie ; Síndrome de Hunter ; outras mucopolissacaridoses |
| Prognóstico | A morte geralmente ocorre antes dos 12 anos |
| Frequência | 1 em 100.000 |
A síndrome de Hurler , também conhecida como mucopolissacaridose Tipo IH ( MPS-IH ), doença de Hurler e anteriormente gárgula , é um distúrbio genético que resulta no acúmulo de grandes moléculas de açúcar chamadas glicosaminoglicanos (GAGs) nos lisossomos . A incapacidade de quebrar essas moléculas resulta em uma ampla variedade de sintomas causados por danos a vários sistemas de órgãos diferentes , incluindo, mas não se limitando ao sistema nervoso , sistema esquelético , olhos e coração .
O mecanismo subjacente é uma deficiência de alfa-L iduronidase , uma enzima responsável por quebrar os GAGs. Sem essa enzima, ocorre um acúmulo de sulfato de dermatan e sulfato de heparan no corpo. Os sintomas aparecem durante a infância e geralmente ocorre a morte prematura. Outras formas menos graves de MPS Tipo I incluem a Síndrome de Hurler-Scheie (MPS-IHS) e a Síndrome de Scheie (MPS-IS).
A síndrome de Hurler é classificada como uma doença de armazenamento lisossomal . Está clinicamente relacionada à síndrome de Hunter (MPS II); no entanto, a síndrome de Hunter está ligada ao X , enquanto a síndrome de Hurler é autossômica recessiva .
sinais e sintomas
Crianças com síndrome de Hurler podem parecer normais ao nascimento e desenvolver sintomas durante os primeiros anos de vida. Os sintomas variam entre os pacientes.
Uma das primeiras anormalidades que podem ser detectadas é o enrugamento das características faciais; esses sintomas podem começar aos 3–6 meses de idade. A cabeça pode ser grande com ossos frontais proeminentes . O crânio pode ser alongado . O nariz pode ter uma ponte nasal achatada com secreção nasal contínua. As órbitas oculares podem estar bem espaçadas e os olhos podem projetar-se do crânio. Os lábios podem ser grandes e as crianças afetadas podem manter suas mandíbulas abertas constantemente. As anormalidades esqueléticas ocorrem por volta dos 6 meses de idade, mas podem não ser clinicamente óbvias até os 10–14 meses. Os pacientes podem apresentar deformidades debilitantes da coluna e do quadril, síndrome do túnel do carpo e rigidez articular. Os pacientes podem ter altura normal na infância, mas param de crescer aos 2 anos de idade. Eles não podem atingir uma altura superior a 4 pés.
Outros sintomas iniciais podem incluir hérnias inguinais e umbilicais . Eles podem estar presentes no nascimento ou podem se desenvolver nos primeiros meses de vida. O turvamento da córnea e a degeneração retinal podem ocorrer durante o primeiro ano de vida, levando à cegueira. O aumento do fígado e do baço são comuns. Não há disfunção orgânica, mas a deposição de GAG nesses órgãos pode levar a um aumento maciço de tamanho. Os pacientes também podem ter diarreia . Pode ocorrer doença da válvula aórtica .
A obstrução das vias aéreas é frequente, geralmente secundária a vértebras cervicais anormais. As infecções do trato respiratório superior e inferior podem ser frequentes.
O atraso no desenvolvimento pode se tornar aparente aos 1–2 anos de idade, com idade funcional máxima de 2–4 anos. Segue-se uma deterioração progressiva. A maioria das crianças desenvolve capacidades limitadas de linguagem. A morte geralmente ocorre por volta dos 10 anos.
Mecanismos
O gene IDUA é responsável pela codificação de uma enzima chamada alfa-L-iduronidase. Por meio da hidrólise , a alfa-L-iduronidase é responsável por quebrar uma molécula chamada ácido alfa-L-idurônico não sulfatado . Este é um ácido urônico encontrado nos GAGs dermatan sulfato e heparan sulfato. A enzima alfa-L-iduronidase está localizada nos lisossomas. Sem função enzimática suficiente, esses GAGs não podem ser digeridos adequadamente.
Genética
Crianças com síndrome de Hurler carregam duas cópias defeituosas do gene IDUA , que foi mapeado para o local 4p16.3 no cromossomo 4 . Este é o gene que codifica a proteína iduronidase. Em 2018, mais de 201 mutações diferentes no gene IDUA causaram a MPS I.
Como a síndrome de Hurler é um transtorno autossômico recessivo , as pessoas afetadas têm duas cópias não funcionais do gene. Uma pessoa que nasce com uma cópia normal e uma com defeito é chamada de portador . Eles produzirão menos α-L-iduronidase do que um indivíduo com duas cópias normais do gene. A produção reduzida da enzima em portadores, entretanto, permanece suficiente para o funcionamento normal; a pessoa não deve apresentar nenhum sintoma da doença.
Diagnóstico
O diagnóstico geralmente pode ser feito por meio de exame clínico e testes de urina (o excesso de mucopolissacarídeos é excretado na urina ). Ensaios enzimáticos (teste de uma variedade de células ou fluidos corporais em cultura para deficiência enzimática) também são usados para fornecer o diagnóstico definitivo de uma das mucopolissacaridoses. O diagnóstico pré-natal por meio de amniocentese e biópsia de vilo corial pode verificar se um feto carrega uma cópia do gene defeituoso ou está afetado pelo distúrbio. O aconselhamento genético pode ajudar os pais com histórico familiar de mucopolissacaridoses a determinar se são portadores do gene mutado que causa os distúrbios.
Classificação
Todos os membros da família da mucopolissacaridose também são doenças de depósito lisossomal . A mucopolissacaridose tipo I (MPS I) é dividida em três subtipos com base na gravidade dos sintomas. Todos os três tipos resultam na ausência ou diminuição do funcionamento da mesma enzima. A MPS-IH (síndrome de Hurler) é o mais grave dos subtipos da MPS I. Os outros dois tipos são MPS-IS ( síndrome de Scheie ) e MPS-IHS ( síndrome de Hurler-Scheie ).
Devido à sobreposição substancial entre a síndrome de Hurler, a síndrome de Hurler-Scheie e a síndrome de Scheie, algumas fontes consideram esses termos desatualizados. Em vez disso, o MPS I pode ser dividido em formas "graves" e "atenuadas".
Tratamento
Atualmente não há cura para a Síndrome de Hurler. A terapia de reposição enzimática com iduronidase (Aldurazyme) pode melhorar a função pulmonar e a mobilidade. Pode reduzir a quantidade de carboidratos armazenados indevidamente nos órgãos. A correção cirúrgica das deformidades das mãos e pés pode ser necessária. A cirurgia da córnea pode ajudar a aliviar problemas de visão.
O transplante de medula óssea (BMT) e o transplante de sangue do cordão umbilical (UCBT) podem ser usados como tratamentos para MPS I. O BMT de irmãos com genes HLA idênticos e de parentes com genes HLA semelhantes pode melhorar significativamente a sobrevivência, função cognitiva e sintomas físicos. Os pacientes podem desenvolver doença enxerto contra hospedeiro ; isso é mais provável em doadores não irmãos. Em um estudo de 1998, crianças com irmãos doadores HLA idênticos tiveram uma sobrevida de 5 anos de 75%; crianças com doadores não irmãos tiveram uma sobrevida de 5 anos de 53%.
Freqüentemente, as crianças não têm acesso a um doador de medula óssea adequado. Nesses casos, o UCBT de doadores não aparentados pode aumentar a sobrevida, diminuir os sinais físicos da doença e melhorar a cognição. As complicações desse tratamento podem incluir doença do enxerto contra o hospedeiro .
Prognóstico
Um estudo britânico de 2008 encontrou uma expectativa de vida média estimada de 8,7 anos para pacientes com síndrome de Hurler. Em comparação, a expectativa de vida média para todas as formas de MPS tipo I era de 11,6 anos. Os pacientes que receberam transplantes de medula óssea com sucesso tiveram uma taxa de sobrevivência de 2 anos de 68% e uma taxa de sobrevivência de 10 anos de 64%. Os pacientes que não receberam transplante de medula óssea tiveram uma expectativa de vida significativamente reduzida, com uma idade média de 6,8 anos.
Epidemiologia
A síndrome de Hurler tem uma frequência geral de um por 100.000. Combinadas, todas as mucopolissacaridoses têm uma frequência de aproximadamente um em cada 25.000 nascimentos nos Estados Unidos.
Pesquisar
Terapia de genes
Existe um grande interesse no tratamento da MPS I com terapia genética . Em modelos animais, a entrega do gene da iduronidase foi realizada com retrovírus , adenovírus , vírus adeno-associados e vetores de plasmídeo . Camundongos e cães com MPS I foram tratados com sucesso com terapia genética. A maioria dos vetores pode corrigir a doença no fígado e no baço e pode corrigir os efeitos cerebrais com uma dosagem alta. A terapia gênica melhorou a sobrevida, os sintomas neurológicos e físicos; no entanto, alguns animais desenvolveram tumores hepáticos inexplicáveis. Se os problemas de segurança puderem ser resolvidos, a terapia genética pode fornecer um tratamento humano alternativo para os distúrbios da MPS no futuro.
A Sangamo Therapeutics , sediada em Richmond, Califórnia , está atualmente conduzindo um ensaio clínico envolvendo a edição de genes usando a nuclease de dedo de zinco (ZFN) para o tratamento de MPS I.
História
Em 1919, Gertrud Hurler , uma pediatra alemã, descreveu uma síndrome envolvendo opacificação da córnea, anormalidades esqueléticas e retardo mental. Uma doença semelhante de "gárgula" foi descrita em 1917 por Charles A. Hunter. Hurler não mencionou o artigo de Hunter. Por causa das interrupções de comunicação causadas pela Primeira Guerra Mundial , é provável que ela não soubesse de seu estudo. A síndrome de Hurler agora se refere a MPS IH, enquanto a síndrome de Hunter se refere a MPS II. Em 1962, uma forma mais branda de MPS I foi identificada por Scheie, levando à designação de síndrome de Scheie.
Veja também
- Síndrome de Hunter (MPS II)
- Síndrome de Sanfilippo (MPS III)
- Síndrome de Morquio (MPS IV)
- Síndrome de Maroteaux-Lamy (MPS VI)
Referências
links externos
| Classificação | |
|---|---|
| Fontes externas |



