Ligação metal-metal - Metal–metal bond
Na química inorgânica , as ligações metal-metal descrevem interações atraentes entre os centros metálicos. Os exemplos mais simples são encontrados em complexos bimetálicos. As ligações metal-metal podem ser "suportadas", ou seja, acompanhadas por um ou mais ligantes de ponte , ou "não suportadas". Eles também podem variar de acordo com a ordem do título. O tópico da ligação metal-metal é geralmente discutido no âmbito da química de coordenação , mas o tópico está relacionado à ligação metálica estendida , que descreve as interações entre metais em sólidos estendidos, como metais a granel e subhaletos de metal.
Ligações metal-metal não suportadas
O principal exemplo de um complexo com uma ligação metal-metal sem suporte é o dimanganês decacarbonil , Mn 2 (CO) 10 . Muitos aglomerados de metal contêm várias ligações M – M sem suporte. Alguns exemplos são M 3 (CO) 12 (M = Ru, Os) e Ir 4 (CO) 12 .
Uma subclasse de matrizes ligadas metal-metal sem suporte são compostos de cadeia linear . Em tais casos, a ligação M – M é fraca, conforme sinalizado por ligações M – M mais longas e a tendência de tais compostos se dissociarem em solução.
Ligações de metal-metal suportadas
Um exemplo inicial de uma ligação metal-metal suportada é o dímero de dicarbonil de ciclopentadieniliron , [(C 5 H 5 ) Fe (CO) 2 ] 2 . Nos isômeros predominantes deste complexo, os dois centros de Fe são unidos não apenas por uma ligação Fe-Fe, mas também por ligantes de CO em ponte . O dímero de dicarbonil ciclopentadienilrutênio relacionado apresenta uma ligação Ru – Ru sem suporte. Muitos aglomerados de metal contêm várias ligações M – M suportadas. Alguns exemplos são Fe 3 (CO) 12 e Co 4 (CO) 12 .
Múltiplas ligações metal-metal
Hexa ( terc- butoxi) ditungstênio (III) , apresentando uma ligação tripla W – W.
Acetato de cromo (II) , apresentando uma ligação quádrupla metal-metal.
Além das ligações simples M – M, os pares de metais podem ser ligados por ligações duplas, triplas, quádruplas e, em alguns casos, quíntuplas . Complexos isoláveis com ligações múltiplas são mais comuns entre os metais de transição no meio do bloco d , como rênio , tungstênio , tecnécio , molibdênio e cromo . Os co- ligantes típicos são doadores π, não aceitadores π. Exemplos bem estudados são as tetra acetatos , tais como dimolybdenum tetra-acetato (ligação quádruplo) e tetra-acetato de dirhodium (ligação simples). Os tetraacetatos de drutênio de valência mista têm ordens de ligação M – M fracionárias, ou seja, 2,5 para [Ru 2 (OAc) 4 (H 2 O) 2 ] + .
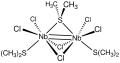
Os complexos Nb 2 X 6 (SR 2 ) 3 adotam uma estrutura bioctaédrica de compartilhamento de face (X = Cl, Br; SR 2 = tioéter). Como dímeros de Nb (III), apresentam duplas ligações metal-metal, o máximo possível para um par de metais com configuração d 2 . Hexa ( terc- butoxi) ditungstênio (III) é um exemplo bem estudado de um complexo com uma ligação tripla metal-metal.
Referências
- ^ Berry, John F .; Lu, Connie C. (2017). "Metal-Metal Bonds: From Fundamentals to Applications" . Química Inorgânica . 56 (14): 7577–7581. doi : 10.1021 / acs.inorgchem.7b01330 . PMID 28715854 .
- ^ Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ^ Radius, U .; Breher, F. (2006). " ' Para passar corajosamente a ligação quádrupla metal-metal". Angew. Chem. Int. Ed. 45 (19): 3006–3010. doi : 10.1002 / anie.200504322 . PMID 16642513 .
- ^ Algodão, FA; Walton, RA (1993). Várias ligações entre átomos de metal . Oxford: Oxford University Press . ISBN 0-19-855649-7.
- ^ Aquino, Manuel AS (1998). "Tetracarboxilatos de dirutênio e diosmio: Síntese, propriedades físicas e aplicações". Revisões de Química de Coordenação . 170 : 141–202. doi : 10.1016 / S0010-8545 (97) 00079-9 .
- ^ Kakeya, Masaki; Fujihara, Takashi; Nagasawa, Akira (2006). "Di-μ-cloro-μ- (sulfeto de dimetil) -bis [dicloro (sulfeto de dimetil) nióbio (III)]". Acta Crystallographica Secção E . 62 (3): m553 – m554. doi : 10.1107 / S1600536806005149 .
- ^ Broderick, Erin M .; Browne, Samuel C .; Johnson, Marc JA (2014). "Dimolibdênio e hexa de ditungstênio (alcóxidos)". Sínteses inorgânicas . 36 : 95–102. doi : 10.1002 / 9781118744994.ch18 .