Receptor ativado por proliferador de peroxissoma - Peroxisome proliferator-activated receptor
No campo da biologia molecular , os receptores ativados por proliferadores de peroxissoma ( PPARs ) são um grupo de proteínas receptoras nucleares que funcionam como fatores de transcrição reguladores da expressão de genes . PPARs desempenham papéis essenciais na regulação da diferenciação celular , desenvolvimento e metabolismo ( carboidratos , lipídios , proteínas ) e tumorigênese de organismos superiores.
Nomenclatura e distribuição de tecidos
| Receptor alfa ativado por proliferador de peroxissoma | |||||||
|---|---|---|---|---|---|---|---|
| Identificadores | |||||||
| Símbolo | PPARA | ||||||
| Alt. símbolos | PPAR | ||||||
| Gene NCBI | 5465 | ||||||
| HGNC | 9232 | ||||||
| OMIM | 170998 | ||||||
| RefSeq | NM_001001928 | ||||||
| UniProt | Q07869 | ||||||
| Outros dados | |||||||
| Locus | Chr. 22 q12-q13.1 | ||||||
| |||||||
| Receptor gama ativado por proliferador de peroxissoma | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Identificadores | |||||||
| Símbolo | PPARG | ||||||
| Gene NCBI | 5468 | ||||||
| HGNC | 9236 | ||||||
| OMIM | 601487 | ||||||
| RefSeq | NM_005037 | ||||||
| UniProt | P37231 | ||||||
| Outros dados | |||||||
| Locus | Chr. 3 p25 | ||||||
| |||||||
| Delta do receptor ativado por proliferador de peroxissoma | |||||||
|---|---|---|---|---|---|---|---|
| Identificadores | |||||||
| Símbolo | PPARD | ||||||
| Gene NCBI | 5467 | ||||||
| HGNC | 9235 | ||||||
| OMIM | 600409 | ||||||
| RefSeq | NM_006238 | ||||||
| UniProt | Q03181 | ||||||
| Outros dados | |||||||
| Locus | Chr. 6 p21.2 | ||||||
| |||||||
Três tipos de PPARs foram identificados: alfa, gama e delta (beta):
- α (alfa) - expresso no fígado , rim , coração , músculo , tecido adiposo e outros
- β / δ (beta / delta) - expresso em muitos tecidos, mas marcadamente no cérebro , tecido adiposo e pele
-
γ (gama) - embora transcrito pelo mesmo gene, este PPAR por meio de splicing alternativo é expresso em três formas:
- γ1 - expresso em praticamente todos os tecidos, incluindo coração , músculo , cólon , rim , pâncreas e baço
- γ2 - expresso principalmente no tecido adiposo (30 aminoácidos a mais do que γ1)
- γ3 - expresso em macrófagos , intestino grosso , tecido adiposo branco .
História
Os PPARs foram originalmente identificados em rãs Xenopus como receptores que induzem a proliferação de peroxissomos nas células. O primeiro PPAR (PPARα) foi descoberto durante a busca de um alvo molecular para um grupo de agentes então denominado proliferadores de peroxissoma , pois aumentavam o número de peroxissomas no tecido hepático de roedores, além de melhorar a sensibilidade à insulina . Esses agentes, farmacologicamente relacionados aos fibratos, foram descobertos no início da década de 1980. Quando se descobriu que os PPARs desempenhavam um papel muito mais versátil na biologia, os agentes foram, por sua vez, denominados ligantes de PPAR . Os ligantes PPAR mais conhecidos são as tiazolidinedionas ; Veja abaixo para mais detalhes.
Depois que o PPARδ (delta) foi identificado em humanos em 1992, ele mostrou estar intimamente relacionado ao PPARβ (beta) previamente descrito durante o mesmo ano em outros animais ( Xenopus ). O nome PPARδ é geralmente usado nos EUA, enquanto o uso da denominação PPARβ permaneceu na Europa, onde esse receptor foi inicialmente descoberto no Xenopus .
Os PPARs foram assim chamados porque foram descobertos que induzem a proliferação de peroxissomas em roedores, mas não se acredita que a indução da proliferação de peroxissomas ocorra em humanos.
Função fisiológica
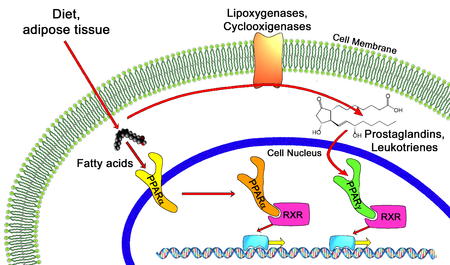
Todos os PPARs se heterodimerizam com o receptor retinóide X (RXR) e se ligam a regiões específicas no DNA de genes alvo. Essas sequências de DNA são denominadas PPREs ( elementos de resposta do hormônio proliferador de peroxissoma ). A sequência de consenso de DNA é AGGTCANAGGTCA, com N sendo qualquer nucleotídeo . Em geral, essa sequência ocorre na região promotora de um gene e, quando o PPAR se liga ao seu ligante, a transcrição dos genes-alvo é aumentada ou diminuída, dependendo do gene. O RXR também forma um heterodímero com vários outros receptores (por exemplo, vitamina D e hormônio da tireoide ).
A função dos PPARs é modificada pela forma precisa do seu domínio de ligação ao ligante (ver abaixo) induzido pela ligação do ligante e por uma série de proteínas coativadoras e corepressoras , cuja presença pode estimular ou inibir a função do receptor, respectivamente.
Ligantes endógenos para os PPARs incluem ácidos graxos livres , eicosanóides e vitamina B3 . O PPARγ é ativado por PGJ 2 (uma prostaglandina ) e certos membros da família 5-HETE de metabólitos do ácido araquidônico, incluindo 5-oxo-15 (S) -HETE e 5-oxo-ETE. Em contraste, o PPARα é ativado pelo leucotrieno B 4 . Certos membros da família do ácido 15-hidroxieicosatetraenóico de metabólitos do ácido araquidônico, incluindo 15 (S) -HETE, 15 (R) -HETE e 15-HpETE ativam em vários graus PPAR alfa, beta / delta e gama. Além disso, foi relatado que o PPARγ está envolvido na patogênese e no crescimento do câncer. A ativação do PPARγ pelo agonista RS5444 pode inibir o crescimento do câncer anaplásico da tireoide. Consulte Recursos para uma revisão e crítica dos papéis do PPAR gama no câncer.
Genética
As três formas principais são transcritas a partir de genes diferentes :
- PPARα - cromossomo 22q 12-13.1 (OMIM 170998 )
- PPARβ / δ - cromossomo 6p 21,2-21,1 (OMIM 600409 )
- PPARγ - cromossomo 3p 25 (OMIM 601487 ).
Foram descritos distúrbios hereditários de todos os PPARs, geralmente levando a uma perda de função e lipodistrofia concomitante , resistência à insulina e / ou acantose nigricante . De PPARγ , uma mutação de ganho de função foi descrita e estudada ( Pro 12 Ala ) que diminuiu o risco de resistência à insulina ; é bastante prevalente ( frequência do alelo 0,03 - 0,12 em algumas populações). Em contraste, o pro 115 gln está associado à obesidade . Alguns outros polimorfismos têm alta incidência em populações com elevados índices de massa corporal.
Estrutura
Como outros receptores nucleares, os PPARs são modulares na estrutura e contêm os seguintes domínios funcionais :
- (A / B) região N-terminal
- (C) DBD ( domínio de ligação ao DNA )
- (D) região de dobradiça flexível
- (E) LBD (domínio de ligação do ligante)
- (F) região C-terminal
O DBD contém dois motivos de dedo de zinco , que se ligam a sequências específicas de DNA conhecidas como elementos de resposta hormonal quando o receptor é ativado. O LBD tem uma extensa estrutura secundária que consiste em 13 hélices alfa e uma folha beta . Ligantes naturais e sintéticos ligam-se ao LBD, ativando ou reprimindo o receptor.
Farmacologia e moduladores PPAR
PPARα e PPARγ são os alvos moleculares de vários medicamentos comercializados . Por exemplo, os fibratos hipolipidêmicos ativam o PPARα e as tiazolidinedionas antidiabéticas ativam o PPARγ. O ácido perfluorooctanóico sintético ativa o PPARα, enquanto o ácido perfluorononanóico sintético ativa o PPARα e o PPARγ. A berberina ativa o PPARγ, assim como outros compostos naturais de diferentes classes químicas.
Veja também
Referências
links externos
- [1] (Página de recursos do PPAR, Penn State University).
- [2] (Recurso de Receptor Nuclear).
- Esboço de referência do PPAR (Rutgers University).
- Peroxissomo + Proliferator-Activated + Receptors na Biblioteca Nacional de Medicina dos EUA Medical Subject Headings (MeSH)
- Proteopedia Peroxisome_Proliferator-Activated_Receptors - a Estrutura do Receptor Peroxisome Proliferator-Activated em 3D Interativo