Níquel de Raney - Raney nickel
 Níquel Raney ativado a seco
|
|
| Identificadores | |
|---|---|
| UNII | |
| Propriedades | |
| Aparência | Pó cinza claro |
| Perigos | |
| Pictogramas GHS |
  
|
| H250 , H317 , H351 , H372 , H412 | |
| P210 , P273 , P280 , P302 | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
Níquel de Raney / r eɪ n i n ɪ k əl / , também chamado níquel esponjoso , é um sólido constituído principalmente de granulação fina- níquel derivado de um níquel de alumínio de liga. Vários graus são conhecidos, dos quais a maioria são sólidos cinzentos. Alguns são pirofóricos , mas a maioria é usada como pasta estável ao ar. O níquel de Raney é usado como reagente e como catalisador em química orgânica . Foi desenvolvido em 1926 pelo engenheiro americano Murray Raney para a hidrogenação de óleos vegetais.
Nomenclatura
Uma vez que Raney é uma marca registrada da WR Grace and Company , apenas os produtos produzidos por sua Divisão Grace são apropriadamente chamados de "níquel de Raney". Os termos mais genéricos "catalisador esquelético" ou "catalisador de metal esponja" podem referir-se a catalisadores com propriedades físicas e químicas semelhantes às do níquel de Raney. No entanto, uma vez que a própria Grace Company não usa nenhum nome genérico para os catalisadores que fornece, "Raney" pode se tornar genérico de acordo com a lei de marcas dos Estados Unidos .
Preparação
Preparação de liga

A liga de Ni-Al é preparada dissolvendo níquel em alumínio fundido seguido de resfriamento ("têmpera"). Dependendo da razão Ni: Al, a têmpera produz várias fases diferentes. Durante o procedimento de têmpera, pequenas quantidades de um terceiro metal, como zinco ou cromo, são adicionadas para aumentar a atividade do catalisador resultante. Este terceiro metal é chamado de " promotor ". O promotor muda a mistura de uma liga binária para uma liga ternária, o que pode levar a diferentes propriedades de têmpera e lixiviação durante a ativação.
Ativação
No processo de ativação, a liga, geralmente na forma de pó fino, é tratada com uma solução concentrada de hidróxido de sódio . A reação de lixiviação simplificada é dada pela seguinte equação química :
- 2 Al + 2 NaOH + 6 H 2 O → 2 Na [Al (OH) 4 ] + 3 H 2
A formação de aluminato de sódio (Na [Al (OH) 4 ]) requer que soluções de alta concentração de hidróxido de sódio sejam usadas para evitar a formação de hidróxido de alumínio , que de outra forma precipitaria como bayerita . Portanto, soluções de hidróxido de sódio com concentrações de até 5 M são usadas.
A temperatura usada para lixiviar a liga tem um efeito marcante nas propriedades do catalisador. Normalmente, a lixiviação é conduzida entre 70 e 100 ° C. A área superficial do níquel de Raney (e catalisadores relacionados em geral) tende a diminuir com o aumento da temperatura de lixiviação. Isso ocorre devido a rearranjos estruturais dentro da liga que podem ser considerados análogos à sinterização , onde os ligamentos da liga começariam a aderir uns aos outros em temperaturas mais altas, levando à perda da estrutura porosa.
Durante o processo de ativação, o Al é lixiviado das fases NiAl 3 e Ni 2 Al 3 que estão presentes na liga, enquanto a maior parte do Ni permanece, na forma de NiAl. A remoção do Al de algumas fases, mas não de outras, é conhecida como " lixiviação seletiva ". Foi demonstrado que a fase NiAl fornece a estabilidade estrutural e térmica do catalisador. Como resultado, o catalisador é bastante resistente à decomposição ("quebra", comumente conhecido como "envelhecimento"). Essa resistência permite que o níquel de Raney seja armazenado e reutilizado por um período prolongado; no entanto, preparações frescas são geralmente preferidas para uso em laboratório. Por esta razão, o níquel Raney comercial está disponível nas formas "ativa" e "inativa".
Antes do armazenamento, o catalisador pode ser lavado com água destilada à temperatura ambiente para remover o aluminato de sódio remanescente. Água sem oxigênio ( desgaseificada ) é preferida para armazenamento para evitar a oxidação do catalisador, o que aceleraria seu processo de envelhecimento e resultaria em redução da atividade catalítica.
Propriedades
Macroscopicamente, o níquel de Raney é um pó cinza finamente dividido. Microscopicamente, cada partícula desse pó é uma malha tridimensional , com poros de tamanho e formato irregulares, cuja grande maioria é criada durante o processo de lixiviação. O níquel de Raney é notável por ser térmica e estruturalmente estável, além de ter uma grande área de superfície Brunauer - Emmett - Teller ( BET ). Essas propriedades são um resultado direto do processo de ativação e contribuem para uma atividade catalítica relativamente alta.
A área de superfície é normalmente determinada por uma medição BET usando um gás que é preferencialmente adsorvido em superfícies metálicas, como o hidrogênio . Usando este tipo de medição, quase toda a área exposta em uma partícula do catalisador mostrou ter Ni em sua superfície. Como o Ni é o metal ativo do catalisador, uma grande área de superfície de Ni implica que uma grande superfície esteja disponível para que as reações ocorram simultaneamente, o que se reflete em um aumento da atividade do catalisador. Comercialmente disponível de níquel de Raney tem uma área de superfície média de Ni de cerca de 100 m 2 por grama de catalisador.
Uma alta atividade catalítica, associada ao fato de que o hidrogênio é absorvido pelos poros do catalisador durante a ativação, torna o níquel de Raney um catalisador útil para muitas reações de hidrogenação . Sua estabilidade estrutural e térmica (ou seja, não se decompõe em altas temperaturas) permite seu uso em uma ampla gama de condições de reação. Além disso, a solubilidade do níquel de Raney é desprezível na maioria dos solventes de laboratório comuns, com exceção dos ácidos minerais como o ácido clorídrico, e sua densidade relativamente alta (cerca de 6,5 g cm- 3 ) também facilita sua separação de uma fase líquida após uma reação está completo.
Formulários
O níquel de Raney é utilizado em um grande número de processos industriais e em síntese orgânica devido à sua estabilidade e alta atividade catalítica à temperatura ambiente.
Aplicações industriais
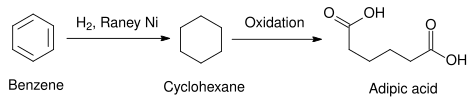
Um exemplo prático do uso do níquel de Raney na indústria é mostrado na reação a seguir, onde o benzeno é reduzido a ciclohexano . A redução do anel de benzeno é muito difícil de conseguir por outros meios químicos, mas pode ser realizada usando níquel de Raney. Outros catalisadores heterogêneos, como aqueles que usam elementos do grupo da platina , podem ser usados em vez disso, com efeito semelhante, mas tendem a ser mais caros de produzir do que o níquel de Raney. O ciclohexano assim produzido pode ser utilizado na síntese do ácido adípico , matéria-prima utilizada na produção industrial de poliamidas como o náilon.
Outras aplicações industriais de níquel Raney incluem a conversão de:
- Dextrose em sorbitol ;
- Compostos nitro para aminas , por exemplo, 2,4- dinitrotolueno para 2,4-toluenodiamina;
- Nitrilos para aminas, por exemplo, estearonitrilo para estearilamina e adiponitrilo para hexametilenodiamina ;
- Olefinas em parafinas , por exemplo, sulfoleno em sulfolano ;
- Acetilenos para parafinas, por exemplo, 1,4-butinodiol para 1,4-butanodiol .
Aplicações em síntese orgânica
Dessulfuração
O níquel de Raney é usado em síntese orgânica para dessulfuração . Por exemplo, os tioacetais serão reduzidos a hidrocarbonetos na última etapa da redução de Mozingo :
Tióis e sulfetos podem ser removidos de compostos alifáticos , aromáticos ou heteroaromáticos. Da mesma forma, o níquel de Raney removerá o enxofre do tiofeno para dar um alcano saturado .
Redução de grupos funcionais
É normalmente usado na redução de compostos com ligações múltiplas , como alcinos , alcenos , nitrilos , dienos , compostos aromáticos e contendo carbonil . Além disso, o níquel de Raney reduzirá as ligações heteroátomo-heteroátomo, como hidrazinas , grupos nitro e nitrosaminas. Também encontrou uso na alquilação redutiva de aminas e na aminação de álcoois.
Ao reduzir uma ligação dupla carbono-carbono, o níquel de Raney adicionará hidrogênio de maneira sincrônica .
Segurança
Devido à sua grande área superficial e alto volume de gás hidrogênio contido, o níquel de Raney ativado e seco é um material pirofórico que requer manuseio sob uma atmosfera inerte . O níquel de Raney é normalmente fornecido como uma pasta de 50% em água. Mesmo após a reação, o níquel de Raney residual contém quantidades significativas de gás hidrogênio e pode inflamar-se espontaneamente quando exposto ao ar.
Além disso, a exposição aguda ao níquel de Raney pode causar irritação do trato respiratório e das cavidades nasais e causar fibrose pulmonar se inalado. A ingestão pode causar convulsões e distúrbios intestinais. Também pode causar irritação nos olhos e na pele. A exposição crônica pode causar pneumonite e outros sinais de sensibilização ao níquel, como erupções cutâneas ("coceira de níquel").
|
NFPA 704 Fire Diamond | |
|---|---|
O níquel também é classificado como um possível carcinógeno humano pelo IARC (Grupo 2B, categoria 3 da UE ) e teratógeno , enquanto a inalação de partículas finas de óxido de alumínio está associada à doença de Shaver .
A natureza pirofórica do níquel de Raney iniciou o desenvolvimento de catalisadores à base de siliceto de níquel mais seguros com propriedades catalíticas semelhantes.
Desenvolvimento
Murray Raney formou-se engenheiro mecânico pela University of Kentucky em 1909. Em 1915 ingressou na Lookout Oil and Refining Company no Tennessee e foi responsável pela instalação de células eletrolíticas para a produção de hidrogênio que era usado na hidrogenação de óleos vegetais . Durante esse tempo, a indústria usava um catalisador de níquel preparado a partir de óxido de níquel (II) . Acreditando que melhores catalisadores poderiam ser produzidos, por volta de 1921 ele começou a realizar pesquisas independentes enquanto ainda trabalhava para a Lookout Oil. Em 1924, foi produzida uma liga de Ni / Si de proporção 1: 1 , que após tratamento com hidróxido de sódio, revelou ser cinco vezes mais ativa do que o melhor catalisador usado na hidrogenação do óleo de semente de algodão. Uma patente para esta descoberta foi emitida em dezembro de 1925.
Posteriormente, Raney produziu uma liga 1: 1 Ni / Al seguindo um procedimento semelhante ao usado para o catalisador de níquel-silício. Ele descobriu que o catalisador resultante era ainda mais ativo e entrou com um pedido de patente em 1926. Esta é agora uma composição de liga comum para os catalisadores de níquel Raney modernos. Outras composições de ligas comuns incluem 21:29 Ni / Al e 3: 7 Ni / Al. Ambos os protocolos de atividade e preparação para esses catalisadores variam.
Seguindo o desenvolvimento do níquel de Raney, outros sistemas de liga com alumínio foram considerados, dos quais os mais notáveis incluem cobre, rutênio e cobalto . Outras pesquisas mostraram que a adição de uma pequena quantidade de um terceiro metal à liga binária promoveria a atividade do catalisador. Alguns promotores amplamente usados são zinco, molibdênio e cromo . Uma maneira alternativa de preparar níquel de Raney enantiosseletivo foi concebida por adsorção superficial de ácido tartárico .
Veja também
- Alumineto de níquel
- Urushibara níquel
- Níquel de Rieke
- Catalisador boreto de níquel
- Cobalto Raney , um catalisador semelhante de liga de cobalto / alumínio que às vezes é mais seletivo para certos produtos de hidrogenação (por exemplo, aminas primárias por redução de nitrila ).
Referências
links externos
- Cartão Internacional de Segurança Química 0062
- Guia de bolso do NIOSH para perigos químicos
- Artigo de 1941 que descreve a preparação de níquel de Raney de grau W-2: Mozingo, Ralph (1941). "Catalisador, níquel de Raney, W-2" . Sínteses orgânicas . 21 : 15. doi : 10.15227 / orgsyn.021.0015 .