Reação Retro-Diels-Alder - Retro-Diels–Alder reaction
A reação retro-Diels-Alder (rDA) é o reverso microscópico da reação Diels-Alder - a formação de um dieno e dienófilo a partir de um ciclohexeno . Pode ser realizado espontaneamente com calor ou com mediação ácida ou básica.
Em princípio, torna-se termodinamicamente favorável para as reações de Diels-Alder ocorrerem na direção reversa se a temperatura for alta o suficiente. Na prática, essa reação geralmente requer algumas características estruturais especiais para prosseguir em temperaturas de relevância sintética. Por exemplo, a clivagem do ciclohexeno para dar butadieno e etileno foi observada, mas apenas em temperaturas superiores a 800 K. Com uma força motriz apropriada, no entanto, a reação de Diels-Alder prossegue no sentido inverso sob condições relativamente suaves, fornecendo dieno e dienófilo de derivados de ciclohexeno de partida. Já em 1929, esse processo era conhecido e aplicado à detecção de ciclohexadienos, que liberavam etileno e compostos aromáticos após reagir com acetilenos por meio de uma sequência Diels-Alder / retro-Diels-Alder. Desde então, vários substratos foram submetidos ao rDA, produzindo muitos dienos e dienófilos diferentes. Além disso, a condução do rDA na presença de um dieno ou dienófilo eliminador levou à captura de muitas espécies reativas transitórias.
(1)

Mecanismo e estereoquímica
Mecanismo prevalecente
A reação retro-Diels-Alder propriamente dita é o reverso microscópico da reação Diels-Alder: um processo combinado (mas não necessariamente síncrono), pericíclico, de etapa única. A evidência da reação retro-Diels-Alder foi fornecida pela observação da isomerização endo - exo dos adutos de Diels-Alder. Foi postulado que, em altas temperaturas, a isomerização de adutos endo cinéticos para produtos exo mais termodinamicamente estáveis ocorreu por meio de uma sequência rDA / DA. No entanto, essa isomerização pode ocorrer por meio de um processo completamente intramolecular, [3,3] -sigmatrópico (Cope). A evidência para o último foi fornecida pela reação abaixo - nenhum isômero "cabeça a cabeça" foi obtido, sugerindo um processo de isomerização totalmente intramolecular.
(2)

Estereoquímica
Como a reação de Diels-Alder, o rDA preserva a configuração no dieno e no dienófilo. Muito menos se sabe sobre as taxas relativas de reversão de endo e exo adutos, e os estudos apontaram para nenhuma correlação entre a configuração relativa no material de partida de ciclohexeno e a taxa de reversão.
Escopo e limitações
Algumas reações rDA ocorrem espontaneamente à temperatura ambiente devido à alta reatividade ou volatilidade do dienófilo emitido. A maioria, entretanto, requer ativação térmica ou química adicional. As tendências relativas de uma variedade de dienos e dienófilos para se formar via rDA são descritas abaixo:
Dieno : furano , pirrol > benzeno > naftaleno > fulveno > ciclopentadieno > antraceno > butadieno
Dienófilo : N 2 > CO 2 > naftaleno > benzeno , nitrilos > metacrilato > maleimidas > ciclopentadieno , iminas , alcenos > alcinos
Dienófilos totalmente carbonados
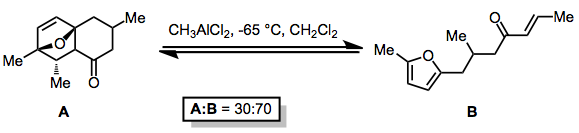
Como a reação de Diels-Alder troca duas ligações π por duas ligações σ, ela é intrinsecamente termodinamicamente favorecida na direção direta. No entanto, são conhecidas várias estratégias para superar esse viés termodinâmico inerente. A complexação de ácidos de Lewis à funcionalidade básica no material de partida pode induzir a reação retro-Diels-Alder, mesmo nos casos em que a reação direta é intramolecular.
(3)
A mediação de base pode ser usada para induzir rDA nos casos em que os produtos separados são menos básicos do que o material de partida. Essa estratégia tem sido usada, por exemplo, para gerar ânions ciclopentadienil aromáticos a partir de adutos de ciclopentadieno. Grupos de retirada de elétrons estrategicamente colocados no material de partida podem tornar este processo essencialmente irreversível.
(4)

Se o isolamento ou reação de um dieno ou dienófilo indescritível for o objetivo, uma de duas estratégias pode ser usada. A pirólise instantânea a vácuo de adutos de Diels-Alder sintetizados por meios independentes pode fornecer dienófilos extremamente reativos e de vida curta (que podem então ser capturados por um dieno único). Alternativamente, a reação de rDA pode ser realizada na presença de um eliminador. O eliminador reage com o dieno ou (mais tipicamente) com o dienófilo para direcionar o equilíbrio do processo retro-DA em direção aos produtos. Os cianoacrilatos altamente reativos podem ser isolados dos adutos de Diels-Alder (sintetizados independentemente) com o uso de um necrófago.
(5)

Dienófilos heteroatômicos
Os nitrilos podem ser liberados em reações rDA de adutos DA de pirimidinas ou pirazinas. As piridinas altamente substituídas resultantes podem ser de difícil acesso por outros meios.
(6)

A liberação de isocianatos de adutos de Diels-Alder de piridonas pode ser usada para gerar compostos aromáticos altamente substituídos. Os isocianatos podem ser isolados ou aprisionados se forem o produto desejado.
(7)

A liberação de nitrogênio de diazenos cíclicos de seis membros é comum e freqüentemente espontânea à temperatura ambiente. Neste exemplo particular, o epóxido mostrado sofre rDA a 0 ° C. O isômero com uma relação cis entre o diazeno e o epóxido reage somente após aquecimento a> 180 ° C.
(8)

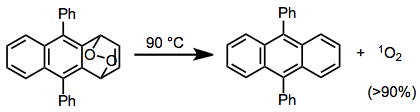
A liberação combinada de oxigênio via rDA resulta na formação de oxigênio singlete . Rendimentos muito altos de oxigênio singlete resultam de reações rDA de alguns peróxidos cíclicos - neste exemplo, foi obtido um rendimento superior a 90% de oxigênio singlete.
(9)
O dióxido de carbono é um dienófilo comum liberado durante as reações de rDA. Os adutos de Diels-Alder de alcinos e 2-pironas podem sofrer rDA para liberar dióxido de carbono e gerar compostos aromáticos.
(10)

Condições experimentais e procedimento
Condições típicas
A energia interna é o único fator que controla a extensão das reações de rDA, e a temperatura geralmente é a única variável citada para essas reações. Portanto, não há condições que possam ser consideradas "típicas". Para reações de rDA que fornecem um produto volátil, a remoção desse produto pode facilitar a reação, embora a maioria dessas reações (rDA de liberação de nitrogênio e oxigênio, por exemplo) sejam irreversíveis sem qualquer indução extra.
