Cianeto de amônio - Ammonium cyanide
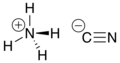
|
|

|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| NH 4 CN | |
| Massa molar | 44.0559 g / mol |
| Aparência | sólido cristalino incolor |
| Densidade | 1,02 g / cm 3 |
| Ponto de ebulição | 36 ° C (97 ° F; 309 K) |
| muito solúvel | |
| Solubilidade | muito solúvel em álcool |
| Compostos relacionados | |
|
Outros ânions
|
Hidróxido de amônio Azida de amônio Nitrato de amônio |
|
Outros cátions
|
Cianeto de sódio Cianeto de potássio |
|
Compostos relacionados
|
Cianeto de hidrogênio de amônia |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cianeto de amônio é um composto inorgânico instável com a fórmula NH 4 CN.
Usos
O cianeto de amônio é geralmente usado em síntese orgânica. Por ser instável, não é enviado ou vendido comercialmente.
Preparação
O cianeto de amônio é preparado em solução borbulhando cianeto de hidrogênio em amônia aquosa a baixa temperatura
- HCN + NH 3 (aq) → NH 4 CN (aq)
Pode ser preparado pela reação de cianeto de cálcio e carbonato de amônio :
- Ca (CN) 2 + (NH 4 ) 2 CO 3 → 2 NH 4 CN + CaCO 3
No estado seco, o cianeto de amônio é feito aquecendo uma mistura de cianeto de potássio ou ferrocianeto de potássio com cloreto de amônio e condensando os vapores em cristais de cianeto de amônio:
- KCN + NH 4 Cl → NH 4 CN + KCl
Reações
O cianeto de amônio se decompõe em amônia e cianeto de hidrogênio, muitas vezes formando um polímero preto de cianeto de hidrogênio:
- NH 4 CN → NH 3 + HCN
Ele sofre reações de decomposição dupla em solução com vários sais de metal.
Ele reage com o glioxal , produzindo glicina (ácido aminoacético):
- NH 4 CN + (CHO) 2 → NH 2 CH 2 COOH + HCN
As reações com cetonas produzem aminonitrilas , como na primeira etapa da síntese de aminoácidos de Strecker :
- NH 4 CN + CH 3 COCH 3 → (CH 3 ) 2 C (NH 2 ) CN + H 2 O
Toxicidade
O sólido ou sua solução é altamente tóxico. A ingestão pode causar a morte. A exposição ao sólido pode ser prejudicial, pois se decompõe em cianeto de hidrogênio altamente tóxico e amônia.
Análises químicas
O cianeto de amônio pode ser analisado aquecendo o sal e prendendo os produtos decompostos: cianeto de hidrogênio e amônia em água a baixas temperaturas. A solução aquosa é analisada quanto ao íon cianeto pelo método titulométrico de nitrato de prata ou um método de eletrodo seletivo de íons, e a amônia é medida por titulação ou técnica de eletrodo.
Notas
Referências
- AF Wells, Structural Inorganic Chemistry , 5ª ed., Oxford University Press, Oxford, UK, 1984.
