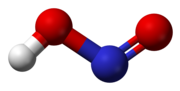
Ácido nitroso - Nitrous acid
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Ácido nitroso |
|
|
Nome IUPAC sistemático
Hidroxidooxidonitrogênio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3DMet | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.029.057 |
| Número EC | |
| 983 | |
| KEGG | |
| Malha | Nitroso + ácido |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| HNO 2 | |
| Massa molar | 47,013 g / mol |
| Aparência | Solução azul pálido |
| Densidade | Aproximadamente. 1 g / ml |
| Ponto de fusão | Conhecido apenas em solução ou como gás |
| Acidez (p K a ) | 3,15 |
| Base conjugada | Nitrito |
| Perigos | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Compostos relacionados | |
|
Outros ânions
|
Ácido nítrico |
|
Outros cátions
|
Nitrito de sódio Nitrito de potássio Nitrito de amônio |
|
Compostos relacionados
|
Trióxido de dinitrogênio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
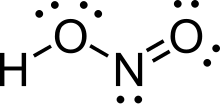
Ácido nitroso (fórmula molecular H N O
2) é um ácido monoprótico fraco conhecido apenas em solução , na fase gasosa e na forma de nitrito ( NO-
2) sais. O ácido nitroso é usado para fazer sais de diazônio a partir de aminas. Os sais de diazônio resultantes são reagentes em reações de acoplamento azo para dar corantes azo .
Estrutura
Na fase gasosa, a molécula de ácido nitroso planar pode adotar tanto a forma sin quanto a anti . A forma anti predomina à temperatura ambiente, e as medições de IV indicam que é mais estável em torno de 2,3 kJ / mol.
Dimensões da forma anti
(do espectro de microondas )Modelo da forma anti
Preparação
O ácido nitroso é geralmente gerado pela acidificação de soluções aquosas de nitrito de sódio com um ácido mineral . A acidificação é geralmente conduzida em temperaturas de gelo, e o HNO 2 é consumido in situ. O ácido nitroso livre é instável e se decompõe rapidamente.
O ácido nitroso também pode ser produzido dissolvendo trióxido de dinitrogênio em água de acordo com a equação
- N 2 O 3 + H 2 O → 2 HNO 2
Reações
O ácido nitroso é o principal quimíforo do reagente de Liebermann , usado para realizar testes pontuais de alcalóides.
Decomposição
O ácido nitroso gasoso, que raramente é encontrado, se decompõe em dióxido de nitrogênio , óxido nítrico e água:
- 2 HNO 2 → NO 2 + NO + H 2 O
O dióxido de nitrogênio é desproporcional em ácido nítrico e ácido nitroso em solução aquosa:
- 2 NO 2 + H 2 O → HNO 3 + HNO 2
Em soluções quentes ou concentradas, a reação geral resulta na produção de ácido nítrico, água e óxido nítrico:
- 3 HNO 2 → HNO 3 + 2 NO + H 2 O
O óxido nítrico pode ser posteriormente reoxidado pelo ar em ácido nítrico, tornando a reação geral:
- 2 HNO 2 + O 2 → 2 HNO 3
Redução
Com os íons I - e Fe 2+ , o NO é formado:
- 2 KNO 2 + 2 KI + 2 H 2 SO 4 → I 2 + 2 NO + 2 H 2 O + 2 K 2 SO 4
- 2 KNO 2 + 2 FeSO 4 + 2 H 2 SO 4 → Fe 2 (SO 4 ) 3 + 2 NO + 2 H 2 O + K 2 SO 4
Com íons Sn 2+ , N 2 O é formado:
- 2 KNO 2 + 6 HCl + 2 SnCl 2 → 2 SnCl 4 + N 2 O + 3 H 2 O + 2 KCl
Com o gás SO 2 , NH 2 OH é formado:
- 2 KNO 2 + 6 H 2 O + 4 SO 2 → 3 H 2 SO 4 + K 2 SO 4 + 2 NH 2 OH
Com Zn em solução alcalina, NH 3 é formado:
- 5 H 2 O + KNO 2 + 3 Zn → NH 3 + KOH + 3 Zn (OH) 2
Com N
2H+
5, HN 3 e, subsequentemente, o gás N 2 é formado:
- HNO 2 + [N 2 H 5 ] + → HN 3 + H 2 O + H 3 O +
- HNO 2 + HN 3 → N 2 O + N 2 + H 2 O
A oxidação por ácido nitroso tem um controle cinético sobre o controle termodinâmico . Isso é mais bem ilustrado que o ácido nitroso diluído é capaz de oxidar I - a I 2 , mas o ácido nítrico diluído não.
- I 2 + 2 e - ⇌ 2 I - E o = +0,54 V
-
NÃO-
3+ 3 H + + 2 e - ⇌ HNO 2 + H 2 O E o = +0,93 V
- HNO 2 + H + + e - ⇌ NO + H 2 O E o = +0,98 V
Pode-se ver que os valores de Eo
celularpois essas reações são semelhantes, mas o ácido nítrico é um agente oxidante mais poderoso. Com base no fato de que o ácido nitroso diluído pode oxidar o iodeto em iodo , pode-se deduzir que o nitro é um agente oxidante mais rápido, em vez de mais poderoso, do que o ácido nítrico diluído.
Química orgânica
O ácido nitroso é usado para preparar sais de diazônio :
- HNO 2 + ArNH 2 + H + → ArN+
2 + 2 H 2 O
onde Ar é um grupo aril .
Esses sais são amplamente usados em síntese orgânica , por exemplo, para a reação de Sandmeyer e na preparação de corantes azo , compostos de cores vivas que são a base de um teste qualitativo para anilinas . O ácido nitroso é usado para destruir a azida de sódio tóxica e potencialmente explosiva . Para a maioria dos propósitos, o ácido nitroso é geralmente formado in situ pela ação do ácido mineral sobre o nitrito de sódio : é principalmente de cor azul
- NaNO 2 + HCl → HNO 2 + NaCl
- 2 NaN 3 + 2 HNO 2 → 3 N 2 + 2 NO + 2 NaOH
A reação com dois átomos de hidrogênio α nas cetonas cria oximas , que podem ser posteriormente oxidadas a um ácido carboxílico ou reduzidas para formar aminas. Este processo é usado na produção comercial de ácido adípico .
O ácido nitroso reage rapidamente com álcoois alifáticos para produzir nitritos de alquil , que são vasodilatadores potentes :
- (CH 3 ) 2 CHCH 2 CH 2 OH + HNO 2 → (CH 3 ) 2 CHCH 2 CH 2 ONO + H 2 O
Os carcinógenos chamados nitrosaminas são produzidos, geralmente não intencionalmente, pela reação do ácido nitroso com aminas secundárias :
- HNO 2 + R 2 NH → R 2 N-NO + H 2 O
Atmosfera da Terra
O ácido nitroso está envolvido no orçamento de ozônio da baixa atmosfera , a troposfera . A reação heterogênea de óxido nítrico (NO) e água produz ácido nitroso. Quando essa reação ocorre na superfície dos aerossóis atmosféricos , o produto fotolisa prontamente em radicais hidroxila .