Tetrafluoreto de enxofre - Sulfur tetrafluoride

|
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Fluoreto de enxofre (IV)
|
|||
| Outros nomes
Tetrafluoreto de enxofre
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.029.103 |
||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 2418 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| SF 4 | |||
| Massa molar | 108,07 g / mol | ||
| Aparência | gás incolor | ||
| Densidade | 1,95 g / cm 3 , -78 ° C | ||
| Ponto de fusão | -121,0 ° C | ||
| Ponto de ebulição | −38 ° C | ||
| reage | |||
| Pressão de vapor | 10,5 atm (22 ° C) | ||
| Estrutura | |||
| Gangorra ( C 2 v ) | |||
| 0,632 D | |||
| Perigos | |||
| Riscos principais | corrosivo altamente tóxico |
||
| Ficha de dados de segurança | ICSC 1456 | ||
| NFPA 704 (diamante de fogo) | |||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
Nenhum | ||
|
REL (recomendado)
|
C 0,1 ppm (0,4 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
WL | ||
| Compostos relacionados | |||
|
Outros ânions
|
Dicloreto de enxofre Dibrometo de dissulfur Trifluoreto de enxofre |
||
|
Outros cátions
|
Difluoreto de oxigênio Tetrafluoreto de selênio Tetrafluoreto de telúrio |
||
|
Fluoretos de enxofre relacionados
|
Dissulfur difluoride Enxofre difluoride Dissulfur decafluoride Enxofre hexafluoride |
||
|
Compostos relacionados
|
Fluoreto de tionila | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O tetrafluoreto de enxofre é o composto químico com a fórmula S F 4 . É um gás corrosivo incolor que libera HF perigoso quando exposto à água ou umidade. Apesar dessas características indesejáveis, este composto é um reagente útil para a preparação de compostos organofluorados , alguns dos quais são importantes nas indústrias farmacêutica e de especialidades químicas .
Estrutura
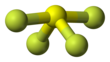
O enxofre no SF 4 está no estado formal de oxidação +4 . Do total de seis elétrons de valência do enxofre , dois formam um único par . A estrutura de SF 4 pode, portanto, ser antecipada usando os princípios da teoria VSEPR : é uma forma de gangorra , com S no centro. Uma das três posições equatoriais é ocupada por um par solitário não ligado de elétrons. Consequentemente, a molécula possui dois tipos distintos de ligantes F, dois axiais e dois equatoriais . As distâncias de ligação relevantes são S – F ax = 164,3 pm e S – F eq = 154,2 pm. É típico que os ligantes axiais em moléculas hipervalentes tenham uma ligação menos forte. Em contraste com SF 4 , a molécula relacionada SF 6 tem enxofre no estado 6+, nenhum elétron de valência permanece não ligado ao enxofre, portanto, a molécula adota uma estrutura octaédrica altamente simétrica. Contrastando ainda mais com o SF 4 , o SF 6 é extraordinariamente inerte quimicamente.
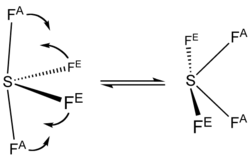
O espectro de 19 F NMR de SF 4 revela apenas um sinal, o que indica que as posições dos átomos F axial e equatorial se interconvertem rapidamente por meio de pseudo - rotação .
Síntese e fabricação
SF 4 é produzido pela reação de SCl 2 e NaF em acetonitrila :
- 3 SCl 2 + 4 NaF → SF 4 + S 2 Cl 2 + 4 NaCl
SF 4 também é produzido na ausência de solvente em temperaturas elevadas.
Alternativamente, SF 4 com alto rendimento é produzido usando enxofre (S) , NaF e cloro (Cl 2 ) na ausência de meio de reação, também em temperaturas de reação elevadas menos desejáveis (por exemplo, 225–450 ° C).
Um método de baixa temperatura (por exemplo, 20-86 ° C) de produção de SF 4 com alto rendimento, sem a necessidade de meio de reação, foi demonstrado utilizando bromo (Br 2 ) em vez de cloro (Cl 2 ) , S e KF :
- S + (2 + x ) Br 2 + 4 KF → SF 4 ↑ + x Br 2 + 4 KBr
Uso de SF 4 para a síntese de fluorocarbonos
Na síntese orgânica , o SF 4 é usado para converter os grupos COH e C = O em grupos CF e CF 2 , respectivamente. Certos álcoois fornecem prontamente o fluorocarbono correspondente . Cetonas e aldeídos dão difluoretos geminais. A presença de prótons alfa para a carbonila leva a reações colaterais e diminuição do rendimento (30–40%). Além disso pode dar-dióis cíclicos sulfito de ésteres, (RO) 2 SO. Os ácidos carboxílicos convertem-se em derivados trifluorometil. Por exemplo, o tratamento de ácido heptanóico com SF 4 a 100-130 ° C produz 1,1,1-trifluoroheptano. O hexafluoro-2-butino pode ser produzido de forma semelhante a partir do ácido acetilenodicarboxílico . Os coprodutos dessas fluorações, incluindo SF 4 não reagido junto com SOF 2 e SO 2 , são tóxicos, mas podem ser neutralizados por seu tratamento com KOH aquoso.
O uso de SF 4 está sendo substituído nos últimos anos pelo trifluoreto de dietilaminoenxofre mais convenientemente manuseado , Et 2 NSF 3 , "DAST", onde Et = CH 3 CH 2 . Este reagente é preparado a partir de SF 4 :
- SF 4 + Me 3 SiNEt 2 → Et 2 NSF 3 + Me 3 SiF
Outras reações
Pentafluoreto de cloreto de enxofre ( SF
5 Cl ), uma fonte útil do grupo SF 5 , é preparada a partir do SF 4 .
A hidrólise de SF 4 dá dióxido de enxofre :
- SF 4 + 2 H 2 O → SO 2 + 4 HF
Essa reação ocorre por intermédio do fluoreto de tionila , que geralmente não interfere no uso de SF 4 como reagente.
Toxicidade
SF
4 reage dentro dos pulmões com a umidade, gerando dióxido de enxofre e fluoreto de hidrogênio :
- SF 4 + 2 H 2 O → SO 2 + 4 HF