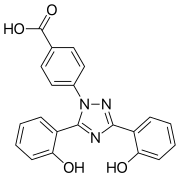
Deferasirox - Deferasirox
 | |
 | |
| Dados clínicos | |
|---|---|
| Pronúncia | de FER um senhor boi |
| Nomes comerciais | Exjade, Jadenu |
| Outros nomes | CGP-72670, ICL-670A, IC L670 |
| AHFS / Drugs.com | Monografia |
| Dados de licença | |
Categoria de gravidez |
|
| Vias de administração |
Pela boca |
| Código ATC | |
| Status legal | |
| Status legal | |
| Dados farmacocinéticos | |
| Biodisponibilidade | 70% |
| Ligação proteica | 99% |
| Metabolismo | Glucuronidação hepática |
| Meia-vida de eliminação | 8 a 16 horas |
| Excreção | Fecal (84%) e renal (8%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Painel CompTox ( EPA ) | |
| ECHA InfoCard |
100.211.077 |
| Dados químicos e físicos | |
| Fórmula | C 21 H 15 N 3 O 4 |
| Massa molar | 373,368 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| Densidade | 1,4 ± 0,1 g / cm 3 |
| |
| |
|
| |
O deferasirox , vendido sob a marca Exjade & Asunra (na forma injetável) e Oleptiss (formulação em comprimido), ambos pela Novartis, entre outros, é um quelante de ferro oral . Seu principal uso é reduzir a sobrecarga crônica de ferro em pacientes que estão recebendo transfusões de sangue de longo prazo para doenças como beta- talassemia e outras anemias crônicas . É o primeiro medicamento oral aprovado nos Estados Unidos para essa finalidade.
Foi aprovado pela Food and Drug Administration (FDA) dos Estados Unidos em novembro de 2005. De acordo com a FDA (maio de 2007), foram relatados casos de insuficiência renal e citopenias em pacientes recebendo comprimidos de suspensão oral deferasirox. É aprovado na União Europeia pela Agência Europeia de Medicamentos (EMA) para crianças de seis anos ou mais com sobrecarga crônica de ferro em transfusões de sangue repetidas. Está na Lista de Medicamentos Essenciais da Organização Mundial de Saúde .
Em julho de 2020, a Teva decidiu descontinuar o deferasirox. Ele está disponível como um medicamento genérico.
Propriedades
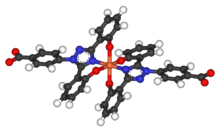
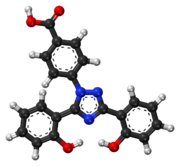
A meia-vida do deferasirox é de 8 a 16 horas, permitindo a administração de uma vez ao dia. Duas moléculas de deferasirox são capazes de se ligar a 1 átomo de ferro, que são subsequentemente eliminadas por excreção fecal. Seu baixo peso molecular e alta lipofilicidade permitem que o medicamento seja administrado por via oral, ao contrário da deferoxamina, que deve ser administrada por via intravenosa (infusão intravenosa). Junto com a deferiprona , o deferasirox parece ser capaz de remover o ferro das células (miócitos cardíacos e hepatócitos), bem como remover o ferro do sangue.
Síntese
O deferasirox pode ser preparado a partir de materiais de partida simples comercialmente disponíveis (ácido salicílico, salicilamida e ácido 4-hidrazinobenzoico) na seguinte sequência sintética de duas etapas:
A condensação de cloreto de saliciloil (formado in situ a partir de ácido salicílico e cloreto de tionila) com salicilamida sob condições de reação de desidratação resulta na formação de 2- (2-hidroxifenil) -1,3 ( 4H ) -benzoxazin-4-ona. Este intermediário é isolado e reagido com ácido 4-hidrazinobenzoico na presença de base para dar ácido 4- (3,5-bis (2-hidroxifenil) -1,2,4-triazol-1-il) benzóico (deferasirox).
Riscos
O deferasirox ficou em segundo lugar na lista de medicamentos mais frequentemente suspeitos em mortes de pacientes relatadas, compilada para 2019 pelo Institute for Safe Medical Practices , com 1320 mortes suspeitas. Um aviso em caixa foi adicionado no mesmo ano em relação a insuficiência renal , insuficiência hepática e sangramento gastrointestinal . Suspeita-se que o principal fator para esse aumento nas mortes suspeitas esteja relacionado à reanálise dos dados de eventos adversos pela Novartis .
Referências
links externos
- "Deferasirox" . Portal de informações sobre medicamentos . Biblioteca Nacional de Medicina dos EUA.