Dihidrogenofosfato de amônio - Ammonium dihydrogen phosphate

|
|
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dihidrogenofosfato de amônio
|
|
| Outros nomes
Fosfato de monoamônio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.028.877 |
| Número EC | |
| Número E | E342 (i) (antioxidantes, ...) |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| H 6 N O 4 P | |
| Massa molar | 115,025 g · mol −1 |
| Aparência | cristais brancos |
| Odor | Nenhum |
| Densidade | 1,80 g / cm 3 |
| Ponto de fusão | 190 ° C (374 ° F; 463 K) |
| (g / dL ) 28 (10 ° C) 36 (20 ° C) 44 (30 ° C) 56 (40 ° C) 66 (50 ° C) 81 (60 ° C) 99 (70 ° C) 118 (80 ° C) 173 (100 ° C) |
|
| Solubilidade | insolúvel em etanol insolúvel em acetona |
|
Índice de refração ( n D )
|
1.525 |
| Estrutura | |
| tetragonal | |
| Termoquímica | |
| -1445,07 kJ / mol | |
| Perigos | |
| Pictogramas GHS |

|
| Palavra-sinal GHS | Aviso |
| H319 | |
| P261 , P264 , P271 , P280 , P302 + 352 , P304 + 340 , P305 + 351 + 338 , P312 , P321 , P332 + 313 , P337 + 313 , P362 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
5750 mg / kg (rato, oral) |
| Compostos relacionados | |
|
Outros ânions
|
Fosfato de amônio Fosfato de diamônio |
|
Outros cátions
|
Fosfato monossódico Dihidrogenofosfato de potássio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
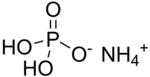
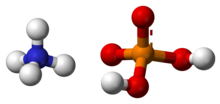
O dihidrogenofosfato de amônio ( ADP ), também conhecido como fosfato monoamônico ( MAP ), é um composto químico com a fórmula química (NH 4 ) (H 2 PO 4 ). ADP é um ingrediente importante de fertilizantes agrícolas e alguns extintores de incêndio . Ele também tem usos significativos em óptica e eletrônica .
Propriedades quimicas
O fosfato de monoamônio é solúvel em água e cristaliza a partir dela como o sal anidro no sistema tetragonal , como prismas alongados ou agulhas. É praticamente insolúvel em etanol .
O fosfato de monoamônio sólido pode ser considerado estável na prática para temperaturas de até 200 ° C, quando se decompõe em amônia gasosa NH
3e ácido fosfórico fundido H
3PO
4. A 125 ° C, a pressão parcial da amônia é de 0,05 mm Hg.
Uma solução de fosfato monoamônio esteiquométrico é ácida ( pH 4,7 a 0,1% de concentração, 4,2 a 5%).
Preparação
O fosfato monoamônico é preparado industrialmente pela reação exotérmica de ácido fosfórico e amônia nas proporções corretas:
-
NH
3+ H
3PO
4→ NH
6PO
4
O MAP cristalino então precipita.
Usos
Agricultura
O maior uso de fosfato monoamônio por peso é na agricultura, como ingrediente de fertilizantes. Fornece ao solo os elementos nitrogênio e fósforo em uma forma utilizável pelas plantas. Seu rótulo NPK é 12-61-0 (12-27-0), o que significa que contém 12% em peso de nitrogênio elementar e (nominalmente) 61% de pentóxido de fósforo P
2O
5, ou 27% do fósforo elementar.
Extintores de incêndio
O composto também é um componente do pó ABC em alguns extintores de pó químico .
Óptica
O fosfato de monoamônio é um cristal amplamente utilizado no campo da óptica devido às suas propriedades de birrefringência . Como resultado de sua estrutura de cristal tetragonal, este material tem simetria óptica uniaxial negativa com índices de refração típicos n o = 1,522 e n e = 1,478 em comprimentos de onda ópticos.
Eletrônicos
Os cristais de fosfato de monoamônio são piezoelétricos , uma propriedade necessária em alguns transdutores de sonar ativos (a alternativa são os transdutores que usam magnetostrição ). Na década de 1950, os cristais de ADP substituíram amplamente os cristais de quartzo e de sal de Rochelle em transdutores porque são mais fáceis de trabalhar do que o quartzo e, ao contrário do sal de Rochelle, não são deliquescentes .
Brinquedos
Por ser relativamente atóxico, o MAP também é uma substância popular para o cultivo recreativo de cristais, sendo vendido como kits de brinquedos misturados com corantes de várias cores.
Ocorrência natural
O composto aparece na natureza como o raro mineral bifosfamita. É formado em depósitos de guano. Um composto relacionado, que é a contraparte do monohidrogênio, é a ainda mais escassa fosfamita
Referências

