Succinato desidrogenase - Succinate dehydrogenase
| succinato desidrogenase (succinato-ubiquinona oxidoredutase) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
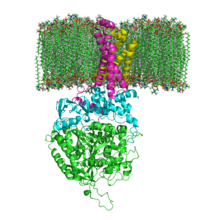 A estrutura do SQR em uma membrana fosfolipídica. SdhA , SdhB , SdhC e SdhD
| |||||||||
| Identificadores | |||||||||
| EC nº | 1.3.5.1 | ||||||||
| CAS no. | 9028-11-9 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
| Succinato desidrogenase | |
|---|---|
| Identificadores | |
| Símbolo | Complexo respiratório II |
| Superfamília OPM | 3 |
| Proteína OPM | 1zoy |
| Membranome | 656 |
A succinato desidrogenase ( SDH ) ou succinato-coenzima Q redutase ( SQR ) ou complexo respiratório II é um complexo enzimático encontrado em muitas células bacterianas e na membrana mitocondrial interna de eucariotos . É a única enzima que participa tanto do ciclo do ácido cítrico quanto da cadeia de transporte de elétrons . A análise histoquímica mostrando alta succinato desidrogenase no músculo demonstra alto conteúdo mitocondrial e alto potencial oxidativo.
Na etapa 6 do ciclo do ácido cítrico , o SQR catalisa a oxidação do succinato a fumarato com a redução da ubiquinona a ubiquinol . Isso ocorre na membrana mitocondrial interna ao acoplar as duas reações.
Estrutura
Subunidades
SQRs mitocondriais e muitos bacterianos são compostos de quatro subunidades estruturalmente diferentes : duas hidrofílicas e duas hidrofóbicas . As duas primeiras subunidades, uma flavoproteína (SdhA) e uma proteína ferro-enxofre (SdhB), formam uma cabeça hidrofílica onde ocorre a atividade enzimática do complexo. SdhA contém um cofator dinucleotídeo flavina adenina covalentemente ligado (FAD) e o sítio de ligação de succinato e SdhB contém três aglomerados de ferro-enxofre: [2Fe-2S], [4Fe-4S] e [3Fe-4S]. As segundas duas subunidades são subunidades de âncora de membrana hidrofóbica, SdhC e SdhD. As mitocôndrias humanas contêm duas isoformas distintas de SdhA (subunidades Fp tipo I e tipo II), essas isoformas também são encontradas em Ascaris suum e Caenorhabditis elegans . As subunidades formam um complexo de citocromo b ligado à membrana com seis hélices transmembrana contendo um grupo heme b e um local de ligação da ubiquinona . Duas moléculas de fosfolipídios , uma cardiolipina e uma fosfatidiletanolamina , também são encontradas nas subunidades SdhC e SdhD (não mostradas na imagem). Eles servem para ocupar o espaço hidrofóbico abaixo do heme b. Essas subunidades são exibidas na imagem anexada. SdhA é verde, SdhB é verde-azulado, SdhC é fúcsia e SdhD é amarelo. Em torno de SdhC e SdhD está uma membrana fosfolipídica com o espaço intermembranar no topo da imagem.
Tabela de composição de subunidades
| Não. | Nome da subunidade | Proteína humana | Descrição da proteína do UniProt | Família Pfam com Proteína Humana |
|---|---|---|---|---|
| 1 | SdhA | SDHA _HUMAN | Subunidade da flavoproteína da succinato desidrogenase [ubiquinona], mitocondrial | Pfam PF00890 , Pfam PF02910 |
| 2 | SdhB | SDHB _HUMAN | Subunidade de ferro-enxofre da succinato desidrogenase [ubiquinona], mitocondrial | Pfam PF13085 , Pfam PF13183 |
| 3 | SdhC | C560_HUMAN | Subunidade do citocromo b560 da succinato desidrogenase, mitocondrial | Pfam PF01127 |
| 4 | SdhD | DHSD_HUMAN | Succinato desidrogenase [ubiquinona] subunidade pequena do citocromo b, mitocondrial | Pfam PF05328 |
Local de ligação da ubiquinona
Dois locais distintos de ligação da ubiquinona podem ser reconhecidos no SDH de mamíferos - Q P proximal da matriz e Q D distal da matriz . O sítio de ligação da ubiquinona Qp, que mostra maior afinidade para a ubiquinona, está localizado em uma lacuna composta por SdhB, SdhC e SdhD. Ubiquinona é estabilizada pelas cadeias laterais de His207 da subunidade B, Ser27 e Arg31 da subunidade C e Tyr83 da subunidade D. O anel de quinona é rodeado por Ile28 da subunidade C e Pro160 da subunidade B. Estes resíduos , juntamente com Il209, Trp163 e Trp164 da subunidade B e Ser27 (átomo C) da subunidade C, formam o ambiente hidrofóbico da bolsa de ligação à quinona Qp. Em contraste, o sítio de ligação da ubiquinona Q D , que fica mais próximo do espaço entre as membranas, é composto apenas de SdhD e tem menor afinidade para a ubiquinona.
Sítio de ligação do succinato
SdhA fornece o local de ligação para a oxidação do succinato . As cadeias laterais Thr254, His354 e Arg399 da subunidade A estabilizam a molécula enquanto o FAD oxida e carrega os elétrons para o primeiro dos aglomerados de ferro-enxofre , [2Fe-2S]. Isso pode ser visto na imagem 5.
Centros redox
O sítio de ligação do succinato e o sítio de ligação da ubiquinona são conectados por uma cadeia de centros redox incluindo FAD e os aglomerados de ferro - enxofre . Essa cadeia se estende por mais de 40 Å através do monômero da enzima . Todas as distâncias de ponta a ponta entre os centros são menores do que o limite sugerido de 14 Å para a transferência fisiológica de elétrons . Esta transferência de elétrons é demonstrada na imagem 8.
Subunidade E
| SdhE | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Estrutura de solução NMR da proteína NMA1147 de Neisseria meningitidis . Mr19 alvo do consórcio de genômica estrutural do Nordeste
| |||||||||
| Identificadores | |||||||||
| Símbolo | SdhE | ||||||||
| Pfam | PF03937 | ||||||||
| InterPro | IPR005631 | ||||||||
| |||||||||
Em biologia molecular , o domínio da proteína denominado Sdh5 também é denominado SdhE, que significa proteína succinato desidrogenase E. No passado, também foi denominado YgfY e DUF339. Outro nome para SdhE é fator de montagem succinato desidrogenase 2 (Sdhaf2). Esta proteína pertence a um grupo de pequenas proteínas altamente conservadas encontradas em eucariotos e procariotos , incluindo NMA1147 de Neisseria meningitidis e YgfY de Escherichia coli . A proteína SdhE é encontrada na membrana mitocondrial e é importante para a criação de energia por meio de um processo denominado cadeia de transporte de elétrons .
Função
A função da SdhE foi descrita como um flavinador da succinato desidrogenase. SdhE funciona como um co-fator acompanhante que incorpora FAD em SdhA. Isso resulta na flavinilação SdhA, que é necessária para a função adequada da succinato desidrogenase. Estudos indicam que a SdhE é necessária à bactéria para crescer em succinato , utilizando o succinato como única fonte de carbono e, adicionalmente, para a função, da succinato desidrogenase, um componente vital da cadeia de transporte de elétrons que produz energia.
Estrutura
A estrutura dessas proteínas consiste em um feixe complexo de cinco alfa-hélices, que é composto de um feixe de 3 hélices para cima e para baixo mais um feixe de 2 hélices ortogonais.
Interações de proteínas
SdhE interage com a subunidade catalítica do complexo succinato desidrogenase (SDH).
Doença humana
O gene humano denominado SDH5 , codifica para a proteína SdhE. O próprio gene está localizado na posição cromossômica 11q13.1. Mutações de perda de função resultam em paraganglioma , um tumor neuroendócrino .
História
Os estudos recentes que sugerem que a SdhE é necessária para a flavinilação bacteriana contradizem os pensamentos anteriores sobre a SdhE. Foi originalmente proposto que a incorporação de FAD em flavoproteínas bacterianas era um processo autocatalítico . Estudos recentes agora argumentam que SdhE é a primeira proteína a ser identificada como necessária para a flavinilação em bactérias. Historicamente, a proteína SdhE já foi considerada uma proteína hipotética. Acredita-se que o YgfY também esteja envolvido na regulação da transcrição .
Montagem e maturação
Todas as subunidades de SDH mitocondrial humana são codificadas no genoma nuclear . Após a tradução, a subunidade SDHA é translocada como apoproteína na matriz mitocondrial. Posteriormente, uma das primeiras etapas é a ligação covalente do cofator FAD (flavinilação). Este processo parece ser regulado por alguns dos intermediários do ciclo do ácido tricarboxílico. Especificamente, succinato , isocitrato e citrato estimulam a flavinilação do SDHA. No caso de Sdh1 eucariótica (SDHA em mamíferos), outra proteína é necessária para o processo de incorporação de FAD - a saber, Sdh5 em levedura, fator de montagem succinato desidrogenase 2 ( SDHAF2 ) em células de mamíferos.
Antes de formar um heterodímero com a subunidade SDHB , alguma porção de SDHA com FAD ligado covalentemente parece interagir com outro fator de montagem - SDHAF4 (Sdh8 em levedura). O SDHA flavinilado não ligado se dimeriza com o SDHAF4, que serve como acompanhante . Estudos sugerem que a formação de dímero SDHA-SDHB é prejudicada na ausência de SDHAF4, de modo que o fator de montagem semelhante a chaperon pode facilitar a interação das subunidades. Além disso, o SDHAF4 parece impedir a geração de ROS por meio da aceitação de elétrons do succinato, que ainda pode ser oxidado pela subunidade monomérica SDHA não ligada.
Grupos protéticos Fe-S da subunidade SDHB estão sendo pré-formados na matriz mitocondrial pelo complexo proteico ISU. Acredita-se que o complexo também seja capaz de inserir os aglomerados de ferro-enxofre no SDHB durante sua maturação. Os estudos sugerem que a inserção do cluster Fe-S precede a formação do dímero SDHA-SDHB. Tal incorporação requer redução de resíduos de cisteína dentro do sítio ativo de SDHB. Tanto os resíduos de cisteína reduzidos quanto os aglomerados de Fe-S já incorporados são altamente suscetíveis a danos por ROS . Mais dois fatores de montagem SDH, SDHAF1 (Sdh6) e SDHAF3 (Sdh7 em levedura), parecem estar envolvidos na maturação SDHB na forma de proteger a subunidade ou dímero SDHA-SDHB de danos ao cluster Fe-S causados por ROS.
A montagem da âncora hidrofóbica que consiste nas subunidades SDHC e SDHD permanece obscura. Principalmente no caso de inserção do heme b e até mesmo sua função. O grupo prostético heme b não parece fazer parte da via de transporte de elétrons dentro do complexo II. Em vez disso, o cofator mantém a estabilidade da âncora.
Mecanismo
Oxidação de succinato
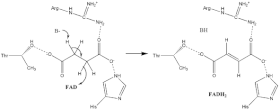
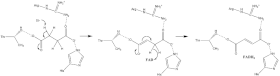
Pouco se sabe sobre o mecanismo exato de oxidação do succinato . No entanto, a estrutura cristalina mostra que FAD , Glu255, Arg286 e His242 da subunidade A (não mostrado) são bons candidatos para a etapa de desprotonação inicial . Depois disso, existem dois mecanismos de eliminação possíveis: E2 ou E1cb. Na eliminação E2, o mecanismo é combinado. O resíduo básico ou cofator desprotona o carbono alfa e FAD aceita o hidreto do carbono beta , oxidando o succinato ligado a fumarato - consulte a imagem 6. Em E1cb, um intermediário enolato é formado, mostrado na imagem 7, antes de FAD aceitar o hidreto . Mais pesquisas são necessárias para determinar qual mecanismo de eliminação succinato sofre na Succinato Desidrogenase. Fumarato oxidado , agora fracamente ligado ao sítio ativo , está livre para sair da proteína .
Tunelamento de elétrons
Depois que os elétrons são derivados da oxidação do succinato via FAD , eles fazem um túnel ao longo do relé [Fe-S] até atingirem o agrupamento [3Fe-4S]. Esses elétrons são subsequentemente transferidos para uma molécula de ubiquinona dentro do sítio ativo . O sistema de tunelamento de elétrons Ferro - Enxofre é mostrado na imagem 9.
Redução de ubiquinona
O oxigênio carbonil O1 da ubiquinona é orientado no sítio ativo (imagem 4) por interações de ligações de hidrogênio com Tyr83 da subunidade D. A presença de elétrons no aglomerado de ferro e enxofre [3Fe-4S] induz o movimento da ubiquinona em uma segunda orientação. Isso facilita uma segunda interação de ligação de hidrogênio entre o grupo O4 carbonil da ubiquinona e Ser27 da subunidade C. Após a primeira etapa de redução de elétron único , uma espécie de radical semiquinona é formada. O segundo elétron chega do aglomerado [3Fe-4S] para fornecer redução total da ubiquinona a ubiquinol . Esse mecanismo de redução da ubiquinona é mostrado na imagem 8.
Grupo protético heme
Embora a funcionalidade do heme na succinato desidrogenase ainda esteja sendo pesquisada, alguns estudos afirmaram que o primeiro elétron entregue à ubiquinona por meio de [3Fe-4S] pode criar um túnel para frente e para trás entre o heme e o intermediário ubiquinona . Desta forma, o cofator heme atua como um sumidouro de elétrons . Seu papel é prevenir a interação do intermediário com o oxigênio molecular para produzir espécies reativas de oxigênio (ROS). O grupo heme , em relação à ubiquinona , é mostrado na imagem 4.
Também foi proposto que um mecanismo de gating pode estar em vigor para evitar que os elétrons tunelem diretamente para o heme do aglomerado [3Fe-4S]. Um candidato potencial é o resíduo His207, que fica diretamente entre o cluster e o heme . His207 da subunidade B está na proximidade direta do agrupamento [3Fe-4S], da ubiquinona ligada e do heme ; e poderia modular o fluxo de elétrons entre esses centros redox.
Transferência de prótons
Para reduzir totalmente a quinona no SQR, dois elétrons e dois prótons são necessários. Tem sido argumentado que uma molécula de água (HOH39) chega ao sítio ativo e é coordenada por His207 da subunidade B, Arg31 da subunidade C e Asp82 da subunidade D. A espécie de semiquinona é protonada por prótons liberados de HOH39, completando a ubiquinona redução a ubiquinol . His207 e Asp82 provavelmente facilitam esse processo. Outros estudos afirmam que Tyr83 da subunidade D é coordenado com uma histidina próxima , bem como com o oxigênio carbonil O1 da ubiquinona . O resíduo de histidina diminui o pKa da tirosina , tornando-o mais adequado para doar seu próton ao intermediário ubiquinona reduzido .
Inibidores
Existem duas classes distintas de inibidores (SDHIs) do complexo II: aqueles que se ligam na bolsa de succinato e aqueles que se ligam na bolsa de ubiquinona. Os inibidores do tipo ubiquinona incluem carboxina e tenoiltrifluoroacetona . Os inibidores de análogos de succinato incluem o composto sintético malonato , bem como os intermediários do ciclo do TCA, malato e oxaloacetato . Na verdade, o oxaloacetato é um dos inibidores mais potentes do Complexo II. Por que um intermediário do ciclo TCA comum inibiria o Complexo II não é totalmente compreendido, embora possa exercer um papel protetor na minimização da produção de superóxido mediada por transferência reversa de elétrons pelo Complexo I. A atpenina 5a são inibidores do Complexo II altamente potentes que mimetizam a ligação da ubiquinona.
Os inibidores do tipo ubiquinona têm sido usados como fungicidas na agricultura desde 1960. A carboxina foi usada principalmente para controlar doenças causadas por basidiomicetos , como ferrugem do caule e doenças por Rhizoctonia . Mais recentemente, outros compostos com um espectro mais amplo contra uma variedade de patógenos de plantas foram desenvolvidos, incluindo boscalide , pentiopirade e fluopirame . Alguns fungos importantes para a agricultura não são sensíveis aos membros da nova geração de inibidores do tipo ubiquinona
Papel na doença
O papel fundamental da succinato-coenzima Q redutase na cadeia de transferência de elétrons da mitocôndria a torna vital na maioria dos organismos multicelulares . A remoção dessa enzima do genoma também demonstrou ser letal no estágio embrionário em camundongos.
- As mutações SdhA podem levar à síndrome de Leigh , encefalopatia mitocondrial e atrofia óptica .
- Mutações SDHB pode levar a tumorigénese em células de cromafina , fazendo com que uma classe de tumores conhecidos como succinato desidrogenase deficiente incluindo hereditária paraganglioma e hereditária feocromocitoma , succinato desidrogenase deficiente renal carcinoma e succinato desidrogenase deficiente tumor estromal gastrointestinal (GIST). Os tumores tendem a ser malignos . Também pode levar à redução do tempo de vida e ao aumento da produção de íons superóxido .
- Mutações SdhC pode levar à diminuição do tempo de vida, o aumento da produção de superóxido iões, hereditária paraganglioma e hereditária feocromocitoma . Os tumores tendem a ser benignos . Essas mutações são incomuns.
- Mutações SDHD pode levar a hereditária paraganglioma e hereditária feocromocitoma . Os tumores tendem a ser benignos e ocorrem frequentemente nas regiões da cabeça e pescoço. Essas mutações também podem diminuir a expectativa de vida e aumentar a produção de íons superóxido .
A succinato desidrogenase de mamíferos não atua apenas na geração de energia mitocondrial , mas também na detecção de oxigênio e na supressão de tumores ; e, portanto, é objeto de pesquisas em andamento.
Níveis reduzidos da enzima mitocondrial succinato desidrogenase (SDH), o principal elemento do complexo II, são observados post mortem nos cérebros de pacientes com doença de Huntington, e defeitos no metabolismo energético foram identificados em pacientes em HD pré-sintomáticos e sintomáticos.