Lista de estruturas cristalinas macromoleculares biofisicamente importantes - List of biophysically important macromolecular crystal structures
Estruturas cristalinas de proteínas e moléculas de ácido nucléico e seus complexos são centrais para a prática da maioria das partes da biofísica e moldaram muito do que entendemos cientificamente no nível de detalhes atômicos da biologia. Sua importância é sublinhada pela declaração das Nações Unidas de 2014 como o Ano Internacional da Cristalografia , como o 100º aniversário do prêmio Nobel de 1914 de Max von Laue pela descoberta da difração de raios X pelos cristais. Esta lista cronológica de proteínas biofisicamente notáveis e estruturas de ácido nucléico é vagamente baseada em uma revisão no Biophysical Journal . A lista inclui todas as primeiras doze estruturas distintas, aquelas que abriram novos caminhos no assunto ou método, e aquelas que se tornaram sistemas modelo para trabalhar em futuras áreas biofísicas de pesquisa.
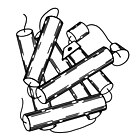
Mioglobina
1960 - A mioglobina foi a primeira estrutura cristalina de alta resolução de uma molécula de proteína. A mioglobina embala um grupo heme contendo ferro que se liga reversivelmente ao oxigênio para uso na alimentação das fibras musculares , e os primeiros cristais eram de mioglobina do cachalote , cujos músculos precisam de abundante armazenamento de oxigênio para mergulhos profundos. A estrutura tridimensional da mioglobina é composta por 8 alfa-hélices , e a estrutura cristalina mostrou que sua conformação era destra e se aproximava muito da geometria proposta por Linus Pauling , com 3,6 resíduos por volta e ligações de hidrogênio de base do peptídeo NH de um resíduo para o peptídeo CO do resíduo i + 4. A mioglobina é um sistema modelo para muitos tipos de estudos biofísicos, especialmente envolvendo o processo de ligação de pequenos ligantes, como oxigênio e monóxido de carbono .
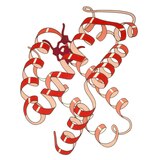
Hemoglobina
1960 - A estrutura de cristal da hemoglobina mostrou um tetrâmero de dois tipos de cadeia relacionados e foi resolvido em resolução muito menor do que a mioglobina monomérica, mas claramente tinha a mesma arquitetura básica de 8 hélices (agora chamada de "dobra globina"). Outras estruturas de cristal de hemoglobina em resolução mais alta [PDB 1MHB, 1DHB) logo mostraram a mudança acoplada da conformação local e quaternária entre os estados oxi e desoxi da hemoglobina, o que explica a cooperatividade da ligação do oxigênio no sangue e o efeito alostérico de fatores como como pH e DPG . Por décadas, a hemoglobina foi o principal exemplo de ensino para o conceito de alosteria, além de ser um foco intensivo de pesquisa e discussão sobre alosteria. Em 1909, cristais de hemoglobina de> 100 espécies foram usados para relacionar a taxonomia às propriedades moleculares. Esse livro foi citado por Perutz no relatório de 1938 sobre os cristais de hemoglobina de cavalos que deu início a sua longa saga para resolver a estrutura do cristal. Os cristais de hemoglobina são pleocróicos - vermelho escuro em duas direções e vermelho claro na terceira - por causa da orientação dos hemes, e a banda Soret brilhante dos grupos heme porfirina é usada na análise espectroscópica da ligação do ligante de hemoglobina.
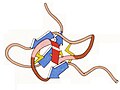
Lisozima clara de ovo de galinha
1965 - lisozima de clara de ovo de galinha (arquivo PDB 1lyz). foi a primeira estrutura cristalina de uma enzima (ela divide pequenos carboidratos em açúcares simples), usada nos primeiros estudos do mecanismo enzimático. Continha folha beta (antiparalela), bem como hélices, e também foi a primeira estrutura macromolecular a ter suas coordenadas atômicas refinadas (no espaço real). O material inicial para preparação pode ser comprado no supermercado, e a lisozima de ovo de galinha cristaliza muito facilmente em muitos grupos espaciais diferentes ; é o caso de teste favorito para novos instrumentos e experimentos cristalográficos. Exemplos recentes são nanocristais de lisozima para coleta de dados de laser de elétrons livres e microcristais para difração de microeletrons.
Ribonuclease
1967 - Ribonuclease A (arquivo PDB 2RSA) é uma enzima de clivagem de RNA estabilizada por 4 ligações dissulfeto. Foi usado na pesquisa seminal da Anfinsen sobre o dobramento de proteínas, que levou ao conceito de que a estrutura tridimensional de uma proteína era determinada por sua sequência de aminoácidos . A ribonuclease S , a forma clivada de dois componentes estudada por Fred Richards , também era enzimaticamente ativa, tinha uma estrutura cristalina quase idêntica (arquivo PDB 1RNS) e mostrou ser cataliticamente ativa até mesmo no cristal, ajudando a dissipar as dúvidas sobre a relevância de estruturas de cristal de proteína para função biológica.
Serina proteases
1967 - As serina proteases são um grupo historicamente muito importante de estruturas enzimáticas, porque coletivamente iluminaram o mecanismo catalítico (no caso deles, pela "tríade catalítica" de Ser-His-Asp), a base de diferentes especificidades de substrato e o mecanismo de ativação pelo qual uma clivagem enzimática controlada enterra a nova extremidade da cadeia para reorganizar adequadamente o sítio ativo. As primeiras estruturas cristalinas incluíam quimotripsina (arquivo PDB 2CHA), quimiotripsinogênio (arquivo PDB 1CHG), tripsina (arquivo PDB 1PTN) e elastase (arquivo PDB 1EST). Eles também foram as primeiras estruturas de proteínas que mostraram dois domínios quase idênticos, presumivelmente relacionados por duplicação de genes . Uma razão para seu amplo uso como exemplos de livros e salas de aula foi o sistema de numeração de código de inserção (odiado por todos os programadores de computador), que tornou Ser195 e His57 consistentes e memoráveis, apesar das diferenças de sequência específicas de proteínas.
Papaína
1968 - Papaína
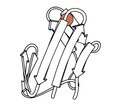
Carboxipeptidase
1969 - Carboxipeptidase A é uma metaloprotease de zinco . Sua estrutura cristalina (arquivo PDB 1CPA) mostrou a primeira estrutura beta paralela: uma grande folha central torcida de 8 fios com o sítio ativo Zn localizado na extremidade C-terminal dos fios do meio e a folha flanqueada em ambos os lados com hélices alfa. É uma exopeptidase que cliva peptídeos ou proteínas da extremidade carboxi-terminal em vez de interna à sequência. Posteriormente, um pequeno inibidor de proteína de carboxipeptidase foi resolvido (arquivo PDB 4CPA) que interrompe mecanicamente a catálise ao apresentar sua extremidade C-terminal apenas saindo de um anel de ligações dissulfeto com estrutura rígida atrás dele, impedindo a enzima de sugar a cadeia passado o primeiro resíduo.
Subtilisina
1969 - A subtilisina (arquivo PDB 1sbt) era um segundo tipo de serina protease com um sítio ativo quase idêntico ao da família de enzimas da tripsina, mas com uma dobra geral completamente diferente. Isso deu a primeira visão da evolução convergente no nível atômico. Mais tarde, um estudo mutacional intensivo da subtilisina documentou os efeitos de todos os 19 outros aminoácidos em cada posição individual.
Lactato desidrogenase
1970 - Lactato desidrogenase
Inibidor de tripsina
1970 - O inibidor básico de tripsina pancreática , ou BPTI (arquivo PDB 2pti), é uma proteína pequena e muito estável que tem sido um sistema modelo altamente produtivo para o estudo de ligação supertensa, formação de ligação dissulfeto (SS), dobramento de proteína , estabilidade molecular por mutações de aminoácidos ou troca de hidrogênio-deutério e dinâmica local rápida por RMN . Biologicamente, o BPTI se liga e inibe a tripsina enquanto é armazenada no pâncreas , permitindo a ativação da digestão de proteínas somente depois que a tripsina é liberada no estômago.
Rubredoxina
1970 - Rubredoxin (arquivo PDB 2rxn) foi a primeira estrutura redox resolvida, uma proteína minimalista com o ferro ligado por 4 cadeias laterais Cys de 2 laços no topo dos grampos β. Ele difratou para 1,2Å, permitindo o primeiro refinamento de espaço recíproco de uma proteína (4,5rxn). [NB: cuidado com 4rxn, feito sem restrições de geometria!] As rubredoxinas de Archaeal são responsáveis por muitas das pequenas estruturas de mais alta resolução no PDB.
Insulina
1971 - A insulina (arquivo PDB 1INS) é um hormônio central para o metabolismo do açúcar e do armazenamento de gordura, e importante em doenças humanas como obesidade e diabetes . É biofisicamente notável por sua ligação de Zn, seu equilíbrio entre os estados de monômero, dímero e hexâmero, sua capacidade de formar cristais in vivo e sua síntese como uma forma "pro" mais longa que é então clivada para dobrar como o ativo 2- cadeia, monômero ligado a SS. A insulina foi um sucesso do programa de crescimento de cristais da NASA no ônibus espacial , produzindo preparações a granel de minúsculos cristais muito uniformes para dosagem controlada.
Nuclease estafilocócica
1971 - Nuclease estafilocócica
Citocromo C
1971 - Citocromo C
Lisozima de fago T4
1974 - lisozima do fago T4
Imunoglobulinas
1974 - Imunoglobulinas
Superoxido dismutação
1975 - Cu, Zn Superóxido dismutase
RNA de transferência
1976 - Transferência de RNA
Triose fosfato isomerase
1976 - Triose fosfato isomerase
Proteases aspárticas semelhantes à pepsina
1976 - Rhizopuspepsin
1976 - Endotiapepsina
1976 - Penicilopepsina
Estruturas posteriores (1978 em diante)
1978 - vírus icosaédrico
1981 - Dodecâmero de DNA da forma B de Dickerson
1981 - Crambin
1985 - Calmodulin
1985 - DNA polimerase
1985 - Centro de reação fotossintética Pares de bacterioclorofilas (verdes) dentro da membrana capturam energia da luz solar, então viajando por muitos passos para se tornarem disponíveis nos grupos heme (vermelhos) no módulo citocromo-C no topo. Esta foi a primeira estrutura cristalina resolvida para uma proteína de membrana, um marco reconhecido pelo Prêmio Nobel de Hartmut Michel, Hans Deisenhofer e Robert Huber.
1986 - Interações Repressor / DNA
1987 - Complexo principal de histocompatibilidade '
1987 - Ubiquitina
1987 - proteína ROP
1989 - protease HIV-1
1990 - Bacteriorodopsina
1991 - bobina GCN4
1991 - transcriptase reversa do HIV-1
1993 - Beta hélice de Pectato-liase
1994 - Colágeno
1994 - complexo Barnase / barstar
1994 - F1 ATPase
1995 - Proteínas G heterotriméricas
1996 - proteína fluorescente verde
1996 - proteína motor cinesina
1997 - acompanhante GroEL / ES
1997 - Nucleosome
1998 - íntron de autoexclusão do Grupo I
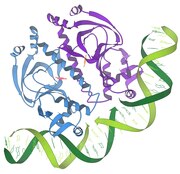
1998 - As topoisomerases de DNA desempenham o trabalho biologicamente importante e necessário de desemaranhar fitas ou hélices de DNA que se entrelaçam ou são torcidas com muita força durante processos celulares normais, como a transcrição de informações genéticas.
1998 - Dímero alfa / beta de tubulina
1998 - canal de potássio
1998 - junção Holliday
2000 - Os ribossomos são uma parte central da biologia e da biofísica, que se tornou acessível estruturalmente em 2000.
2000 - AAA + ATPase
2002 - Ankyrin se repete
2003 - Projeto de proteína TOP7
2004 - Proteínas do relógio circadiano de cianobactérias
2004 - Riboswitch
2006 - Exossomo humano
2007 - receptor acoplado à proteína G
2009 - A partícula Vault é uma intrigante nova descoberta de uma grande partícula oca comum nas células, com várias sugestões diferentes para sua possível função biológica. As estruturas cristalinas (arquivos PDB 2zuo, 2zv4, 2zv5 e 4hl8) mostram que cada metade da abóbada é composta por 39 cópias de uma longa proteína de 12 domínios que giram juntas para formar o invólucro. A desordem nas extremidades superior e inferior sugere aberturas para possível acesso ao interior da abóbada.