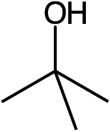
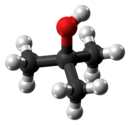
Álcool terc-butílico - tert-Butyl alcohol
|
|
|||

|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
2-metilpropan-2-ol |
|||
Outros nomes
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 906698 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard |
100.000.809 |
||
| Número EC | |||
| 1833 | |||
| Malha | terc-butil + álcool | ||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 1120 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 4 H 10 O | |||
| Massa molar | 74,123 g · mol −1 | ||
| Aparência | Sólido incolor | ||
| Odor | Cânfora | ||
| Densidade | 0,775 g / mL | ||
| Ponto de fusão | 25 a 26 ° C; 77 a 79 ° F; 298 a 299 K | ||
| Ponto de ebulição | 82 a 83 ° C; 179 a 181 ° F; 355 a 356 K | ||
| miscível | |||
| log P | 0,584 | ||
| Pressão de vapor | 4,1 kPa (a 20 ° C) | ||
| Acidez (p K a ) | 16,54 | ||
| 5,742 × 10 −5 cm 3 / mol | |||
|
Índice de refração ( n D )
|
1.387 | ||
| 1,31 D | |||
| Termoquímica | |||
|
Capacidade de calor ( C )
|
215,37 J K −1 mol −1 | ||
|
Entropia molar padrão ( S |
189,5 J K −1 mol −1 | ||
| −360,04 a −358,36 kJ mol −1 | |||
| −2.64479 a −2.64321 MJ mol −1 | |||
| Perigos | |||
| Ficha de dados de segurança | inchem.org | ||
| Pictogramas GHS |
 
|
||
| Palavra-sinal GHS | Perigo | ||
| H225 , H319 , H332 , H335 | |||
| P210 , P261 , P305 + 351 + 338 | |||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | 11 ° C (52 ° F; 284 K) | ||
| 480 ° C (896 ° F; 753 K) | |||
| Limites explosivos | 2,4–8,0% | ||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
3559 mg / kg (coelho, oral) 3500 mg / kg (rato, oral) |
||
| NIOSH (limites de exposição à saúde dos EUA): | |||
|
PEL (permitido)
|
TWA 100 ppm (300 mg / m 3 ) | ||
|
REL (recomendado)
|
TWA 100 ppm (300 mg / m 3 ) ST 150 ppm (450 mg / m 3 ) | ||
|
IDLH (perigo imediato)
|
1600 ppm | ||
| Compostos relacionados | |||
|
Butanóis relacionados
|
2-butanol |
||
|
Compostos relacionados
|
2-Metil-2-butanol Trimetilsilanol |
||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
O álcool terc-butílico é o álcool terciário mais simples, com uma fórmula de (CH 3 ) 3 COH (às vezes representado como t -BuOH). É um dos quatro isômeros do butanol . O álcool terc-butílico é um sólido incolor que derrete próximo à temperatura ambiente e tem umodor semelhante ao da cânfora . É miscível com água , etanol e éter dietílico .
Ocorrência natural
O álcool terc-butílico foi identificado na cerveja e no grão de bico . Também é encontrada na mandioca , que é usada como ingrediente de fermentação em certas bebidas alcoólicas .
Preparação
O álcool terc-butílico é derivado comercialmente do isobutano como um coproduto da produção de óxido de propileno . Também pode ser produzido pela hidratação catalítica do isobutileno ou por uma reação de Grignard entre acetona e cloreto de metilmagnésio .
A purificação não pode ser realizada por destilação simples devido à formação de um azeótropo com água, embora a secagem inicial do solvente contendo grandes quantidades de água seja realizada pela adição de benzeno para formar um azeótropo terciário e destilação da água. Quantidades menores de água são removidas por secagem com óxido de cálcio (CaO), carbonato de potássio (K 2 CO 3 ), sulfato de cálcio (CaSO 4 ) ou sulfato de magnésio (MgSO 4 ), seguido por destilação fracionada. Álcool terc-butílico anidro é obtido por refluxo adicional e destilação de magnésio ativado com iodo, ou metais alcalinos, como sódio ou potássio. Outros métodos incluem o uso de peneiras moleculares de 4 Å , terc- butilato de alumínio , hidreto de cálcio (CaH 2 ) ou cristalização fracionada sob atmosfera inerte.
Formulários
Álcool terc-butílico é usado como solvente, desnaturante de etanol , ingrediente removedor de tinta e booster de octanagem e oxigenação da gasolina . É um intermediário químico usado para produzir metil terc- butil éter (MTBE) e etil terc- butil éter (ETBE) por reação com metanol e etanol , respectivamente, e terc- butil hidroperóxido (TBHP) por reação com peróxido de hidrogênio .
Reações
Como um álcool terciário, o álcool terc-butílico é mais resistente à oxidação do que os outros isômeros do butanol.
O álcool terc-butílico é desprotonado com uma base forte para dar o alcóxido . Particularmente comum é o terc- butóxido de potássio , que é preparado tratando o terc- butanol com potássio metálico.
- K + t -BuOH → t -BuO - K + + 1/2 H 2
O terc- butóxido é uma base forte e não nucleofílica em química orgânica. Ele prontamente abstrai prótons ácidos de substratos, mas seu volume estérico inibe o grupo de participar da substituição nucleofílica , como em uma síntese de éter de Williamson ou uma reação S N 2 .
O álcool terc-butílico reage com o cloreto de hidrogênio para formar o cloreto terc-butílico .
O-cloração de álcool terc-butílico com ácido hipocloroso para dar hipoclorito tert-butílico :
- (CH 3 ) 3 COH + HOCl → (CH 3 ) 3 COCl + H 2 O
Farmacologia e Toxicologia
Existem dados limitados sobre a farmacologia e a toxicologia do terc-butanol em humanos e outros animais. A exposição humana pode ocorrer devido ao metabolismo do oxigênio do combustível. O tert-butanol é pouco absorvido pela pele, mas rapidamente absorvido se inalado ou ingerido. O tert-butanol é irritante para a pele ou os olhos. A toxicidade de doses únicas é geralmente baixa, mas doses altas podem produzir um efeito sedativo ou anestésico.
Notas
Referências
links externos
- Cartão Internacional de Segurança Química 0114
- Guia de bolso do NIOSH para perigos químicos. "# 0078" . Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH).
- Critérios de saúde ambiental 65 do IPCS : Butanóis: quatro isômeros
- Guia 7 de saúde e segurança do IPCS : terc- butanol