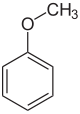
Anisole - Anisole
|
|
|||

|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Metoxibenzeno
|
|||
|
Nome IUPAC preferido
Anisole |
|||
| Outros nomes
Metil fenil éter
fenoximetano |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 506892 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard |
100,002,615 |
||
| Número EC | |||
| 2964 | |||
| KEGG | |||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
| Número ONU | 2222 | ||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| C 7 H 8 O | |||
| Massa molar | 108,140 g · mol −1 | ||
| Aparência | Líquido incolor | ||
| Densidade | 0,995 g / cm 3 | ||
| Ponto de fusão | −37 ° C (−35 ° F; 236 K) | ||
| Ponto de ebulição | 154 ° C (309 ° F; 427 K) | ||
| Solubilidade | Insolúvel | ||
| -72,79 · 10 −6 cm 3 / mol | |||
| Perigos | |||
| Pictogramas GHS |
 
|
||
| Palavra-sinal GHS | Aviso | ||
| H226 , H315 , H319 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P264 , P280 , P302 + 352 , P303 + 361 + 353 , P305 + 351 + 338 , P321 , P332 + 313 , P337 + 313 , P362 , P370 + 378 , P403 + 235 , P501 | |||
| NFPA 704 (diamante de fogo) | |||
| Dose ou concentração letal (LD, LC): | |||
|
LD 50 ( dose mediana )
|
3700 mg / kg (rato, oral) | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Anisol , ou metoxibenzeno , é um composto orgânico com a fórmula CH 3 OC 6 H 5 . É um líquido incolor com um cheiro que lembra a semente de erva- doce e, de fato, muitos de seus derivados são encontrados em fragrâncias naturais e artificiais. O composto é feito principalmente de forma sintética e é um precursor de outros compostos sintéticos. É um éter . O anisol é um reagente padrão de valor prático e pedagógico.
Pode ser preparado pela síntese de éter Williamson ; o fenóxido de sódio é feito reagir com um halogeneto de metila para produzir anisol.
Reatividade
O anisol sofre uma reação de substituição aromática eletrofílica em uma velocidade mais rápida do que o benzeno , que por sua vez reage mais rapidamente do que o nitrobenzeno . O grupo metoxi é um grupo de direcionamento orto / para , o que significa que a substituição eletrofílica ocorre preferencialmente nesses três locais. A nucleofilicidade aumentada de anisol vs. benzeno reflete a influência do grupo metoxi , que torna o anel mais rico em elétrons. O grupo metoxi afeta fortemente a nuvem pi do anel como um doador de elétrons mesomérico , mais do que como um grupo removedor de elétrons indutivo , apesar da eletronegatividade do oxigênio . Dito de forma mais quantitativa, a constante de Hammett para a para-substituição do anisol é -0,27.
Ilustrativo de sua nucleofilicidade , o anisol reage com o anidrido acético para dar 4-metoxiacetofenona :
- CH 3 OC 6 H 5 + (CH 3 CO) 2 O → CH 3 OC 6 H 4 C (O) CH 3 + CH 3 CO 2 H
Ao contrário da maioria das acetofenonas, mas refletindo a influência do grupo metoxi, a metoxiacetofenona sofre uma segunda acetilação . Muitas reações relacionadas foram demonstradas. Por exemplo, P 4 S 10 converte anisol no reagente de Lawesson , [(CH 3 OC 6 H 4 ) PS 2 ] 2 .
Também indicando um anel rico em elétrons, o anisol prontamente forma complexos π com carbonilas metálicas , por exemplo, Cr (η 6 -anisol) (CO) 3 .
A ligação éter é altamente estável, mas o grupo metil pode ser removido com ácido iodídrico :
- CH 3 OC 6 H 5 + HI → HOC 6 H 5 + CH 3 I
A redução do anisol em bétula dá 1-metoxiciclohexa-1,4-dieno.
Preparação
O anisol é preparado por metilação de fenóxido de sódio com sulfato de dimetil ou cloreto de metila:
- 2 C 6 H 5 O - Na + + (CH 3 O) 2 SO 2 → 2 C 6 H 5 OCH 3 + Na 2 SO 4
Formulários
O anisol é um precursor de perfumes , feromônios de insetos e produtos farmacêuticos . Por exemplo, o anetol sintético é preparado a partir do anisol.
Segurança
O anisol é relativamente não tóxico com um LD 50 de 3700 mg / kg em ratos. Seu principal perigo é a inflamabilidade.
Veja também
- Anetol
- Bromoanisole
- Hidroxianisol butilado
- Éter
- Éter etil fenil
- Fenol
- 2,4,6-Tricloroanisol (odor de cortiça)
Referências
-
^ a b c
Nomenclatura da química orgânica: Recomendações IUPAC e nomes preferidos 2013 (livro azul) . Cambridge: The Royal Society of Chemistry . 2014. pp. 702–703. doi : 10.1039 / 9781849733069-00648 . ISBN 978-0-85404-182-4.
Anisole, C 6 H 5 -O-CH 3 , é o único nome na classe de éteres que é retido tanto como um nome IUPAC preferido e para uso na nomenclatura geral. Para nomes IUPAC preferidos, nenhuma substituição é permitida; para a nomenclatura geral, a substituição é permitida no anel e na cadeia lateral sob certas condições (ver P-34.1.1.4).
- ^ Smith, Michael B .; Março, Jerry (2007), Advanced Organic Chemistry: Reactions, Mechanisms and Structure (6ª ed.), New York: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Thomsen, K. Clausen, S. Scheibye, S.-O. Lawesson (1984). "Tiação com 2,4-Bis (4-Metoxifenil) -1,3,2,4-Ditiadifosfetano 2,4-Dissulfeto: N-Metiltiopirrolidona". Sínteses orgânicas . 62 : 158. doi : 10.15227 / orgsyn.062.0158 .CS1 maint: vários nomes: lista de autores ( link )
- ^ E. Peter Kündig (2004). "Synthesis of Transition Metal η 6 -Arene Complexes". Tópicos Organomet Chem . 7 : 3-20. doi : 10.1007 / b94489 .
- ^ AJ Birch e KB Chamberlain (1977). "Tricarbonil [(2,3,4,5-η) -2,4-Ciclohexadien-1-ona] Ferro e Tricarbonil [(1,2,3,4,5-η) -2-Metoxi-2,4 -Ciclohexadien-1-il] Ferro (1+) Hexafluorofosfato (1−) de Anisol ". Sínteses orgânicas . 57 : 107. doi : 10.15227 / orgsyn.057.0107 .
- ^ GS Hiers e FD Hager (1929). "Anisole". Sínteses orgânicas . 9 : 12. doi : 10.15227 / orgsyn.009.0012 .
- ^ a b Helmut Fiege, Heinz-Werner Voges, Toshikazu Hamamoto, Sumio Umemura, Tadao Iwata, Hisaya Miki, Yasuhiro Fujita, Hans-Josef Buysch, Dorothea Garbe, Wilfried Paulus "Phenol Derivatives" em Ullmann's Wiley's Encyclopedia of 2002, Industrial Wiley's Encyclopedia of -VCH, Weinheim. doi : 10.1002 / 14356007.a19_313
- ^ a b MSDS arquivado em 1º de julho de 2010, na máquina de Wayback
links externos
- Cartão Internacional de Segurança Química 1014
- Entrada de banco de dados de feromônios de ferobase