Trifluoreto de fósforo - Phosphorus trifluoride
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nomes IUPAC
Trifluoreto de
fósforo Fluoreto de fósforo (III) Trifluorofosfano Trifluoridofosfato Perfluorofosfano |
|||
| Outros nomes
Trifluorofosfina
Fósforo fluoreto TL-75 |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard |
100.029.098 |
||
|
PubChem CID
|
|||
| Número RTECS | |||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| PF 3 | |||
| Massa molar | 87,968971 g / mol | ||
| Aparência | gás incolor | ||
| Densidade | 3,91 g / L, gás | ||
| Ponto de fusão | −151,5 ° C (−240,7 ° F; 121,6 K) | ||
| Ponto de ebulição | −101,8 ° C (−151,2 ° F; 171,3 K) | ||
| hidrólise lenta | |||
| Estrutura | |||
| Trigonal piramidal | |||
| 1,03 D | |||
| Perigos | |||
| Ficha de dados de segurança | Veja: página de dados | ||
| NFPA 704 (diamante de fogo) | |||
| Ponto de inflamação | Não inflamável | ||
| Compostos relacionados | |||
|
Outros ânions
|
Tricloreto de fósforo Tribrometo de fósforo Triiodeto de fósforo Fosfano |
||
|
Outros cátions
|
Trifluoreto de nitrogênio Trifluoreto de arsênio Trifluoreto de antimônio Trifluoreto de bismuto |
||
|
Ligantes relacionados
|
Monóxido de carbono | ||
|
Compostos relacionados
|
Pentafluoreto de fósforo | ||
| Página de dados suplementares | |||
|
Índice de refração ( n ), constante dielétrica (ε r ), etc. |
|||
|
Dados termodinâmicos |
Comportamento da fase sólido-líquido-gás |
||
| UV , IR , NMR , MS | |||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Trifluoreto de fósforo (fórmula P F 3 ), é um líquido incolor e inodoro gás . É altamente tóxico e reage lentamente com a água. Seu principal uso é como ligante em complexos metálicos . Como um ligante, ele é paralelo ao monóxido de carbono em carbonilas metálicas e, de fato, sua toxicidade se deve à sua ligação com o ferro na hemoglobina do sangue de maneira semelhante ao monóxido de carbono.
Propriedades físicas
O trifluoreto de fósforo tem um ângulo de ligação F − P − F de aproximadamente 96,3 °. O PF 3 gasoso tem uma entalpia de formação padrão de −945 kJ / mol (−226 kcal / mol ). O átomo de fósforo tem um deslocamento químico de ressonância magnética nuclear de 97 ppm (campo inferior de H 3 PO 4 ).
Propriedades
O trifluoreto de fósforo hidrolisa especialmente em pH alto , mas é menos sensível hidroliticamente do que o tricloreto de fósforo . Não ataca o vidro, exceto em altas temperaturas, e hidróxido de potássio anidro pode ser usado para secá-lo com pouca perda. Com metais quentes , são formados fosforetos e fluoretos. Com bases de Lewis , como produtos de adição de amônia (adutos), são formados, e o PF 3 é oxidado por agentes oxidantes como o bromo ou o permanganato de potássio .
Como um ligante para metais de transição, o PF 3 é um forte aceptor π. Forma uma variedade de complexos metálicos com metais em estados de baixa oxidação . O PF 3 forma vários complexos para os quais os derivados de CO correspondentes (ver carbonil metálico ) são instáveis ou inexistentes. Assim, Pd (PF 3 ) 4 é conhecido, mas Pd (CO) 4 não. Esses complexos são geralmente preparados diretamente a partir do composto de carbonila de metal relacionado , com perda de CO . No entanto, o níquel metálico reage diretamente com PF 3 a 100 ° C sob pressão de 35 MPa para formar Ni (PF 3 ) 4 , que é análogo ao Ni (CO) 4 . Cr (PF 3 ) 6 , o análogo de Cr (CO) 6 , pode ser preparado a partir de dibenzenocromio :
- Cr (C 6 H 6 ) 2 + 6 PF 3 → Cr (PF 3 ) 6 + 2 C 6 H 6
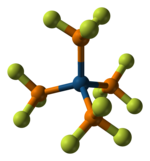 |

|
| Modelo bola e stick de [Pt (PF 3 ) 4 ] | Modelo de preenchimento de espaço de [Pt (PF 3 ) 4 ] |
Preparação
O trifluoreto de fósforo é geralmente preparado a partir de tricloreto de fósforo via troca de halogênio usando vários fluoretos , como fluoreto de hidrogênio , fluoreto de cálcio , trifluoreto de arsênio , trifluoreto de antimônio ou fluoreto de zinco :
Atividade biológica
O trifluoreto de fósforo é semelhante ao monóxido de carbono , pois é um gás que se liga fortemente ao ferro na hemoglobina , impedindo o sangue de absorver oxigênio.
Precauções
O PF 3 é altamente tóxico , comparável ao fosgênio .
Referências
Leitura adicional
- Toy, ADF (1973). The Chemistry of Phosphorus . Oxford, Reino Unido: Pergamon Press.
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Lide, DR, ed. (1990). Handbook of Chemistry and Physics (71ª ed.). Ann Arbor, MI: CRC Press. ISBN 978-0-8493-0471-2.
- March, J. (1992). Advanced Organic Chemistry (4ª ed.). Nova York: Wiley. p. 723. ISBN 978-0-471-60180-7.
- Stecher, PG, ed. (1960). The Merck Index (7ª ed.). Rahway, NJ, EUA: Merck & Co.
- Holmes, RR (1960). "Um Exame da Natureza Básica dos Trihalides de Fósforo, Arsênico e Antimônio". Journal of Inorganic and Nuclear Chemistry . 12 (3–4): 266–275. doi : 10.1016 / 0022-1902 (60) 80372-7 .



