Dicloreto de titanoceno - Titanocene dichloride
|
|

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dicloridobis (η 5- ciclopentadienil) titânio
|
|
| Outros nomes
dicloreto de titanoceno, diclorobis (ciclopentadienil) titânio (IV)
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.013.669 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 10 H 10 Cl 2 Ti | |
| Massa molar | 248,96 g / mol |
| Aparência | sólido vermelho brilhante |
| Densidade | 1,60 g / cm 3 , sólido |
| Ponto de fusão | 289 ° C (552 ° F; 562 K) |
| sl. Sol. com hidrólise | |
| Estrutura | |
| Triclínico | |
| Dist. tetraédrico | |
| Perigos | |
| Frases R (desatualizado) | R37 , R38 |
| Frases S (desatualizado) | S36 |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Compostos relacionados
|
Ferroceno zirconoceno dicloreto hafnocene dicloreto Vanadocene dicloreto Niobocene dicloreto Tantalocene dicloreto Molybdocene dicloreto Tungstenocene dicloreto de TiCl 4 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
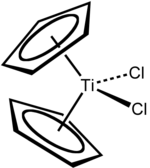
O dicloreto de titanoceno é o composto de organotitânio com a fórmula ( η 5 -C 5 H 5 ) 2 TiCl 2 , comumente abreviado como Cp 2 TiCl 2 . Este metaloceno é um reagente comum em síntese organometálica e orgânica . Ele existe como um sólido vermelho brilhante que se hidrolisa lentamente no ar. Ele mostra atividade antitumoral e foi o primeiro complexo não platinado a passar por testes clínicos como uma droga de quimioterapia .
Estrutura
O Cp 2 TiCl 2 adota uma geometria tetraédrica distorcida (contando o Cp como um ligante monodentado). A distância Ti-Cl é 2,37 Å e o ângulo Cl-Ti-Cl é 95 °.
Preparação
As preparações padrão de Cp 2 TiCl 2 começam com tetracloreto de titânio . A síntese original de Wilkinson e Birmingham, usando ciclopentadienida de sódio , ainda é comumente usada:
- 2 NaC 5 H 5 + TiCl 4 → (C 5 H 5 ) 2 TiCl 2 + 2 NaCl
Também pode ser preparado usando ciclopentadieno destilado recentemente em vez de seu derivado de sódio:
- 2 C 5 H 6 + TiCl 4 → (C 5 H 5 ) 2 TiCl 2 + 2 HCl
Reações
Reações de substituição de haleto
Cp 2 TiCl 2 é um reagente geralmente útil que efetivamente se comporta como uma fonte de Cp 2 Ti 2+ . Uma grande variedade de nucleófilos irá deslocar o cloreto. Com NaSH e com sais de polissulfeto , obtêm-se os derivados sulfido Cp 2 Ti (SH) 2 e Cp 2 TiS 5 .
O reagente Petasis , Cp 2 Ti (CH 3 ) 2 , é preparado a partir da ação do cloreto de metilmagnésio ou do metil - lítio sobre o Cp 2 TiCl 2 . Este reagente é útil para a conversão de ésteres em éteres vinílicos.
O reagente de Tebbe Cp 2 TiCl (CH 2 ) Al (CH 3 ) 2 , surge pela ação de 2 equivalentes de Al (CH 3 ) 3 em Cp 2 TiCl 2 .
Reações que afetam ligantes Cp
Um ligante Cp pode ser removido de Cp 2 TiCl 2 para dar CpTiCl 3 tetraédrico . Esta conversão pode ser realizada com TiCl 4 ou por reação com SOCl 2 .
O próprio titanoceno, TiCp 2 , é tão altamente reativo que se reorganiza em um dímero de hidreto de Ti III e tem sido objeto de muitas investigações. Este dímero pode ser capturado conduzindo a redução do dicloreto de titanoceno na presença de ligantes; na presença de benzeno , um complexo de fulvaleno , μ (η 5 : η 5 -fulvaleno) -di- (μ-hidrido) -bis (η 5- ciclopentadieniltitânio), pode ser preparado e o solvato resultante estruturalmente caracterizado por raios-X cristalografia . O mesmo composto foi relatado anteriormente por uma redução de hidreto de alumínio e lítio e redução de amálgama de sódio de dicloreto de titanoceno, e estudado por 1 H NMR antes de sua caracterização definitiva.
Redução
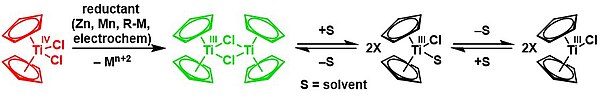
A redução com zinco dá o dímero de cloreto de bis (ciclopentadienil) titânio (III) em um equilíbrio químico mediado por solvente :
Cp 2 TiCl 2 é um precursor de derivados de Ti II . As reduções foram investigadas usando reagente de Grignard e compostos de alquil-lítio. Os redutores manuseados de forma mais conveniente incluem Mg, Al ou Zn. As sínteses a seguir demonstram alguns dos compostos que podem ser gerados pela redução do dicloreto de titanoceno na presença de ligantes aceitadores π:
- Cp 2 TiCl 2 + 2 CO + Mg → Cp 2 Ti (CO) 2 + MgCl 2
- Cp 2 TiCl 2 + 2 PR 3 + Mg → Cp 2 Ti (PR 3 ) 2 + MgCl 2
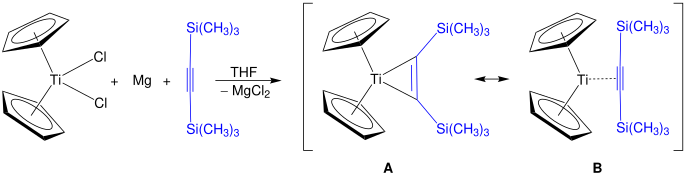
Os derivados alcino do titanoceno têm a fórmula (C 5 H 5 ) 2 Ti (C 2 R 2 ) e os correspondentes complexos de benzina são conhecidos. Uma família de derivados são os titanociclopentadienos. O reagente de Rosenthal , Cp 2 TiMe 3 (η 2 -SiC≡CSiMe 3 ), pode ser preparado por este método. Duas estruturas são mostradas, A e B , que são contribuintes de ressonância para a estrutura real do reagente de Rosenthal.
Equivalentes de titanoceno reagem com alcenil alcinos seguido por carbonilação e hidrólise para formar ciclopentadienonas bicíclicas, relacionadas à reação de Pauson-Khand ). Uma reação semelhante é a ciclização redutiva de enonas para formar o álcool correspondente de uma maneira estereosseletiva.
A redução do dicloreto de titanoceno na presença de dienos conjugados , como 1,3-butadieno, dá complexos de η 3 -alltitânio. Reações relacionadas ocorrem com diynes. Além disso, o titanoceno pode catalisar a metátese da ligação C – C para formar diinas assimétricas.
Derivados de (C 5 Me 5 ) 2 TiCl 2
Muitos análogos de Cp 2 TiCl 2 são conhecidos. Exemplos proeminentes são os derivados metilados de anel (C 5 H 4 Me) 2 TiCl 2 e (C 5 Me 5 ) 2 TiCl 2 . O complexo de etileno (C 5 Me 5 ) 2 Ti (C 2 H 4 ) pode ser sintetizado por redução de Na de (C 5 Me 5 ) 2 TiCl 2 na presença de etileno. O composto Cp não foi preparado. Esta espécie pentametilciclopentadienil (Cp *) sofre muitas reações, como cicloadições de alcinos.
Pesquisa medicinal
O dicloreto de titanoceno foi investigado como uma droga anticâncer. Na verdade, foi o primeiro complexo de coordenação sem platina e o primeiro metaloceno a passar por um ensaio clínico.
Referências
Leitura adicional
- Payack, JF; Hughes, DL; Cai, D .; Cottrell, IF; Verhoeven, TR "Dimethyltitanocene Titanium, bis ( η 5 -2,4-cyclopentadien-1-yl) dimethyl-" . Sínteses orgânicas . 79 : 19. ; Volume coletivo , 10 .
- Gambarotta, S .; Floriani, C .; Chiesi-Villa, A .; Guastini, C. (1983). "Ciclopentadienildiclorotitânio (III): um reagente semelhante a radical livre para reduzir ligações múltiplas azo (N: N) em compostos azo e diazo". Geléia. Chem. Soc. 105 (25): 7295–7301. doi : 10.1021 / ja00363a015 .
- Chirik, PJ (2010). "Grupo 4: Complexos de sanduíche de metal de transição: ainda frescos depois de quase 60 anos". Organometálicos . 29 (7): 1500–1517. doi : 10.1021 / om100016p .