Actinida -Actinide
| Parte de uma série sobre o |
| Tabela periódica |
|---|
A série actinide ( / æ k t ɪ n aɪ d / ) ou actinóide ( / æ k t ɪ n ɔɪ d / ) engloba os 15 elementos químicos metálicos com números atômicos de 89 a 103, actínio a laurêncio . A série de actinídeos deriva seu nome do primeiro elemento da série, actínio. O símbolo químico informal An é usado em discussões gerais da química dos actinídeos para se referir a qualquer actinídeo.
O "Livro Vermelho" da IUPAC de 1985 (p. 45) recomenda que se use "actinóide" em vez de "actinida" . A terminação "-ide" normalmente indica um íon negativo . No entanto, devido ao amplo uso atual, a "actinida" ainda é permitida.
Uma vez que "actinóide" significa "semelhante ao actínio" (cf. humanóide ou andróide), tem sido argumentado por razões semânticas que o actínio não pode ser logicamente um actinoide, mas a IUPAC reconhece sua inclusão com base no uso comum.
Todos os actinídeos são elementos do bloco f , exceto o último (lawrencium) que é um elemento do bloco d . Às vezes, o actínio foi considerado bloco d em vez de laurêncio, mas a classificação com laurêncio no bloco d é mais frequentemente adotada por aqueles que estudam o assunto. A série corresponde principalmente ao preenchimento da camada de elétrons 5f , embora no estado fundamental muitos tenham configurações anômalas envolvendo o preenchimento da camada 6d devido à repulsão intereletrônica. Em comparação com os lantanídeos , também principalmente elementos do bloco f , os actinídeos mostram valência muito mais variável . Todos eles têm raios atômicos e iônicos muito grandes e exibem uma gama extraordinariamente grande de propriedades físicas. Enquanto o actínio e os actinídeos tardios (a partir do amerício) se comportam de forma semelhante aos lantanídeos, os elementos tório, protactínio e urânio são muito mais semelhantes aos metais de transição em sua química, com neptúnio e plutônio ocupando uma posição intermediária.
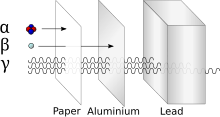
Todos os actinídeos são radioativos e liberam energia no decaimento radioativo; O urânio e o tório de ocorrência natural e o plutônio produzido sinteticamente são os actinídeos mais abundantes na Terra. Estes são usados em reatores nucleares e armas nucleares . O urânio e o tório também têm diversos usos atuais ou históricos, e o amerício é usado nas câmaras de ionização da maioria dos detectores de fumaça modernos .
Dos actinídeos, tório e urânio primordiais ocorrem naturalmente em quantidades substanciais. O decaimento radioativo do urânio produz quantidades transitórias de actínio e protactínio , e átomos de neptúnio e plutônio são ocasionalmente produzidos a partir de reações de transmutação em minérios de urânio . Os outros actinídeos são elementos puramente sintéticos . Testes de armas nucleares liberaram pelo menos seis actinídeos mais pesados que plutônio no meio ambiente ; a análise de detritos de uma explosão de uma bomba de hidrogênio em 1952 mostrou a presença de amerício , cúrio , berquélio , califórnio , einstênio e férmio .
Nas apresentações da tabela periódica , os elementos do bloco f são normalmente mostrados como duas linhas adicionais abaixo do corpo principal da tabela. Esta convenção é inteiramente uma questão de estética e praticidade de formatação; uma tabela periódica de formato largo raramente usada insere as séries 4f e 5f em seus devidos lugares, como partes da sexta e sétima linhas da tabela (períodos).
Descoberta, isolamento e síntese
| Elemento | Ano | Método |
|---|---|---|
| Neptúnio | 1940 | Bombardeando 238 U por nêutrons |
| Plutônio | 1941 | Bombardeando 238 U por deuterons |
| Amerício | 1944 | Bombardeando 239 Pu por nêutrons |
| Curium | 1944 | Bombardeamento de 239 Pu por partículas α |
| Berquélio | 1949 | Bombardeando 241 Am por partículas α |
| Californium | 1950 | Bombardeando 242 Cm por partículas α |
| Einsteinium | 1952 | Como um produto da explosão nuclear |
| Férmio | 1952 | Como um produto da explosão nuclear |
| Mendelévio | 1955 | Bombardeando 253 Es por partículas α |
| Nobélio | 1965 | Bombardeando 243 Am por 15 N ou 238 U com 22 Ne |
| Lourenço | 1961-1971 _ |
Bombardeando 252 Cf por 10 B ou 11 B e de 243 Am com 18 O |
Como os lantanídeos , os actinídeos formam uma família de elementos com propriedades semelhantes. Dentro dos actinídeos, existem dois grupos sobrepostos: elementos transurânicos , que seguem o urânio na tabela periódica ; e elementos transplutônio , que seguem o plutônio. Em comparação com os lantanídeos, que (exceto o promécio ) são encontrados na natureza em quantidades apreciáveis, a maioria dos actinídeos é rara. A maioria não ocorre na natureza, e daqueles que o fazem, apenas o tório e o urânio o fazem em quantidades maiores do que traços. Os actinídeos mais abundantes ou facilmente sintetizados são o urânio e o tório, seguidos pelo plutônio, amerício, actínio, protactínio, neptúnio e cúrio.
A existência de elementos transurânicos foi sugerida em 1934 por Enrico Fermi , com base em seus experimentos. No entanto, embora quatro actinídeos fossem conhecidos naquela época, ainda não se sabia que eles formavam uma família semelhante aos lantanídeos. A visão predominante que dominou as primeiras pesquisas sobre transurânicos era que eles eram elementos regulares no 7º período, com tório, protactínio e urânio correspondendo ao háfnio , tântalo e tungstênio do 6º período , respectivamente. A síntese de transurânicos gradualmente minou esse ponto de vista. Em 1944, uma observação de que o cúrio não exibia estados de oxidação acima de 4 (enquanto seu suposto homólogo do sexto período, platina , pode atingir o estado de oxidação de 6) levou Glenn Seaborg a formular uma " hipótese dos actinídeos ". Estudos de actinídeos conhecidos e descobertas de outros elementos transurânicos forneceram mais dados em apoio a essa posição, mas a frase "hipótese dos actinídeos" (a implicação é que uma "hipótese" é algo que não foi definitivamente comprovado) permaneceu em uso ativo pelos cientistas até o final da década de 1950.
Atualmente, existem dois métodos principais de produção de isótopos de elementos transplutônio: (1) irradiação dos elementos mais leves com nêutrons ; (2) irradiação com partículas carregadas aceleradas. O primeiro método é mais importante para aplicações, pois apenas a irradiação de nêutrons usando reatores nucleares permite a produção de quantidades consideráveis de actinídeos sintéticos; no entanto, é limitado a elementos relativamente leves. A vantagem do segundo método é que podem ser obtidos elementos mais pesados que o plutônio, bem como isótopos deficientes em nêutrons, que não são formados durante a irradiação de nêutrons.
Em 1962-1966, houve tentativas nos Estados Unidos de produzir isótopos de transplutônio usando uma série de seis explosões nucleares subterrâneas . Pequenas amostras de rocha foram extraídas da área da explosão imediatamente após o teste para estudar os produtos da explosão, mas nenhum isótopo com número de massa superior a 257 pôde ser detectado, apesar das previsões de que tais isótopos teriam meias-vidas relativamente longas de decaimento α . Essa não observação foi atribuída à fissão espontânea devido à grande velocidade dos produtos e a outros canais de decaimento, como emissão de nêutrons e fissão nuclear .
Do actínio ao urânio

Urânio e tório foram os primeiros actinídeos descobertos . O urânio foi identificado em 1789 pelo químico alemão Martin Heinrich Klaproth no minério de pechblenda . Ele o nomeou em homenagem ao planeta Urano , que havia sido descoberto oito anos antes. Klaproth foi capaz de precipitar um composto amarelo (provavelmente diuranato de sódio ) dissolvendo pechblenda em ácido nítrico e neutralizando a solução com hidróxido de sódio . Ele então reduziu o pó amarelo obtido com carvão e extraiu uma substância preta que ele confundiu com metal. Sessenta anos depois, o cientista francês Eugène-Melchior Péligot o identificou como óxido de urânio. Ele também isolou a primeira amostra de urânio metálico aquecendo tetracloreto de urânio com potássio metálico . A massa atômica do urânio foi então calculada como 120, mas Dmitri Mendeleev em 1872 corrigiu para 240 usando suas leis de periodicidade. Este valor foi confirmado experimentalmente em 1882 por K. Zimmerman.
O óxido de tório foi descoberto por Friedrich Wöhler no mineral Thorianite , que foi encontrado na Noruega (1827). Jöns Jacob Berzelius caracterizou este material com mais detalhes em 1828. Pela redução do tetracloreto de tório com potássio, ele isolou o metal e o nomeou tório em homenagem ao deus nórdico do trovão e do relâmpago Thor . O mesmo método de isolamento foi usado mais tarde por Péligot para urânio.
O actínio foi descoberto em 1899 por André-Louis Debierne , um assistente de Marie Curie , nos resíduos de pechblenda deixados após a remoção de rádio e polônio. Ele descreveu a substância (em 1899) como semelhante ao titânio e (em 1900) como semelhante ao tório. A descoberta de actínio por Debierne foi, no entanto, questionada em 1971 e 2000, argumentando que as publicações de Debierne em 1904 contradiziam seu trabalho anterior de 1899-1900. Essa visão credita o trabalho de 1902 de Friedrich Oskar Giesel , que descobriu um elemento radioativo chamado emanium que se comportava de maneira semelhante ao lantânio. O nome actínio vem do grego aktis, aktinos (ακτίς, ακτίνος), que significa feixe ou raio. Este metal foi descoberto não por sua própria radiação, mas pela radiação dos produtos derivados. Devido à estreita semelhança de actínio e lantânio e baixa abundância, actínio puro só pôde ser produzido em 1950. O termo actinídeo foi provavelmente introduzido por Victor Goldschmidt em 1937.
O protactínio foi possivelmente isolado em 1900 por William Crookes . Foi identificado pela primeira vez em 1913, quando Kasimir Fajans e Oswald Helmuth Göhring encontraram o isótopo de vida curta 234m Pa (meia-vida de 1,17 minutos) durante seus estudos do decaimento de 238 U. Eles chamaram o novo elemento de brevium (do latim brevis , que significa breve); o nome foi mudado para protoactinium (do grego πρῶτος + ἀκτίς que significa "primeiro elemento de feixe") em 1918, quando dois grupos de cientistas, liderados pela austríaca Lise Meitner e Otto Hahn da Alemanha e Frederick Soddy e John Cranston da Grã-Bretanha, descobriram independentemente o 231 Pa de vida muito mais longa . O nome foi abreviado para protactínio em 1949. Este elemento foi pouco caracterizado até 1960, quando AG Maddock e seus colaboradores no Reino Unido isolaram 130 gramas de protactínio de 60 toneladas de resíduos deixados após a extração de urânio de seu minério.
Neptúnio e acima
Neptunium (nomeado para o planeta Netuno , o próximo planeta fora de Urano, após o qual o urânio foi nomeado) foi descoberto por Edwin McMillan e Philip H. Abelson em 1940 em Berkeley, Califórnia . Eles produziram o isótopo 239 Np (meia-vida = 2,4 dias) bombardeando urânio com nêutrons lentos . Foi o primeiro elemento transurânico produzido sinteticamente.

Elementos de transurânio não ocorrem em quantidades consideráveis na natureza e são comumente sintetizados por meio de reações nucleares conduzidas com reatores nucleares. Por exemplo, sob irradiação com nêutrons do reator, o urânio-238 converte-se parcialmente em plutônio-239 :
Esta reação de síntese foi usada por Fermi e seus colaboradores no projeto dos reatores localizados no local de Hanford , que produziam quantidades significativas de plutônio-239 para as armas nucleares do Projeto Manhattan e o arsenal nuclear pós-guerra dos Estados Unidos.
Os actinídeos com os maiores números de massa são sintetizados bombardeando urânio, plutônio, cúrio e califórnio com íons de nitrogênio, oxigênio, carbono, neônio ou boro em um acelerador de partículas . Assim , o nobélio foi produzido bombardeando urânio-238 com néon-22 como
- .
Os primeiros isótopos de elementos transplutônio, amerício-241 e cúrio-242 , foram sintetizados em 1944 por Glenn T. Seaborg, Ralph A. James e Albert Ghiorso . Curium-242 foi obtido bombardeando plutônio-239 com partículas α de 32-MeV
- .
Os isótopos amerício-241 e cúrio-242 também foram produzidos pela irradiação de plutônio em um reator nuclear. O último elemento recebeu o nome de Marie Curie e seu marido Pierre , que são conhecidos por descobrir o rádio e por seu trabalho em radioatividade .
O bombardeio de cúrio-242 com partículas α resultou em um isótopo de califórnio 245 Cf (1950), e um procedimento semelhante rendeu em 1949 berquélio-243 a partir de amerício-241. Os novos elementos receberam o nome de Berkeley, Califórnia , por analogia com seu homólogo lantanídeo terbium , que recebeu o nome da vila de Ytterby , na Suécia.
Em 1945, BB Cunningham obteve o primeiro composto químico em massa de um elemento transplutônio, ou seja, hidróxido de amerício . Ao longo dos anos, quantidades de miligramas de amerício e quantidades de microgramas de cúrio foram acumuladas que permitiram a produção de isótopos de berquélio (Thomson, 1949) e califórnio (Thomson, 1950). Quantidades consideráveis desses elementos foram produzidas em 1958 (Burris B. Cunningham e Stanley G. Thomson), e o primeiro composto de califórnio (0,3 µg de CfOCl) foi obtido em 1960 por BB Cunningham e JC Wallmann.
Einsteinium e férmio foram identificados em 1952-1953 na precipitação do teste nuclear " Ivy Mike " (1 de novembro de 1952), o primeiro teste bem sucedido de uma bomba de hidrogênio. A exposição instantânea de urânio-238 a um grande fluxo de nêutrons resultante da explosão produziu isótopos pesados de urânio, incluindo urânio-253 e urânio-255, e seu decaimento β rendeu einstênio-253 e férmio-255 . A descoberta dos novos elementos e os novos dados sobre a captura de nêutrons foram inicialmente mantidos em segredo por ordem dos militares dos EUA até 1955 devido às tensões da Guerra Fria . No entanto, a equipe de Berkeley conseguiu preparar einstênio e férmio por meios civis, através do bombardeio de nêutrons de plutônio-239, e publicou este trabalho em 1954 com a ressalva de que não eram os primeiros estudos realizados sobre esses elementos. Os estudos "Ivy Mike" foram desclassificados e publicados em 1955. As primeiras quantidades significativas (submicrogramas) de einstênio foram produzidas em 1961 por Cunningham e colegas, mas isso ainda não foi feito para o férmio.
O primeiro isótopo do mendelévio, 256 Md (meia-vida de 87 min), foi sintetizado por Albert Ghiorso, Glenn T. Seaborg, Gregory R. Choppin, Bernard G. Harvey e Stanley G. Thompson quando bombardearam um alvo 253 Es com alfa partículas no cíclotron de 60 polegadas do Berkeley Radiation Laboratory ; este foi o primeiro isótopo de qualquer elemento a ser sintetizado um átomo de cada vez.
Houve várias tentativas de obtenção de isótopos de nobélio por grupos suecos (1957) e americanos (1958), mas o primeiro resultado confiável foi a síntese de 256 No pelo grupo russo ( Georgy Flyorov et al. ) em 1965, conforme reconhecido pelo IUPAC em 1992. Em seus experimentos, Flyorov et al. bombardeou urânio-238 com néon-22.
Em 1961, Ghiorso et al. obtiveram o primeiro isótopo de laurêncio irradiando califórnio (principalmente califórnio-252 ) com íons boro-10 e boro-11 . O número de massa deste isótopo não foi claramente estabelecido (possivelmente 258 ou 259) na época. Em 1965, 256 Lr foi sintetizado por Flyorov et al. de 243 Am e 18 O . Assim, a IUPAC reconheceu as equipes de física nuclear em Dubna e Berkeley como as co-descobridoras do laurencio.
Isótopos
| Propriedades nucleares de isótopos dos mais importantes isótopos de transplutônio | ||||||
|---|---|---|---|---|---|---|
| Isótopo | Meia vida | Probabilidade de fissão espontânea em % |
Energia de emissão (MeV) (rendimento em %) |
Atividade específica (Bq/kg) de | ||
| α | γ | α, β-partículas | fissão | |||
| 241 da manhã | 432.2(7) y | 4.3(18) × 10 −10 | 5,485 (84,8) 5,442 (13,1) 5,388 (1,66) |
0,059 (35,9) 0,026 (2,27) |
1,27 × 1014 | 546,1 |
| 243 da manhã | 7,37(4) × 103 anos | 3.7(2) × 10 −9 | 5,275 (87,1) 5,233 (11,2) 5,181 (1,36) |
0,074 (67,2) 0,043 (5,9) |
7,39 × 1012 | 273,3 |
| 242 centímetros | 162.8(2)d | 6.2(3) × 10 −6 | 6,069 (25,92) 6,112 (74,08) |
0,044 (0,04) 0,102 (4 × 10 −3 ) |
1,23 × 1017 | 7,6 × 109 |
| 244 centímetros | 18.10(2) y | 1,37(3) × 10 −4 | 5,762 (23,6) 5,804 (76,4) |
0,043 (0,02) 0,100 (1,5 × 10 −3 ) |
2,96 × 1015 | 4,1 × 109 |
| 245 cm | 8,5(1) × 103 anos | 6.1(9) × 10 −7 | 5,529 (0,58) 5,488 (0,83) 5,361 (93,2) |
0,175 (9,88) 0,133 (2,83) |
6,35 × 1012 | 3,9 × 104 |
| 246 centímetros | 4,76(4) × 103 anos | 0,02615(7) | 5,343 (17,8) 5,386 (82,2) |
0,045 (19) | 1,13 × 1013 | 2,95 × 109 |
| 247 centímetros | 1,56(5) × 107 anos | — | 5,267 (13,8) 5,212 (5,7) 5,147 (1,2) |
0,402 (72) 0,278 (3,4) |
3,43 × 109 | — |
| 248 centímetros | 3,48(6) × 105 anos | 8.39(16) | 5,034 (16,52) 5,078 (75) |
— | 1,40 × 1011 | 1,29 × 1010 |
| 249 Bk | 330(4) d | 4,7(2) × 10 −8 | 5,406 (1 × 10 −3 ) 5,378 (2,6 × 10 −4 ) |
0,32 (5,8 × 10 −5 ) | 5,88 × 1016 | 2,76 × 107 |
| 249 Cf. | 351(2) e | 5,0(4) × 10 −7 | 6,193 (2,46) 6,139 (1,33) 5,946 (3,33) |
0,388 (66) 0,333 (14,6) |
1,51 × 1014 | 7,57 × 105 |
| 250 Cf | 13.08(9) y | 0,077(3) | 5,988 (14,99) 6,030 (84,6) |
0,043 | 4,04 × 1015 | 3,11 × 1012 |
| 251 Cf. | 900(40) y | ? | 6,078 (2,6) 5,567 (0,9) 5,569 (0,9) |
0,177 (17,3) 0,227 (6,8) |
5,86 × 1013 | — |
| 252 Cf. | 2.645(8)a | 3.092(8) | 6,075 (15,2) 6,118 (81,6) |
0,042 (1,4 × 10 −2 ) 0,100 (1,3 × 10 −2 ) |
1,92 × 1016 | 6,14 × 1014 |
| 254 Cf. | 60.5(2) d | ≈100 | 5,834 (0,26) 5,792 (5,3 × 10 −2 ) |
— | 9,75 × 1014 | 3,13 × 1017 |
| 253 Es | 20.47(3) d | 8,7(3) × 10 −6 | 6,540 (0,85) 6,552 (0,71) 6,590 (6,6) |
0,387 (0,05) 0,429 (8 × 10 −3 ) |
9,33 × 1017 | 8,12 × 1010 |
| 254 Es | 275.7(5)d | < 3 × 10 −6 | 6,347 (0,75) 6,358 (2,6) 6,415 (1,8) |
0,042 (100) 0,034 (30) |
6,9 × 1016 | — |
| 255 Es | 39.8(12)d | 0,0041(2) | 6,267 (0,78) 6,401 (7) |
— | 4,38 × 1017 (β) 3,81 × 1016 (α) |
1,95 × 1013 |
| 255 Fm | 20.07(7)h | 2,4(10) × 10 −5 | 7,022 (93,4) 6,963 (5,04) 6,892 (0,62) |
0,00057 (19,1) 0,081 (1) |
2,27 × 1019 | 5,44 × 1012 |
| 256 Fm | 157,6(13) min | 91.9(3) | 6,872 (1,2) 6,917 (6,9) |
— | 1,58 × 1020 | 1,4 × 1019 |
| 257 Fm | 100,5(2) d | 0,210(4) | 6,752 (0,58) 6,695 (3,39) 6,622 (0,6) |
0,241 (11) 0,179 (8,7) |
1,87 × 1017 | 3,93 × 1014 |
| 256 Md | 77(2) min | — | 7,142 (1,84) 7,206 (5,9) |
— | 3,53 × 1020 | — |
| 257 Md | 5.52(5)h | — | 7.074 (14) | 0,371 (11,7) 0,325 (2,5) |
8,17 × 1019 | — |
| 258 Md | 51.5(3) d | — | 6,73 | — | 3,64 × 1017 | — |
| 255 Não | 3.1(2) min | — | 8,312 (1,16) 8,266 (2,6) 8,121 (27,8) |
0,187 (3,4) | 8,78 × 1021 | — |
| 259 Não | 58(5) min | — | 7,455 (9,8) 7,500 (29,3) 7,533 (17,3) |
— | 4,63 × 1020 | — |
| 256 Lr | 27(3) s | < 0,03 | 8,319 (5,4) 8,390 (16) 8,430 (33) |
— | 5,96 × 1022 | — |
| 257 Lr | 646(25) ms | — | 8,796 (18) 8,861 (82) |
— | 1,54 × 1024 | — |
32 isótopos de actínio e oito estados isoméricos excitados de alguns de seus nuclídeos foram identificados até 2016. Três isótopos, 225 Ac , 227 Ac e 228 Ac , foram encontrados na natureza e os demais foram produzidos em laboratório; apenas os três isótopos naturais são usados em aplicações. Actinium-225 é um membro da série de neptúnio radioativo ; foi descoberto pela primeira vez em 1947 como um produto de decaimento do urânio-233 , é um emissor α com meia-vida de 10 dias. O actínio-225 é menos disponível do que o actínio-228, mas é mais promissor em aplicações de radiotraçadores. Actínio-227 (meia-vida de 21,77 anos) ocorre em todos os minérios de urânio, mas em pequenas quantidades. Um grama de urânio (em equilíbrio radioativo) contém apenas 2 × 10-10 gramas de 227 Ac. O actínio-228 é um membro da série radioativa do tório formado pelo decaimento de 228 Ra ; é um emissor β − com meia-vida de 6,15 horas. Em uma tonelada de tório há 5 × 10-8 gramas de 228 Ac. Foi descoberto por Otto Hahn em 1906.
Existem 31 isótopos conhecidos de tório que variam em número de massa de 208 a 238. Destes, o mais longevo é 232 Th, cuja meia-vida de1,4 × 10 10 anos significa que ainda existe na natureza como um nuclídeo primordial . O próximo de vida mais longa é 230 Th, um produto de decaimento intermediário de 238 U com meia-vida de 75.400 anos. Vários outros isótopos de tório têm meia-vida ao longo de um dia; todos estes também são transitórios nas cadeias de decaimento de 232 Th, 235 U e 238 U.
28 isótopos de protactínio são conhecidos com números de massa 212-239, bem como três estados isoméricos excitados . Apenas 231 Pa e 234 Pa foram encontrados na natureza. Todos os isótopos têm vida curta, exceto o protactínio-231 (meia-vida de 32.760 anos). Os isótopos mais importantes são 231 Pa e 233 Pa , que é um produto intermediário na obtenção de urânio-233 e é o mais acessível entre os isótopos artificiais de protactínio. O 233 Pa tem meia-vida e energia convenientes da radiação γ e, portanto, foi usado na maioria dos estudos de química do protactínio. O protactínio-233 é um emissor β com meia-vida de 26,97 dias.
Existem 26 isótopos conhecidos de urânio , com números de massa 215–242 (exceto 220 e 241). Três deles, 234 U , 235 U e 238 U, estão presentes em apreciáveis quantidades na natureza. Entre outros, o mais importante é o 233 U, que é um produto final da transformação do 232 Th irradiado por nêutrons lentos. 233 U tem uma eficiência de fissão muito maior por nêutrons de baixa energia (térmicos), em comparação, por exemplo, com 235 U. A maioria dos estudos de química de urânio foram realizados em urânio-238 devido à sua longa meia-vida de 4,4 × 109 anos.
Existem 24 isótopos de neptúnio com números de massa de 219, 220 e 223-244; são todos altamente radioativos. Os mais populares entre os cientistas são 237 Np de longa duração (t 1/2 = 2,20 × 106 anos) e de curta duração 239 Np, 238 Np (t 1/2 ~ 2 dias).
Dezoito isótopos de amerício são conhecidos com números de massa de 229 a 247 (com exceção de 231). Os mais importantes são 241 Am e 243 Am, que são emissores alfa e também emitem raios γ suaves, mas intensos; ambos podem ser obtidos em uma forma isotopicamente pura. As propriedades químicas do amerício foram estudadas pela primeira vez com 241 Am, mas depois mudaram para 243 Am, que é quase 20 vezes menos radioativo. A desvantagem do 243 Am é a produção do isótopo filho de vida curta 239 Np, que deve ser considerado na análise dos dados.
Entre 19 isótopos de cúrio , variando em número de massa de 233 a 251, os mais acessíveis são 242 Cm e 244 Cm; eles são α-emissores, mas com vida muito mais curta do que os isótopos de amerício. Esses isótopos quase não emitem radiação γ, mas sofrem fissão espontânea com a emissão associada de nêutrons. Mais isótopos de cúrio de vida longa ( 245-248 cm, todos os emissores α) são formados como uma mistura durante a irradiação de nêutrons de plutônio ou amerício. Sob irradiação curta, esta mistura é dominada por 246 Cm, e então 248 Cm começam a se acumular. Ambos os isótopos, especialmente 248 cm, têm uma meia-vida mais longa (3,48 × 105 anos) e são muito mais convenientes para a realização de pesquisas químicas do que 242 Cm e 244 Cm, mas também têm uma taxa bastante alta de fissão espontânea. 247 cm tem a vida mais longa entre os isótopos de cúrio (1,56 × 107 anos), mas não se forma em grandes quantidades devido à forte fissão induzida por nêutrons térmicos.
Dezessete isótopos de berquélio foram identificados com números de massa 233-234, 236, 238 e 240-252. Apenas 249 Bk estão disponíveis em grandes quantidades; tem uma meia-vida relativamente curta de 330 dias e emite principalmente partículas β moles , que são inconvenientes para detecção. Sua radiação alfa é bastante fraca (1,45 × 10-3 % em relação à radiação β), mas às vezes é usado para detectar esse isótopo. 247 Bk é um emissor alfa com meia-vida longa de 1.380 anos, mas de difícil obtenção em quantidades apreciáveis; não é formado por irradiação de nêutrons de plutônio por causa da estabilidade β de isótopos de isótopos de cúrio com número de massa abaixo de 248.
Os 20 isótopos de califórnio com números de massa 237–256 são formados em reatores nucleares; californium-253 é um emissor β e o resto são emissores α. Os isótopos com números de massa pares ( 250 Cf, 252 Cf e 254 Cf) têm uma alta taxa de fissão espontânea, especialmente 254 Cf dos quais 99,7% decaem por fissão espontânea. O califórnio-249 tem meia-vida relativamente longa (352 anos), fissão espontânea fraca e forte emissão γ que facilita sua identificação. O 249 Cf não é formado em grandes quantidades em um reator nuclear devido ao lento decaimento β do isótopo original 249 Bk e uma grande seção transversal de interação com nêutrons, mas pode ser acumulado na forma isotopicamente pura como o decaimento β produto de (pré-selecionado) 249 Bk. O califórnio produzido por irradiação de plutônio por reator consiste principalmente em 250 Cf e 252 Cf, sendo este último predominante para grandes fluências de nêutrons, e seu estudo é dificultado pela forte radiação de nêutrons.
Isótopo pai |
1/2 _ | Isótopo filha |
1/2 _ | Tempo para estabelecer o equilíbrio radioativo |
|---|---|---|---|---|
| 243 da manhã | 7370 anos | 239 Np | 2,35 dias | 47,3 dias |
| 245 cm | 8265 anos | 241 Pu | 14 anos | 129 anos |
| 247 centímetros | 1,64 × 107 anos | 243 Pu | 4,95 horas | 7,2 dias |
| 254 Es | 270 dias | 250 Bk | 3,2 horas | 35,2 horas |
| 255 Es | 39,8 dias | 255 Fm | 22 horas | 5 dias |
| 257 Fm | 79 dias | 253 Cf. | 17,6 dias | 49 dias |
Entre os 18 isótopos conhecidos de einstênio com números de massa de 240 a 257, o mais acessível é 253 Es. É um emissor α com meia-vida de 20,47 dias, uma emissão γ relativamente fraca e pequena taxa de fissão espontânea em comparação com os isótopos do califórnio. A irradiação prolongada de nêutrons também produz um isótopo de vida longa 254 Es (t 1/2 = 275,5 dias).
Vinte isótopos de férmio são conhecidos com números de massa de 241-260. 254 Fm, 255 Fm e 256 Fm são emissores α com meia-vida curta (horas), que podem ser isolados em quantidades significativas. 257 Fm (t 1/2 = 100 dias) podem se acumular após irradiação prolongada e forte. Todos esses isótopos são caracterizados por altas taxas de fissão espontânea.
Entre os 17 isótopos conhecidos do mendelévio (números de massa de 244 a 260), o mais estudado é o 256 Md, que decai principalmente através da captura de elétrons (radiação α é ≈10%) com meia-vida de 77 minutos. Outro emissor alfa, 258 Md, tem meia-vida de 53 dias. Ambos os isótopos são produzidos a partir de einstênio raro ( 253 Es e 255 Es respectivamente), o que limita sua disponibilidade.
Isótopos de vida longa de nobélio e isótopos de lawrencium (e de elementos mais pesados) têm meias-vidas relativamente curtas. Para o nobélio, 11 isótopos são conhecidos com números de massa 250–260 e 262. As propriedades químicas do nobélio e do laurêncio foram estudadas com 255 No (t 1/2 = 3 min) e 256 Lr (t 1/2 = 35 s). O isótopo de nobélio de vida mais longa, 259 No, tem uma meia-vida de aproximadamente 1 hora. Lawrencium tem 13 isótopos conhecidos com números de massa 251–262 e 266. O mais estável de todos é 266 Lr com meia-vida de 11 horas.
Entre todos estes, os únicos isótopos que ocorrem em quantidades suficientes na natureza para serem detectados em algo além de traços e têm uma contribuição mensurável para os pesos atômicos dos actinídeos são os primordiais 232 Th, 235 U e 238 U, e três produtos de decaimento de vida longa de urânio natural, 230 Th, 231 Pa e 234 U. O tório natural consiste em 0,02(2)% 230 Th e 99,98(2)% 232 Th; protactínio natural consiste em 100% 231 Pa; e o urânio natural consiste em 0,0054(5)% 234 U, 0,7204(6)% 235 U e 99,2742(10)% 238 U.
Formação em reatores nucleares
A figura acumulada de actinídeos é uma tabela de nuclídeos com o número de nêutrons no eixo horizontal (isótopos) e o número de prótons no eixo vertical (elementos). O ponto vermelho divide os nuclídeos em dois grupos, então a figura é mais compacta. Cada nuclídeo é representado por um quadrado com o número de massa do elemento e seu meio-tempo. Os isótopos de actinídeos naturalmente existentes (Th, U) são marcados com uma borda em negrito, os emissores alfa têm uma cor amarela e os emissores beta têm uma cor azul. Rosa indica captura de elétrons ( 236 Np), enquanto branco representa um estado metaestável de longa duração ( 242 Am).
A formação de nuclídeos actinídeos é caracterizada principalmente por:
- Reações de captura de nêutrons (n,γ), que são representadas na figura por uma seta curta para a direita.
- As reações (n,2n) e as reações de ocorrência menos frequente (γ,n) também são levadas em consideração, ambas marcadas por uma seta curta para a esquerda.
- Ainda mais raramente e apenas desencadeada por nêutrons rápidos, ocorre a reação (n,3n), que é representada na figura com um exemplo, marcado por uma longa seta para a esquerda.
Além dessas reações nucleares induzidas por nêutrons ou gama, a conversão radioativa de nuclídeos de actinídeos também afeta o estoque de nuclídeos em um reator. Esses tipos de decaimento estão marcados na figura por setas diagonais. O decaimento beta-minus , marcado com uma seta apontando para cima-esquerda, desempenha um papel importante para o equilíbrio das densidades de partículas dos nuclídeos. Nuclídeos que decaem por emissão de pósitrons (decaimento beta-plus) ou captura de elétrons (ϵ) não ocorrem em um reator nuclear, exceto como produtos de reações de nocaute; seus decaimentos são marcados com setas apontando para baixo-direita. Devido às longas meias-vidas dos nuclídeos dados, o decaimento alfa quase não desempenha nenhum papel na formação e decaimento dos actinídeos em um reator de energia, pois o tempo de residência do combustível nuclear no núcleo do reator é bastante curto (alguns anos ). As exceções são os dois nuclídeos de vida relativamente curta 242 Cm (T 1/2 = 163 d) e 236 Pu (T 1/2 = 2,9 y). Apenas para esses dois casos, o decaimento α é marcado no mapa de nuclídeos por uma longa seta apontando para baixo-esquerda.
Distribuição na natureza
Tório e urânio são os actinídeos mais abundantes na natureza com as respectivas concentrações de massa de 16 ppm e 4 ppm. O urânio ocorre principalmente na crosta terrestre como uma mistura de seus óxidos no mineral uraninita , que também é chamado de pechblenda por causa de sua cor preta. Existem várias dezenas de outros minerais de urânio , como carnotita (KUO 2 VO 4 ·3H 2 O) e autunita (Ca(UO 2 ) 2 (PO 4 ) 2 ·nH 2 O). A composição isotópica do urânio natural é 238 U (abundância relativa 99,2742%), 235 U (0,7204%) e 234 U (0,0054%); destes 238 U tem a maior meia-vida de 4,51 × 109 anos. A produção mundial de urânio em 2009 foi de 50.572 toneladas , das quais 27,3% foram extraídas no Cazaquistão . Outros importantes países mineradores de urânio são Canadá (20,1%), Austrália (15,7%), Namíbia (9,1%), Rússia (7,0%) e Níger (6,4%).
| Minério | Localização | Teor de urânio , % |
Relação de massa 239 Pu/minério |
Relação 239 Pu/U ( × 1012 ) |
|---|---|---|---|---|
| Uraninita | Canadá | 13,5 | 9,1 × 10−12 | 7.1 |
| Uraninita | Congo | 38 | 4,8 × 10−12 | 12 |
| Uraninita | Colorado , EUA | 50 | 3,8 × 10−12 | 7,7 |
| Monazita | Brasil | 0,24 | 2,1 × 10−14 | 8.3 |
| Monazita | Carolina do Norte , EUA | 1,64 | 5,9 × 10−14 | 3.6 |
| Fergusonita | - | 0,25 | <1 × 10−14 | <4 |
| Carnotita | - | 10 | <4 × 10−14 | <0,4 |
Os minerais de tório mais abundantes são torianita (ThO 2 ), torita (ThSiO 4 ) e monazita , ((Th,Ca,Ce)PO 4 ). A maioria dos minerais de tório contém urânio e vice-versa; e todos eles têm fração significativa de lantanídeos. Depósitos ricos de minerais de tório estão localizados nos Estados Unidos (440.000 toneladas), Austrália e Índia (~300.000 toneladas cada) e Canadá (~100.000 toneladas).
A abundância de actínio na crosta terrestre é apenas cerca de 5 × 10-15 %. O actínio está presente principalmente em urânio, mas também em outros minerais, embora em quantidades muito menores. O conteúdo de actínio na maioria dos objetos naturais corresponde ao equilíbrio isotópico do isótopo parental 235 U, e não é afetado pela migração fraca de Ac. O protactínio é mais abundante ( 10-12 %) na crosta terrestre do que o actínio. Foi descoberto no minério de urânio em 1913 por Fajans e Göhring. Como actínio, a distribuição de protactínio segue a de 235 U.
A meia-vida do isótopo de neptúnio de vida mais longa, 237 Np , é insignificante em comparação com a idade da Terra. Assim, o neptúnio está presente na natureza em quantidades insignificantes produzidas como produtos intermediários de decaimento de outros isótopos. Traços de plutônio em minerais de urânio foram encontrados pela primeira vez em 1942, e os resultados mais sistemáticos sobre 239 Pu estão resumidos na tabela (nenhum outro isótopo de plutônio pode ser detectado nessas amostras). O limite superior de abundância do isótopo de plutônio de vida mais longa, 244 Pu, é 3 × 10-20 %. O plutônio não pôde ser detectado em amostras de solo lunar. Devido à sua escassez na natureza, a maior parte do plutônio é produzido sinteticamente.
Extração

Devido à baixa abundância de actinídeos, sua extração é um processo complexo de várias etapas. Fluoretos de actinídeos são geralmente usados porque são insolúveis em água e podem ser facilmente separados com reações redox . Os fluoretos são reduzidos com cálcio , magnésio ou bário :
Entre os actinídeos, o tório e o urânio são os mais fáceis de isolar. O tório é extraído principalmente da monazita : o pirofosfato de tório (ThP 2 O 7 ) é reagido com ácido nítrico e o nitrato de tório produzido é tratado com fosfato de tributilo . Impurezas de terras raras são separadas aumentando o pH em solução de sulfato.
Em outro método de extração, a monazita é decomposta com uma solução aquosa de hidróxido de sódio a 45% a 140°C. Hidróxidos metálicos misturados são extraídos primeiro, filtrados a 80°C, lavados com água e dissolvidos com ácido clorídrico concentrado . Em seguida, a solução ácida é neutralizada com hidróxidos para pH = 5,8 que resulta na precipitação de hidróxido de tório (Th(OH) 4 ) contaminado com ~3% de hidróxidos de terras raras; o restante dos hidróxidos de terras raras permanece em solução. O hidróxido de tório é dissolvido em um ácido inorgânico e então purificado a partir dos elementos de terras raras . Um método eficiente é a dissolução do hidróxido de tório em ácido nítrico, pois a solução resultante pode ser purificada por extração com solventes orgânicos:
- Th(OH) 4 + 4 HNO 3 → Th(NO 3 ) 4 + 4 H 2 O
O tório metálico é separado do óxido anidro, cloreto ou fluoreto por reação com cálcio em atmosfera inerte:
- ThO 2 + 2 Ca → 2 CaO + Th
Às vezes, o tório é extraído por eletrólise de um fluoreto em uma mistura de cloreto de sódio e potássio a 700-800 ° C em um cadinho de grafite . O tório altamente puro pode ser extraído de seu iodeto com o processo de barra de cristal .
O urânio é extraído de seus minérios de várias maneiras. Em um método, o minério é queimado e então reagido com ácido nítrico para converter o urânio em um estado dissolvido. O tratamento da solução com uma solução de tributil fosfato (TBP) em querosene transforma o urânio em uma forma orgânica UO 2 (NO 3 ) 2 (TBP) 2 . As impurezas insolúveis são filtradas e o urânio é extraído por reação com hidróxidos como (NH 4 ) 2 U 2 O 7 ou com peróxido de hidrogênio como UO 4 ·2H 2 O.
Quando o minério de urânio é rico em minerais como dolomita , magnesita , etc., esses minerais consomem muito ácido. Neste caso, o método do carbonato é usado para extração de urânio. Seu principal componente é uma solução aquosa de carbonato de sódio , que converte o urânio em um complexo [UO 2 (CO 3 ) 3 ] 4− , que é estável em soluções aquosas em baixas concentrações de íons hidróxido. As vantagens do método do carbonato de sódio são que os produtos químicos têm baixa corrosividade (em comparação com os nitratos) e que a maioria dos metais não urânio precipita da solução. A desvantagem é que os compostos de urânio tetravalentes também precipitam. Portanto, o minério de urânio é tratado com carbonato de sódio em temperatura elevada e sob pressão de oxigênio:
- 2 UO 2 + O 2 + 6 CO2-3
_→ 2 [UO 2 (CO 3 ) 3 ] 4−
Esta equação sugere que o melhor solvente para o processamento do carbonato de urânio é uma mistura de carbonato com bicarbonato. Em pH alto, isso resulta na precipitação de diuranato, que é tratado com hidrogênio na presença de níquel, produzindo um tetracarbonato de urânio insolúvel.
Outro método de separação utiliza resinas poliméricas como polieletrólito . Os processos de troca iônica nas resinas resultam na separação do urânio. O urânio das resinas é lavado com uma solução de nitrato de amônio ou ácido nítrico que produz nitrato de uranila , UO 2 (NO 3 ) 2 ·6H 2 O. Quando aquecido, ele se transforma em UO 3 , que é convertido em UO 2 com hidrogênio:
- UO 3 + H 2 → UO 2 + H 2 O
A reação do dióxido de urânio com ácido fluorídrico o transforma em tetrafluoreto de urânio , que produz urânio metálico após a reação com magnésio metálico:
- 4 HF + UO 2 → UF 4 + 2 H 2 O
Para extrair plutônio, urânio irradiado com nêutrons é dissolvido em ácido nítrico e um agente redutor ( FeSO4 , ou H2O2 ) é adicionado à solução resultante . Essa adição altera o estado de oxidação do plutônio de +6 para +4, enquanto o urânio permanece na forma de nitrato de uranila (UO 2 (NO 3 ) 2 ). A solução é tratada com um agente redutor e neutralizada com carbonato de amônio até pH = 8 que resulta na precipitação de compostos Pu 4+ .
Em outro método, Pu 4+ e UO2+
2são extraídos primeiro com fosfato de tributilo, depois reagem com hidrazina lavando o plutônio recuperado.
A maior dificuldade na separação do actínio é a semelhança de suas propriedades com as do lantânio. Assim, o actínio é sintetizado em reações nucleares a partir de isótopos de rádio ou separado usando procedimentos de troca iônica.
Propriedades
Os actinídeos têm propriedades semelhantes aos lantanídeos. As camadas eletrônicas de 6 d e 7 s são preenchidas com actínio e tório, e a camada 5 f está sendo preenchida com aumento adicional do número atômico; a casca 4 f é preenchida com os lantanídeos. A primeira evidência experimental para o preenchimento da camada 5 f em actinídeos foi obtida por McMillan e Abelson em 1940. Como em lantanídeos (veja contração de lantanídeos ), o raio iônico de actinídeos diminui monotonicamente com o número atômico (veja também princípio de Aufbau ).
| Elemento | Ac | º | Pai | você | Np | Pu | Sou | Cm | Bk | Cf | Es | Fm | Md | Não | Lr |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Carga do núcleo ( Z ) | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 |
| massa atômica | [227] | 232.0377(4) | 231.03588(2) | 238.02891(3) | [237] | [244] | [243] | [247] | [247] | [251] | [252] | [257] | [258] | [259] | [266] |
| Número de isótopos naturais | 3 | 7 | 3 | 8 | 3 | 4 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Isótopos naturais | 225, 227-228 | 227–232, 234 | 231, 233-234 | 233–240 | 237, 239-240 | 238–240, 244 | — | — | — | — | — | — | — | — | — |
| Isótopos de quantidade natural | — | 230, 232 | 231 | 234, 235, 238 | — | — | — | — | — | — | — | — | — | — | — |
| Isótopo de vida mais longa | 227 | 232 | 231 | 238 | 237 | 244 | 243 | 247 | 247 | 251 | 252 | 257 | 258 | 259 | 266 |
| Meia-vida do isótopo de vida mais longa | 21,8 anos | 14 bilhões de anos | 32.500 anos | 4,47 bilhões de anos | 2,14 milhões de anos | 80,8 milhões de anos | 7.370 anos | 15,6 milhões de anos | 1.380 anos | 900 anos | 1,29 anos | 100,5 dias | 52 dias | 58 minutos | 11 horas |
| Isótopo mais comum | 227 | 232 | 231 | 238 | 237 | 239 | 241 | 244 | 249 | 252 | 253 | 255 | 256 | 255 | 260 |
| Meia-vida do isótopo mais comum | 21,8 anos | 14 bilhões de anos | 32.500 anos | 4,47 bilhões de anos | 2,14 milhões de anos | 24.100 anos | 433 anos | 18,1 anos | 320 dias | 2,64 anos | 20,47 dias | 20.07 horas | 78 minutos | 3,1 minutos | 2,7 minutos |
| Configuração eletrônica no estado fundamental (fase gasosa) |
6d 1 7s 2 | 6d 2 7s 2 | 5f 2 6d 1 7s 2 | 5f 3 6d 1 7s 2 | 5f 4 6d 1 7s 2 | 5f 6 7s 2 | 5f 7 7s 2 | 5f 7 6d 1 7s 2 | 5f 9 7s 2 | 5f 10 7s 2 | 5f 11 7s 2 | 5f 12 7s 2 | 5f 13 7s 2 | 5f 14 7s 2 | 5f 14 7s 2 7p 1 |
| Estados de oxidação | 2, 3 | 2, 3, 4 | 2, 3, 4, 5 | 2, 3, 4, 5, 6 | 3, 4, 5 , 6, 7 | 3, 4 , 5, 6, 7 | 2, 3 , 4, 5, 6, 7 | 2, 3 , 4, 6 | 2, 3 , 4 | 2, 3 , 4 | 2, 3 , 4 | 2, 3 | 2, 3 | 2 , 3 | 3 |
| Raio metálico (nm) | 0,203 | 0,180 | 0,162 | 0,153 | 0,150 | 0,162 | 0,173 | 0,174 | 0,170 | 0,186 | 0,186 | ? 0,198 | ? 0,194 | ? 0,197 | ? 0,171 |
| Raio iônico (nm): An 4+ An 3+ |
- 0,126 |
0,114 — |
0,104 0,118 |
0,103 0,118 |
0,101 0,116 |
0,100 0,115 |
0,099 0,114 |
0,099 0,112 |
0,097 0,110 |
0,096 0,109 |
0,085 0,098 |
0,084 0,091 |
0,084 0,090 |
0,084 0,095 |
0,083 0,088 |
| Temperatura (°C): fusão ebulição |
1050 3198 |
1842 4788 |
1568 ? 4027 |
1132,2 4131 |
639 ? 4174 |
639,4 3228 |
1176 ? 2607 |
1340 3110 |
986 2627 |
900 ? 1470 |
860 ? 996 |
1530 — |
830 — |
830 — |
1630 — |
| Densidade, g/cm 3 | 10.07 | 11,78 | 15,37 | 19.06 | 20,45 | 19,84 | 11,7 | 13,51 | 14,78 | 15.1 | 8,84 | ? 9.7 | ? 10.3 | ? 9,9 | ? 14,4 |
| Potencial de eletrodo padrão (V): E ° (An 4+ /An 0 ) E ° (An 3+ /An 0 ) |
— −2,13 |
−1,83 — |
−1,47 — |
−1,38 −1,66 |
−1,30 −1,79 |
−1,25 −2,00 |
−0,90 −2,07 |
−0,75 −2,06 |
−0,55 −1,96 |
−0,59 −1,97 |
−0,36 −1,98 |
−0,29 −1,96 |
— −1,74 |
— −1,20 |
— −2,10 |
| Cor: [M(H 2 O) n ] 4+ [M(H 2 O) n ] 3+ |
— Incolor |
Azul incolor |
Amarelo Azul escuro |
Verde Roxo |
Amarelo-verde Roxo |
Violeta Marrom |
Rosa Vermelha |
Amarelo Incolor |
Bege Amarelo-esverdeado |
Verde Verde |
— Rosa |
— — |
— — |
— — |
— — |
| Cores aproximadas dos íons actinídeos em solução aquosa As cores dos actinídeos 100-103 são desconhecidas, pois quantidades suficientes ainda não foram sintetizadas
|
|||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Actinida ( Z ) | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 |
| Estado de oxidação | |||||||||||||||
| +2 | Fm 2+ | Md 2+ | Não 2+ | ||||||||||||
| +3 | Ac 3+ | Th 3+ | Pa 3+ | U 3+ | Np 3+ | Pu 3+ | Tenho 3+ | Cm 3+ | Bk 3+ | Cf 3+ | É 3+ | Fm 3+ | Md 3+ | Não 3+ | Lr 3+ |
| +4 | 4+ _ | Pa 4+ | U 4+ | Np 4+ | Pu 4+ | Sou 4+ | Cm 4+ | Bk 4+ | Cf 4+ | ||||||
| +5 |
PaO+ 2 |
UO+ 2 |
NpO+ 2 |
PuO+ 2 |
AmO+ 2 |
||||||||||
| +6 |
UO2+ 2 |
NpO2+ 2 |
PuO2+ 2 |
AmO2+ 2 |
CmO2+ |
||||||||||
| +7 |
NpO3+ 2 |
PuO3+ 2 |
AmO3-5 _ |
||||||||||||
Propriedades físicas
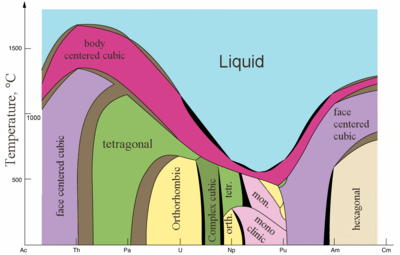
|
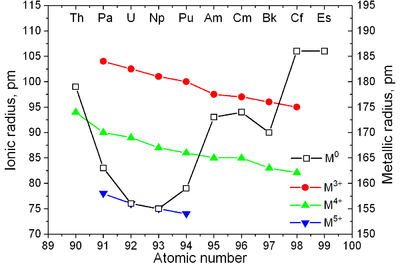
|
| Principais estruturas cristalinas de alguns actinídeos versus temperatura | Raios metálicos e iônicos de actinídeos |

Os actinídeos são metais típicos. Todos eles são macios e têm uma cor prateada (mas mancham ao ar), densidade e plasticidade relativamente altas. Alguns deles podem ser cortados com uma faca. Sua resistividade elétrica varia entre 15 e 150 µΩ·cm. A dureza do tório é semelhante à do aço macio, de modo que o tório puro aquecido pode ser enrolado em folhas e puxado em arame. O tório tem quase a metade da densidade do urânio e do plutônio, mas é mais duro do que qualquer um deles. Todos os actinídeos são radioativos, paramagnéticos e, com exceção do actínio, possuem várias fases cristalinas: plutônio possui sete e urânio, neptúnio e califórnio três. As estruturas cristalinas de protactínio, urânio, neptúnio e plutônio não possuem análogos claros entre os lantanídeos e são mais semelhantes às dos metais de transição 3d .
Todos os actinídeos são pirofóricos , especialmente quando finamente divididos, ou seja, inflamam-se espontaneamente ao reagir com o ar à temperatura ambiente. O ponto de fusão dos actinídeos não tem uma dependência clara do número de elétrons f . O ponto de fusão incomumente baixo de neptúnio e plutônio (~640 ° C) é explicado pela hibridização dos orbitais 5 f e 6 d e pela formação de ligações direcionais nesses metais.
| Lantanídeos | Ln 3+ , Å | Actinídeos | Um 3+ , Å | Um 4+ , Å |
|---|---|---|---|---|
| Lantânio | 1.061 | Actínio | 1.11 | – |
| Cério | 1.034 | Tório | 1,08 | 0,99 |
| Praseodímio | 1.013 | Protactínio | 1,05 | 0,93 |
| Neodímio | 0,995 | Urânio | 1,03 | 0,93 |
| Promécio | 0,979 | Neptúnio | 1,01 | 0,92 |
| Samário | 0,964 | Plutônio | 1,00 | 0,90 |
| Európio | 0,950 | Amerício | 0,99 | 0,89 |
| Gadolínio | 0,938 | Curium | 0,98 | 0,88 |
| Térbio | 0,923 | Berquélio | – | – |
| Disprósio | 0,908 | Californium | – | – |
| Hólmio | 0,894 | Einsteinium | – | – |
| Érbio | 0,881 | Férmio | – | – |
| Túlio | 0,869 | Mendelévio | – | – |
| Itérbio | 0,858 | Nobélio | – | – |
| Lutécio | 0,848 | Lourenço | – | – |
Propriedades quimicas
Como os lantanídeos, todos os actinídeos são altamente reativos com halogênios e calcogênios ; no entanto, os actinídeos reagem mais facilmente. Actinídeos, especialmente aqueles com um pequeno número de elétrons 5 f , são propensos à hibridização . Isso é explicado pela similaridade das energias dos elétrons nas camadas 5f , 7s e 6d . A maioria dos actinídeos exibe uma variedade maior de estados de valência, e os mais estáveis são +6 para urânio, +5 para protactínio e neptúnio, +4 para tório e plutônio e +3 para actínio e outros actinídeos.
O actínio é quimicamente semelhante ao lantânio, o que é explicado por seus raios iônicos e estruturas eletrônicas semelhantes. Como o lantânio, o actínio quase sempre tem um estado de oxidação de +3 em compostos, mas é menos reativo e possui propriedades básicas mais pronunciadas . Entre outros actinídeos trivalentes, Ac 3+ é menos ácido, ou seja, tem a tendência mais fraca para hidrolisar em soluções aquosas.
O tório é bastante ativo quimicamente. Devido à falta de elétrons nos orbitais 6 d e 5 f , os compostos tetravalentes de tório são incolores. Em pH < 3, as soluções de sais de tório são dominadas pelos cátions [Th(H 2 O) 8 ] 4+ . O íon Th 4+ é relativamente grande e dependendo do número de coordenação pode ter um raio entre 0,95 e 1,14 Å. Como resultado, os sais de tório têm uma tendência fraca para hidrolisar. A habilidade distintiva dos sais de tório é sua alta solubilidade tanto em água quanto em solventes orgânicos polares.
O protactínio apresenta dois estados de valência; o +5 é estável, e o estado +4 oxida-se facilmente a protactínio(V). Assim, o protactínio tetravalente em soluções é obtido pela ação de agentes redutores fortes em uma atmosfera de hidrogênio. O protactínio tetravalente é quimicamente semelhante ao urânio (IV) e ao tório (IV). Fluoretos, fosfatos, hipofosfato, iodato e fenilarsonatos de protactínio(IV) são insolúveis em água e ácidos diluídos. O protactínio forma carbonatos solúveis. As propriedades hidrolíticas do protactínio pentavalente são próximas às do tântalo (V) e do nióbio (V). O comportamento químico complexo do protactínio é consequência do início do preenchimento da camada 5 f neste elemento.
O urânio tem uma valência de 3 a 6, sendo a última a mais estável. No estado hexavalente, o urânio é muito semelhante aos elementos do grupo 6 . Muitos compostos de urânio(IV) e urânio(VI) são não estequiométricos , ou seja, têm composição variável. Por exemplo, a fórmula química real do dióxido de urânio é UO 2+x , onde x varia entre -0,4 e 0,32. Os compostos de urânio (VI) são oxidantes fracos . A maioria deles contém o grupo linear " uranil ", UO2+
2. Entre 4 e 6 ligantes podem ser acomodados em um plano equatorial perpendicular ao grupo uranila. O grupo uranila atua como um ácido duro e forma complexos mais fortes com ligantes doadores de oxigênio do que com ligantes doadores de nitrogênio. NpO2+
2e PuO2+
2são também a forma comum de Np e Pu no estado de oxidação +6. Os compostos de urânio(IV) exibem propriedades redutoras, por exemplo, são facilmente oxidados pelo oxigênio atmosférico. O urânio(III) é um agente redutor muito forte. Devido à presença de d-shell, o urânio (assim como muitos outros actinídeos) forma compostos organometálicos , como U III (C 5 H 5 ) 3 e U IV (C 5 H 5 ) 4 .
O neptúnio tem estados de valência de 3 a 7, que podem ser observados simultaneamente em soluções. O estado mais estável em solução é +5, mas a valência +4 é preferida em compostos de neptúnio sólido. O metal Neptúnio é muito reativo. Íons de neptúnio são propensos a hidrólise e formação de compostos de coordenação .
O plutônio também exibe estados de valência entre 3 e 7 inclusive e, portanto, é quimicamente semelhante ao neptúnio e ao urânio. É altamente reativo e forma rapidamente um filme de óxido no ar. O plutônio reage com o hidrogênio mesmo em temperaturas tão baixas quanto 25–50 °C; também forma facilmente haletos e compostos intermetálicos . As reações de hidrólise de íons plutônio de diferentes estados de oxidação são bastante diversas. O plutônio(V) pode entrar em reações de polimerização .
A maior diversidade química entre os actinídeos é observada no amerício, que pode ter valência entre 2 e 6. O amerício bivalente é obtido apenas em compostos secos e soluções não aquosas ( acetonitrila ). Os estados de oxidação +3, +5 e +6 são típicos para soluções aquosas, mas também no estado sólido. O amerício tetravalente forma compostos sólidos estáveis (dióxido, flúor e hidróxido), bem como complexos em soluções aquosas. Foi relatado que em solução alcalina o amerício pode ser oxidado ao estado heptavalente, mas esses dados se mostraram errôneos. A valência mais estável do amerício é 3 em soluções aquosas e 3 ou 4 em compostos sólidos.
A valência 3 é dominante em todos os elementos subsequentes até o laurêncio (com exceção do nobélio). O cúrio pode ser tetravalente em sólidos (fluoreto, dióxido). O berquélio, junto com uma valência de +3, também mostra a valência de +4, mais estável que a do cúrio; a valência 4 é observada em fluoreto sólido e dióxido. A estabilidade do Bk 4+ em solução aquosa é próxima à do Ce 4+ . Apenas a valência 3 foi observada para califórnio, einstênio e férmio. O estado bivalente é comprovado para mendelévio e nobélio, e no nobélio é mais estável que o estado trivalente. Lawrencium mostra valência 3 tanto em soluções quanto em sólidos.
O potencial redox aumenta de -0,32 V no urânio, passando por 0,34 V (Np) e 1,04 V (Pu) para 1,34 V no amerício, revelando a crescente capacidade de redução do íon An 4+ de amerício para urânio. Todos os actinídeos formam hidretos AnH 3 de cor preta com propriedades semelhantes ao sal. Os actinídeos também produzem carbetos com a fórmula geral de AnC ou AnC 2 (U 2 C 3 para urânio), bem como sulfetos An 2 S 3 e AnS 2 .
Compostos
Óxidos e hidróxidos
| Composto | Cor | Simetria de cristal, tipo | Constantes de rede, Å | Densidade, g/cm 3 | Temperatura, °C | ||
|---|---|---|---|---|---|---|---|
| uma | b | c | |||||
| Ac 2 O 3 | Branco | Hexagonal, La 2 O 3 | 4.07 | - | 6,29 | 19/09 | – |
| PaO2 _ | - | Cúbico, CaF 2 | 5.505 | - | - | - | - |
| Pa 2 O 5 | Branco | cúbico, CaF 2 Cúbico Tetragonal Hexagonal Romboédrico Ortorrômbico |
5,446 10,891 5,429 3,817 5,425 6,92 |
- - - - - 4.02 |
- 10,992 5,503 13,22 - 4, 18 |
- | 700 700–1100 1000 1000–1200 1240–1400 – |
| ThO 2 | Incolor | Cúbico | 5,59 | - | - | 9,87 | – |
| UO 2 | Preto amarronzado | Cúbico | 5,47 | - | - | 10,9 | – |
| NpO2 _ | Marrom esverdeado | Cúbico, CaF 2 | 5.424 | - | - | 11.1 | – |
| PuO | Preto | Cúbico, NaCl | 4,96 | - | - | 13,9 | – |
| PuO2 _ | Verde oliva | Cúbico | 5,39 | - | - | 11.44 | – |
| Am 2 O 3 | Castanho -avermelhado Castanho-avermelhado |
Cúbico, Mn 2 O 3 Hexagonal, La 2 O 3 |
11,03 3,817 |
- | - 5.971 |
10,57 11,7 |
– |
| AmO2 _ | Preto | Cúbico, CaF 2 | 5.376 | - | - | - | - |
| Cm 2 O 3 | Branco - - |
Cúbico, Mn 2 O 2 Hexagonal, LaCl 3 Monoclínico, Sm 2 O 3 |
11,01 3,80 14,28 |
- - 3,65 |
- 6 8,9 |
11,7 | – |
| CmO2 _ | Preto | Cúbico, CaF 2 | 5,37 | - | - | - | - |
| Bk 2 O 3 | Marrom claro | Cúbico, Mn 2 O 3 | 10.886 | - | - | - | - |
| BkO2 _ | castanho-avermelhado | Cúbico, CaF 2 | 5,33 | - | - | - | - |
| Cf 2 O 3 | Amarelado Incolor - |
Cúbico, Mn 2 O 3 Monoclínico, Sm 2 O 3 Hexagonal, La 2 O 3 |
10,79 14,12 3,72 |
- 3,59 - |
- 8,80 5,96 |
- | - |
| CfO2 _ | Preto | Cúbico | 5,31 | - | - | - | - |
| Es 2 O 3 | - | Cúbico, Mn 2 O 3 Monoclínico Hexagonal, La 2 O 3 |
10,07 14,1 3,7 |
- 3,59 - |
- 8,80 6 |
- | - |
| Estado de oxidação | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| +3 | Pu 2 O 3 | Am 2 O 3 | Cm 2 O 3 | Bk 2 O 3 | Cf 2 O 3 | Es 2 O 3 | |||||
| +4 | ThO 2 | PaO2 _ | UO 2 | NpO2 _ | PuO2 _ | AmO2 _ | CmO2 _ | BkO2 _ | CfO2 _ | ||
| +5 | Pa 2 O 5 | U 2 O 5 | Np 2 O 5 | ||||||||
| +5,+6 | U 3 O 8 | ||||||||||
| +6 | UO 3 |
| Fórmula química | ThO 2 | PaO2 _ | UO 2 | NpO2 _ | PuO2 _ | AmO2 _ | CmO2 _ | BkO2 _ | CfO2 _ |
| Número CAS | 1314-20-1 | 12036-03-2 | 1344-57-6 | 12035-79-9 | 12059-95-9 | 12005-67-3 | 12016-67-0 | 12010-84-3 | 12015-10-0 |
| Massa molar | 264,04 | 263.035 | 270,03 | 269.047 | 276.063 | 275,06 | 270–284** | 279.069 | 283.078 |
| Ponto de fusão | 3390°C | 2865°C | 2547°C | 2400°C | 2175°C | ||||
| Estrutura de cristal |
 Um 4+ : __ / O 2− : __ |
||||||||
| Grupo espacial | Fm 3 m | ||||||||
| Número de coordenação | Um [8], O[4] | ||||||||
- An – actinida
**Dependendo dos isótopos
Alguns actinídeos podem existir em várias formas de óxidos como An 2 O 3 , AnO 2 , An 2 O 5 e AnO 3 . Para todos os actinídeos, os óxidos AnO 3 são anfotéricos e An 2 O 3 , AnO 2 e An 2 O 5 são básicos, reagem facilmente com a água, formando bases:
- An 2 O 3 + 3 H 2 O → 2 An(OH) 3 .
Essas bases são pouco solúveis em água e por sua atividade estão próximas aos hidróxidos de metais de terras raras. Np(OH) 3 ainda não foi sintetizado, Pu(OH) 3 tem uma cor azul enquanto Am(OH) 3 é rosa e hidróxido de cúrio Cm(OH) 3 é incolor. Bk(OH) 3 e Cf(OH) 3 também são conhecidos, assim como hidróxidos tetravalentes para Np, Pu e Am e pentavalentes para Np e Am.
A base mais forte é de actínio. Todos os compostos de actínio são incolores, exceto o sulfeto de actínio preto (Ac 2 S 3 ). Dióxidos de actinídeos tetravalentes cristalizam no sistema cúbico , assim como no fluoreto de cálcio .
O tório reagindo com o oxigênio forma exclusivamente o dióxido:
O dióxido de tório é um material refratário com o ponto de fusão mais alto entre qualquer óxido conhecido (3390 ° C). A adição de 0,8 a 1% de ThO 2 ao tungstênio estabiliza sua estrutura, de modo que os filamentos dopados têm melhor estabilidade mecânica às vibrações. Para dissolver o ThO 2 em ácidos, ele é aquecido a 500–600 °C; o aquecimento acima de 600 °C produz uma forma de ThO 2 muito resistente a ácidos e outros reagentes . A pequena adição de íons fluoreto catalisa a dissolução do dióxido de tório em ácidos.
Dois óxidos de protactínio foram obtidos: PaO 2 (preto) e Pa 2 O 5 (branco); o primeiro é isomórfico com ThO 2 e o último é mais fácil de obter. Ambos os óxidos são básicos e o Pa(OH) 5 é uma base fraca e pouco solúvel.
A decomposição de certos sais de urânio, por exemplo UO 2 (NO 3 )·6H 2 O no ar a 400 °C, produz UO 3 laranja ou amarelo . Este óxido é anfótero e forma vários hidróxidos, sendo o mais estável o hidróxido de uranila UO 2 (OH) 2 . A reação do óxido de urânio(VI) com hidrogênio resulta em dióxido de urânio, que é semelhante em suas propriedades com ThO 2 . Este óxido também é básico e corresponde ao hidróxido de urânio (U(OH) 4 ).
Plutônio, neptúnio e amerício formam dois óxidos básicos: An 2 O 3 e AnO 2 . O trióxido de neptúnio é instável; assim, apenas Np 3 O 8 pôde ser obtido até agora. No entanto, os óxidos de plutônio e neptúnio com a fórmula química AnO 2 e An 2 O 3 são bem caracterizados.
Sais
| Fórmula química | AcCl 3 | UC 3 | NpCl3 _ | PuCl 3 | AmCl 3 | CmCl3 _ | BkCl 3 | CfCl 3 |
|---|---|---|---|---|---|---|---|---|
| Número CAS | 22986-54-5 | 10025-93-1 | 20737-06-8 | 13569-62-5 | 13464-46-5 | 13537-20-7 | 13536-46-4 | 13536-90-8 |
| Massa molar | 333.386 | 344.387 | 343.406 | 350,32 | 349,42 | 344–358** | 353.428 | 357.438 |
| Ponto de fusão | 837°C | 800°C | 767°C | 715°C | 695°C | 603°C | 545°C | |
| Ponto de ebulição | 1657°C | 1767°C | 850°C | |||||
| Estrutura de cristal |
 Um 3+ : __ / Cl − : __ |
|||||||
| Grupo espacial | P6 3 /m | |||||||
| Número de coordenação | Um *[9], Cl [3] | |||||||
| Constantes de rede |
a = 762 pm c = 455 pm |
a = 745,2 pm c = 432,8 pm |
a = 739,4 pm c = 424,3 pm |
a = 738,2 pm c = 421,4 pm |
a = 726 pm c = 414 pm |
a = 738,2 pm c = 412,7 pm |
a = 738 pm c = 409 pm |
|
- * An – actinide
**Dependendo dos isótopos
| Composto | Cor | Simetria de cristal, tipo | Constantes de rede, Å | Densidade, g/cm 3 | ||
|---|---|---|---|---|---|---|
| uma | b | c | ||||
| AcF 3 | Branco | Hexagonal, LaF 3 | 4,27 | - | 7,53 | 7,88 |
| PaF 4 | Marrom escuro | Monoclínica | 12,7 | 10,7 | 8,42 | – |
| PaF 5 | Preto | Tetragonal , β-UF 5 | 11,53 | - | 5.19 | – |
| ThF 4 | Incolor | Monoclínica | 13 | 10,99 | 8,58 | 5,71 |
| UF3 _ | Roxo-avermelhado | Hexagonal | 7,18 | - | 7,34 | 8,54 |
| UF4 _ | Verde | Monoclínica | 27/11 | 10,75 | 8,40 | 6,72 |
| α-UF 5 | Azulado | Tetragonal | 6,52 | - | 4,47 | 5,81 |
| β-UF 5 | Azulado | Tetragonal | 11,47 | - | 5.20 | 6,45 |
| UF 6 | Amarelado | Ortorrômbico | 9,92 | 8,95 | 5.19 | 5.06 |
| NpF 3 | Preto ou roxo | Hexagonal | 7.129 | - | 7.288 | 9.12 |
| NpF 4 | Luz verde | Monoclínica | 12,67 | 10,62 | 8,41 | 6,8 |
| NpF 6 | Laranja | Ortorrômbico | 9,91 | 8,97 | 5.21 | 5 |
| PuF 3 | Violeta-azul | Trigonal | 7.09 | - | 7,25 | 9,32 |
| PuF 4 | Castanho claro | Monoclínica | 12,59 | 10,57 | 8,28 | 6,96 |
| PuF 6 | castanho-avermelhado | Ortorrômbico | 9,95 | 9.02 | 3,26 | 4,86 |
| AmF 3 | Rosa ou bege claro | hexagonal , LaF 3 | 7.04 | - | 7.255 | 9,53 |
| AmF 4 | Vermelho-alaranjado | Monoclínica | 12,53 | 10,51 | 8.20 | – |
| CmF 3 | Do marrom ao branco | Hexagonal | 4.041 | - | 7.179 | 9.7 |
| CmF 4 | Amarelo | Monoclínica, UF 4 | 12,51 | 10,51 | 8.20 | – |
| BkF 3 | Amarelo verde |
Trigonal , LaF 3 Ortorrômbica , YF 3 |
6,97 6,7 |
- 7.09 |
7,14 4,41 |
10,15 9,7 |
| BkF 4 | - | Monoclínica, UF 4 | 12,47 | 10,58 | 8.17 | – |
| CfF 3 | - - |
Trigonal, LaF 3 Ortorrômbica, YF 3 |
6, 94 6,65 |
- 7.04 |
7,10 4,39 |
– |
| CfF 4 | - - |
Monoclínica, UF 4 Monoclínica, UF 4 |
1,242 1,233 |
1,047 1,040 |
8.126 8.113 |
– |

Os actinídeos reagem facilmente com halogênios formando sais com as fórmulas MX 3 e MX 4 (X = halogênio ). Assim, o primeiro composto de berquélio, BkCl 3 , foi sintetizado em 1962 com uma quantidade de 3 nanogramas. Como os halogênios dos elementos de terras raras, os cloretos , brometos e iodetos de actinídeos são solúveis em água e os fluoretos são insolúveis. O urânio produz facilmente um hexafluoreto incolor, que sublima a uma temperatura de 56,5°C; devido à sua volatilidade, é utilizado na separação de isótopos de urânio com centrifugação a gás ou difusão gasosa . Os hexafluoretos de actinídeos têm propriedades próximas aos anidridos . São muito sensíveis à umidade e hidrolisam formando AnO 2 F 2 . O pentacloreto e o hexacloreto preto de urânio foram sintetizados, mas ambos são instáveis.
A ação dos ácidos sobre os actinídeos produz sais, e se os ácidos não são oxidantes, então o actinídeo no sal está em estado de baixa valência:
- U + 2H 2 SO 4 → U(SO 4 ) 2 + 2H 2
- 2Pu + 6HCl → 2PuCl 3 + 3H 2
No entanto, nestas reações o hidrogênio regenerador pode reagir com o metal, formando o hidreto correspondente. O urânio reage com ácidos e água muito mais facilmente do que o tório.
Os sais de actinídeos também podem ser obtidos dissolvendo os hidróxidos correspondentes em ácidos. Nitratos, cloretos, sulfatos e percloratos de actinídeos são solúveis em água. Ao cristalizar a partir de soluções aquosas, estes sais formam hidratos, tais como Th(NO 3 ) 4 ·6H 2 O, Th(SO 4 ) 2 ·9H 2 O e Pu 2 (SO 4 ) 3 ·7H 2 O. Sais de actinídeos de alta valência hidrolisam facilmente. Assim, sulfato incolor, cloreto, perclorato e nitrato de tório se transformam em sais básicos com as fórmulas Th(OH) 2 SO 4 e Th(OH) 3 NO 3 . A solubilidade e insolubilidade dos actinídeos trivalentes e tetravalentes é semelhante à dos sais de lantanídeos. Assim , fosfatos , fluoretos , oxalatos , iodatos e carbonatos de actinídeos são fracamente solúveis em água; eles precipitam como hidratos, como ThF 4 ·3H 2 O e Th(CrO 4 ) 2 ·3H 2 O.
Os actinídeos com estado de oxidação +6, exceto os cátions do tipo AnO 2 2+ , formam [AnO 4 ] 2− , [An 2 O 7 ] 2− e outros ânions complexos. Por exemplo, urânio, neptúnio e plutônio formam sais dos tipos Na 2 UO 4 (uranato) e (NH 4 ) 2 U 2 O 7 (diuranato). Em comparação com os lantanídeos, os actinídeos formam compostos de coordenação mais facilmente , e essa capacidade aumenta com a valência dos actinídeos. Os actinídeos trivalentes não formam compostos de coordenação do fluoreto, enquanto o tório tetravalente forma os complexos K 2 ThF 6 , KThF 5 e mesmo K 5 ThF 9 . O tório também forma os sulfatos correspondentes (por exemplo Na 2 SO 4 ·Th(SO 4 ) 2 ·5H 2 O), nitratos e tiocianatos. Sais com a fórmula geral An 2 Th(NO 3 ) 6 · n H 2 O são de natureza de coordenação, com o número de coordenação do tório igual a 12. Ainda mais fácil é produzir sais complexos de actinídeos pentavalentes e hexavalentes. Os compostos de coordenação mais estáveis dos actinídeos – tório tetravalente e urânio – são obtidos em reações com dicetonas, por exemplo, acetilacetona .
Formulários
Embora os actinídeos tenham algumas aplicações estabelecidas na vida cotidiana, como em detectores de fumaça (amerício) e mantos de gás (tório), eles são usados principalmente em armas nucleares e como combustível em reatores nucleares. As duas últimas áreas exploram a propriedade dos actinídeos de liberar enorme energia em reações nucleares, que sob certas condições podem se tornar reações em cadeia autossustentáveis .
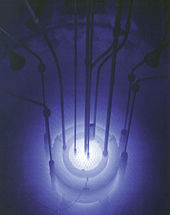
O isótopo mais importante para aplicações de energia nuclear é o urânio-235 . É usado no reator térmico , e sua concentração em urânio natural não ultrapassa 0,72%. Este isótopo absorve fortemente os nêutrons térmicos liberando muita energia. Um ato de fissão de 1 grama de 235 U se converte em cerca de 1 MW·dia. De importância, é que235
92você
emite mais nêutrons do que absorve; ao atingir a massa crítica ,235
92você
entra em uma reação em cadeia auto-sustentável. Normalmente, o núcleo de urânio é dividido em dois fragmentos com a liberação de 2-3 nêutrons, por exemplo:
-
235
92você
+1
0n
⟶115
45Rh
+118
47Ag
+ 31
0n
Outros isótopos de actinídeos promissores para a energia nuclear são o tório-232 e seu produto do ciclo do combustível do tório , o urânio-233 .
| Reator nuclear |
|
O núcleo da maioria dos reatores nucleares da Geração II contém um conjunto de hastes metálicas ocas, geralmente feitas de ligas de zircônio , preenchidas com pastilhas de combustível nuclear sólido – principalmente óxido, carbeto, nitreto ou monossulfeto de urânio, plutônio ou tório, ou sua mistura (o tão -chamado combustível MOX ). O combustível mais comum é o óxido de urânio-235.
Os nêutrons rápidos são retardados por moderadores , que contêm água, carbono , deutério ou berílio , como nêutrons térmicos para aumentar a eficiência de sua interação com o urânio-235. A taxa de reação nuclear é controlada pela introdução de hastes adicionais feitas de boro ou cádmio ou um absorvente líquido, geralmente ácido bórico . Os reatores para produção de plutônio são chamados de reator reprodutor ou reprodutores; eles têm um design diferente e usam nêutrons rápidos. |
A emissão de nêutrons durante a fissão do urânio é importante não apenas para a manutenção da reação nuclear em cadeia, mas também para a síntese dos actinídeos mais pesados. O urânio-239 converte-se via decaimento β em plutônio-239, que, como o urânio-235, é capaz de fissão espontânea. Os primeiros reatores nucleares do mundo foram construídos não para energia, mas para produzir plutônio-239 para armas nucleares.
Cerca de metade do tório produzido é usado como material emissor de luz dos mantos de gás. O tório também é adicionado em ligas multicomponentes de magnésio e zinco . Assim as ligas Mg-Th são leves e fortes, mas também possuem alto ponto de fusão e ductilidade e por isso são amplamente utilizadas na indústria aeronáutica e na produção de mísseis . O tório também possui boas propriedades de emissão de elétrons , com longa vida útil e baixa barreira de potencial para a emissão. O conteúdo relativo de isótopos de tório e urânio é amplamente utilizado para estimar a idade de vários objetos, incluindo estrelas (ver datação radiométrica ).
A principal aplicação do plutônio foi em armas nucleares , onde o isótopo plutônio-239 foi um componente chave devido à sua facilidade de fissão e disponibilidade. Projetos baseados em plutônio permitem reduzir a massa crítica para cerca de um terço da do urânio-235. As bombas de plutônio do tipo "Fat Man" produzidas durante o Projeto Manhattan usaram compressão explosiva de plutônio para obter densidades significativamente mais altas que o normal, combinadas com uma fonte central de nêutrons para iniciar a reação e aumentar a eficiência. Assim, apenas 6,2 kg de plutônio foram necessários para um rendimento explosivo equivalente a 20 quilotons de TNT . (Veja também Projeto de armas nucleares .) Hipoteticamente, apenas 4 kg de plutônio – e talvez até menos – poderiam ser usados para fazer uma única bomba atômica usando projetos de montagem muito sofisticados.
O plutônio-238 é um isótopo potencialmente mais eficiente para reatores nucleares, pois tem massa crítica menor que o urânio-235, mas continua a liberar muita energia térmica (0,56 W/g) por decaimento mesmo quando a reação em cadeia de fissão é interrompida por barras de controle . Sua aplicação é limitada pelo alto preço (cerca de US$ 1.000/g). Este isótopo tem sido usado em termopilhas e sistemas de destilação de água de alguns satélites e estações espaciais. Assim , as naves espaciais Galileo e Apollo (por exemplo, Apollo 14 ) tinham aquecedores alimentados por quilogramas de óxido de plutônio-238; esse calor também é transformado em eletricidade com termopilhas. O decaimento do plutônio-238 produz partículas alfa relativamente inofensivas e não é acompanhado por radiação gama. Portanto, este isótopo (~160 mg) é usado como fonte de energia em marcapassos cardíacos onde dura cerca de 5 vezes mais que as baterias convencionais.
Actínio-227 é usado como fonte de nêutrons. Sua alta energia específica (14,5 W/g) e a possibilidade de obter quantidades significativas de compostos termicamente estáveis são atrativos para uso em geradores termoelétricos de longa duração para uso remoto. O 228 Ac é usado como indicador de radioatividade em pesquisas químicas, pois emite elétrons de alta energia (2,18 MeV) que podem ser facilmente detectados. As misturas de 228 Ac - 228 Ra são amplamente utilizadas como fonte gama intensa na indústria e na medicina.
O desenvolvimento de materiais auto-incandescentes dopados com actinídeos com matrizes cristalinas duráveis é uma nova área de utilização de actinídeos, pois a adição de radionuclídeos emissores de alfa a alguns vidros e cristais pode conferir luminescência.
Toxicidade

As substâncias radioativas podem prejudicar a saúde humana por (i) contaminação local da pele, (ii) exposição interna devido à ingestão de isótopos radioativos e (iii) superexposição externa por atividade β e radiação γ . Juntamente com os elementos rádio e transurânio, o actínio é um dos venenos radioativos mais perigosos com alta atividade α específica . A característica mais importante do actínio é sua capacidade de acumular e permanecer na camada superficial dos esqueletos . No estágio inicial do envenenamento, o actínio se acumula no fígado . Outro perigo do actínio é que ele sofre decaimento radioativo mais rápido do que é excretado. A adsorção do trato digestivo é muito menor (~0,05%) para o actínio do que para o rádio.
O protactínio no corpo tende a se acumular nos rins e nos ossos. A dose máxima segura de protactínio no corpo humano é de 0,03 µCi que corresponde a 0,5 microgramas de 231 Pa. Este isótopo, que pode estar presente no ar como aerossol , é 2,5 × 108 vezes mais tóxico que o ácido cianídrico .
O plutônio, ao entrar no corpo através do ar, alimentos ou sangue (por exemplo, uma ferida), instala-se principalmente nos pulmões, fígado e ossos, com apenas cerca de 10% indo para outros órgãos, e permanece lá por décadas. O longo tempo de residência do plutônio no corpo é parcialmente explicado por sua baixa solubilidade em água. Alguns isótopos de plutônio emitem radiação alfa ionizante, que danifica as células vizinhas. A dose letal mediana (DL 50 ) por 30 dias em cães após injeção intravenosa de plutônio é de 0,32 miligrama por kg de massa corporal e, portanto, a dose letal para humanos é de aproximadamente 22 mg para uma pessoa pesando 70 kg; a quantidade para exposição respiratória deve ser aproximadamente quatro vezes maior. Outra estimativa assume que o plutônio é 50 vezes menos tóxico que o rádio e, portanto, o conteúdo permitido de plutônio no corpo deve ser de 5 µg ou 0,3 µCi. Tal quantidade é quase invisível ao microscópio. Após testes em animais, esta dose máxima permitida foi reduzida para 0,65 µg ou 0,04 µCi. Estudos em animais também revelaram que a via de exposição ao plutônio mais perigosa é a inalação, após a qual 5-25% das substâncias inaladas são retidas no corpo. Dependendo do tamanho das partículas e da solubilidade dos compostos de plutônio, o plutônio é localizado nos pulmões ou no sistema linfático , ou é absorvido no sangue e depois transportado para o fígado e os ossos. A contaminação através dos alimentos é a forma menos provável. Nesse caso, apenas cerca de 0,05% dos compostos solúveis 0,01% insolúveis de plutônio são absorvidos pelo sangue e o restante é excretado. A exposição da pele danificada ao plutônio reteria quase 100% dele.
O uso de actinídeos em combustível nuclear, fontes radioativas seladas ou materiais avançados, como cristais auto-incandescentes, tem muitos benefícios potenciais. No entanto, uma séria preocupação é a radiotoxicidade extremamente alta dos actinídeos e sua migração no meio ambiente. O uso de formas quimicamente instáveis de actinídeos em MOX e fontes radioativas seladas não é apropriado pelos padrões de segurança modernos. Existe um desafio para desenvolver materiais contendo actinídeos estáveis e duráveis, que proporcionem armazenamento, uso e disposição final seguros. Uma necessidade chave é a aplicação de soluções sólidas de actinídeos em fases hospedeiras cristalinas duráveis.
Propriedades nucleares
| Nuclídeo | Meia vida | Modo de decaimento | Fração de ramificação | Fonte |
|---|---|---|---|---|
| 206 81Tl |
4,202 ± 0,011 m | β- _ | 1,0 | LNHB |
| 208 81Tl |
3,060 ± 0,008 m | β- _ | 1,0 | BIPM-5 |
| 210 82Pb |
22,20 ± 0,22 anos | β- _ | 1,0 | ENSDF |
| α | ( 1,9 ± 0,4 ) x 10 −8 | |||
| 211 82Pb |
36,1 ± 0,2 m | β- _ | 1,0 | ENSDF |
| 212 82Pb |
10,64 ± 0,01 h | β- _ | 1,0 | BIPM-5 |
| 214 82Pb |
26,8 ± 0,9 m | β- _ | 1,0 | ENSDF |
| 211 83Bi |
2,14 ± 0,02 m | β- _ | 0,00276 ± 0,00004 | ENSDF |
| α | 0,99724 ± 0,00004 | |||
| 212 83Bi |
60,54 ± 0,06 m | α | 0,3593 ± 0,0007 | BIPM-5 |
| β- _ | 0,6407 ± 0,0007 | |||
| 214 83Bi |
19,9 ± 0,4 m | α | 0,00021 ± 0,00001 | ENSDF |
| β- _ | 0,99979 ± 0,00001 | |||
| 210 84Po |
138,376 ± 0,002 d | α | 1,0 | ENSDF |
| 219 86Rn |
3,96 ± 0,01 s | α | 1,0 | ENSDF |
| 220 86Rn |
55,8 ± 0,3 s | α | 1,0 | BIPM-5 |
| 221 87Fr |
4,9 ± 0,2 m | β- _ | 0,00005 ± 0,00003 | ENSDF |
| α | 0,99995 ± 0,00003 | |||
| 223 88Rá |
11,43 ± 0,05 d | α | 1,0 | ENSDF |
| 14 °C | ( 8,9 ± 0,4 ) x 10 −10 | |||
| 224 88Rá |
3,627 ± 0,007 d | α | 1,0 | BIPM-5 |
| 225 88Rá |
14,9 ± 0,2 d | β- _ | 1,0 | ENSDF |
| 226 88Rá |
( 1,600 ± 0,007 ) x 10 3 anos | α | 1,0 | BIPM-5 |
| 228 88Rá |
5,75 ± 0,03 anos | β- _ | 1,0 | ENSDF |
| 224 89Ac |
2,78 ± 0,17 h | α | 0,091 +0,020 -0,014 | ENSDF |
| CE | 0,909 +0,014 -0,020 | |||
| 225 89Ac |
10,0 ± 0,1 d | α | 1,0 | ENSDF |
| 227 89Ac |
21,772 ± 0,003 anos | α | 0,01380 ± 0,00004 | ENSDF |
| β- _ | 0,98620 ± 0,00004 | |||
| 228 89Ac |
6,15 ± 0,02 h | β- _ | 1,0 | ENSDF |
| 227 90º |
18,718 ± 0,005 d | α | 1,0 | BIPM-5 |
| 228 90º |
698,60 ± 0,23 d | α | 1,0 | BIPM-5 |
| 229 90º |
( 7,34 ± 0,16 ) x 10 3 anos | α | 1,0 | ENSDF |
| 230 90º |
( 7,538 ± 0,030 ) x 10 4 anos | α | 1,0 | ENSDF |
| SF | ≤ 4 x 10 −13 | |||
| 231 90º |
25,52 ± 0,01 h | β- _ | 1,0 | ENSDF |
| α | ~ 4 x 10 −13 | |||
| 232 90º |
( 1,405 ± 0,006 ) x 10 10 anos | α | 1,0 | ENSDF |
| SF | ( 1,1 ± 0,4 ) x 10 −11 | |||
| 233 90º |
22,15 ± 0,15 m | β- _ | 1,0 | LNHB |
| 234 90º |
24,10 ± 0,03 d | β- _ | 1,0 | ENSDF |
| 231 91Pai |
( 3,276 ± 0,011 ) x 10 4 anos | α | 1,0 | ENSDF |
| SF | ≤ 3 x 10 −12 | |||
| 232 91Pai |
1,32 ± 0,02 d | CE | 0,00003 ± 0,00001 | ENSDF |
| β- _ | 0,99997 ± 0,00001 | |||
| 233 91Pai |
26,98 ± 0,02 d | β- _ | 1,0 | LNHB |
| 234 91Pai |
6,70 ± 0,05 h | β- _ | 1,0 | ENSDF |
| 234m 91Pai |
1,159 ± 0,016 m | ISTO | 0,0016 ± 0,0002 | AIEA-CRP-XG |
| β- _ | 0,9984 ± 0,0002 | |||
| 232 92você |
68,9 ± 0,4 anos | α | 1,0 | ENSDF |
| SF | ||||
| 233 92você |
( 1,592 ± 0,002 ) x 10 5 anos | α | 1,0 | ENSDF |
| SF | ||||
| 234 92você |
( 2,455 ± 0,006 ) x 10 5 anos | α | 1,0 | LNHB |
| SF | ( 1,6 ± 0,2 ) x 10 −11 | |||
| 235m 92você |
26 ± 1 m | ISTO | 1,0 | ENSDF |
| 235 92você |
( 7,038 ± 0,005 ) x 10 8 anos | α | 1,0 | ENSDF |
| SF | ( 7 ± 2 ) x 10 −11 | |||
| 236 92você |
( 2,342 ± 0,004 ) x 10 7 anos | α | 1,0 | ENSDF |
| SF | ( 9,4 ± 0,4 ) x 10 −10 | |||
| 237 92você |
6,749 ± 0,016 d | β- _ | 1,0 | LNHB |
| 238 92você |
( 4,468 ± 0,005 ) x 10 9 anos | α | 1,0 | LNHB |
| SF | ( 5,45 ± 0,04 ) x 10 −7 | |||
| 239 92você |
23,45 ± 0,02 m | β- _ | 1,0 | ENSDF |
| 236 93Np |
( 1,55 ± 0,08 ) x 10 5 anos | α | 0,0016 ± 0,0006 | LNHB |
| β- _ | 0,120 ± 0,006 | |||
| CE | 0,878 ± 0,006 | |||
| 236m 93Np |
22,5 ± 0,4 h | β- _ | 0,47 ± 0,01 | LNHB |
| CE | 0,53 ± 0,01 | |||
| 237 93Np |
( 2,144 ± 0,007 ) x 10 6 anos | α | 1,0 | ENSDF |
| SF | ||||
| 238 93Np |
2,117 ± 0,002 d | β- _ | 1,0 | ENSDF |
| 239 93Np |
2,356 ± 0,003 d | β- _ | 1,0 | ENSDF |
| 236 94Pu |
2,858 ± 0,008 anos | α | 1,0 | ENSDF |
| LNHB | Laboratoire National Henri Becquerel, Dados recomendados,
http://www.nucleide.org/DDEP_WG/DDEPdata.htm , 3 de outubro de 2006. |
| BIPM-5 | MILÍMETROS. Bé, V. Chisté, C. Dulieu, E. Browne, V. Chechev, N. Kuzmenko, R. Helmer,
A. Nichols, E. Schönfeld, R. Dersch, Monographie BIPM-5, Table of Radionuclides, Vol. 2 – A = 151 a 242, 2004. |
| ENSDF | "Arquivo de Dados da Estrutura Nuclear Avaliada" . Laboratório Nacional de Brookhaven . Recuperado em 15 de novembro de 2006 . |
| AIEA-CRP-XG | MILÍMETROS. Bé, VP Chechev, R. Dersch, OAM Helene, RG Helmer, M. Herman,
S. Hlavác, A. Marcinkowski, GL Molnár, AL Nichols, E. Schönfeld, VR Vanin, MJ Woods, IAEA CRP "Atualização dos Padrões de Dados de Decaimento de Raios X e Gama para Calibração de Detectores e Outras Aplicações", Informações Científicas e Técnicas da IAEA relatório STI/PUB/1287, maio de 2007, Agência Internacional de Energia Atômica, Viena, Áustria, ISBN 92-0-113606-4 . |
Veja também
Referências e notas
Bibliografia
- Golub, AM (1971). Общая и неорганическая химия (Química Geral e Inorgânica) . Vol. 2.
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- Myasoedov, B. (1972). Química analítica de elementos transplutônio . Moscou: Nauka. ISBN 978-0-470-62715-0.
links externos
- Lawrence Berkeley Laboratory imagem da tabela periódica histórica de Seaborg mostrando séries de actinídeos pela primeira vez
- Lawrence Livermore National Laboratory, Descobrindo os Segredos dos Actinídeos
- Laboratório Nacional de Los Alamos, Actinide Research Quarterly

![{\displaystyle {\ce {{^{238}_{92}U}+{}_{0}^{1}n->{}_{92}^{239}U->[\beta ^{ -}][23,5\ {\ce {min}}]{}_{93}^{239}Np->[\beta ^{-}][2,3\ {\ce {dias}}]{}_{ 94}^{239}Pu}}\left({\ce {->[\alpha ][2.4\cdot 10^{4}\ {\ce {anos}}]}}\right){\ce {^ {235}_{92}U}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e7a95dee843f1cf5e9156013e8ca01c30870d896)



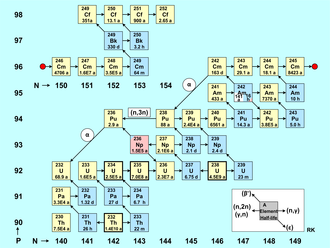

![{\displaystyle {\begin{array}{l}{}\\{\ce {2AmF3{}+3Ba->[{\ce {1150-1350^{\circ }C}}]3BaF2{}+2Am} }\\{\ce {PuF4{}+2Ba->[{\ce {1200^{\circ }C}}]2BaF2{}+Pu}}\\{\ce {UF4{}+2Mg->[ {\ce {>500^{\circ }C}}]U{}+2MgF2}}\\{}\end{array}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/057c8209f7427fca3331e574fa79f36c0e2a81db)










![{\displaystyle {\ce {Th{}+O2->[{\ce {1000^{\circ }C}}]\overbrace {ThO2} ^{Thorium~dioxide}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/13e4a27b9ed3d03fc5420ed4a04020bf77562406)