Valência (química) - Valence (chemistry)
Em química , a valência ou valência de um elemento é a medida de sua capacidade de combinação com outros átomos quando forma compostos químicos ou moléculas .
Descrição
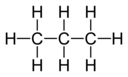
A capacidade de combinação, ou afinidade de um átomo de um determinado elemento, é determinada pelo número de átomos de hidrogênio com os quais ele se combina. No metano , o carbono tem valência 4; na amônia , o nitrogênio tem valência 3; na água, o oxigênio tem valência 2; e no cloreto de hidrogênio, o cloro tem valência 1. O cloro, como tem valência um, pode substituir o hidrogênio. O fósforo tem uma valência de 5 no pentacloreto de fósforo , PCl 5 . Os diagramas de valência de um composto representam a conectividade dos elementos, com linhas traçadas entre dois elementos, às vezes chamadas de ligações, representando uma valência saturada para cada elemento. As duas tabelas abaixo mostram alguns exemplos de compostos diferentes, seus diagramas de valência e as valências de cada elemento do composto.
| Composto | H 2 Hidrogênio |
CH 4 metano |
C 3 H 8 Propano |
C 2 H 2 acetileno |
|---|---|---|---|---|
| Diagrama |
|

|
|
|
| Valências |
| Composto | NH 3 Amônia |
Cianeto de sódio NaCN |
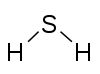
H 2 S sulfeto de hidrogênio |
H 2 SO 4 ácido sulfúrico |
Cl 2 O 7 Heptoxido de dicloro |
XeO 4 tetróxido de xenônio |
|---|---|---|---|---|---|---|
| Diagrama |

|
|
|

|

|

|
| Valências |
Definições modernas
Valência é definida pela IUPAC como:
- O número máximo de átomos univalentes (originalmente átomos de hidrogênio ou cloro) que podem se combinar com um átomo do elemento em consideração, ou com um fragmento, ou para o qual um átomo deste elemento pode ser substituído.
Uma descrição moderna alternativa é:
- O número de átomos de hidrogênio que podem se combinar com um elemento em um hidreto binário ou duas vezes o número de átomos de oxigênio combinados com um elemento em seu óxido ou óxidos.
Esta definição difere da definição IUPAC, pois pode-se dizer que um elemento tem mais de uma valência.
Uma definição moderna muito semelhante dada em um artigo recente define a valência de um átomo particular em uma molécula como "o número de elétrons que um átomo usa na ligação", com duas fórmulas equivalentes para calcular a valência:
- valência = número de elétrons na camada de valência do átomo livre - número de elétrons não ligados no átomo na molécula ,
e
- valência = número de ligações + carga formal .
Desenvolvimento histórico
A etimologia das palavras de valência (plural valências ) e valência (plural valências ) remonta a 1425, que significa "extrair, preparação", do latim valentia "força, capacidade", a partir do início valor "valor, valor", ea química o significado que se refere ao "poder de combinação de um elemento" é registrado em 1884, do alemão Valenz .
O conceito de valência foi desenvolvido na segunda metade do século 19 e ajudou a explicar com sucesso a estrutura molecular dos compostos inorgânicos e orgânicos. A busca pelas causas subjacentes da valência levou às teorias modernas de ligações químicas, incluindo o átomo cúbico (1902), estruturas de Lewis (1916), teoria das ligações de valência (1927), orbitais moleculares (1928), teoria de repulsão do par de elétrons da camada de valência (1958), e todos os métodos avançados da química quântica .
Em 1789, William Higgins publicou opiniões sobre o que chamou de combinações de partículas "finais", que prenunciaram o conceito de ligações de valência . Se, por exemplo, de acordo com Higgins, a força entre a partícula final de oxigênio e a partícula final de nitrogênio fosse 6, então a força da força seria dividida em conformidade, e da mesma forma para as outras combinações de partículas finais (ver ilustração) .
O início exato, no entanto, da teoria das valências químicas pode ser rastreada até um artigo de 1852 de Edward Frankland , no qual ele combinou a teoria radical mais antiga com pensamentos sobre afinidade química para mostrar que certos elementos têm a tendência de se combinar com outros elementos para formar compostos contendo 3, ou seja, nos grupos de 3 átomos (por exemplo, NO 3 , NH 3 , NI 3 , etc.) ou 5, ou seja, nos grupos de 5 átomos (por exemplo, NO 5 , NH 4 O, PO 5 , etc.), equivalentes dos elementos anexados. Segundo ele, esta é a maneira pela qual suas afinidades são mais satisfeitas e, seguindo esses exemplos e postulados, ele declara quão óbvio é que
Uma tendência ou lei prevalece (aqui), e que, não importa quais sejam os caracteres dos átomos que se unem, o poder de combinação do elemento de atração, se me permite o termo, é sempre satisfeito pelo mesmo número desses átomos .
Esse “poder de combinação” foi posteriormente chamado de quantivalência ou valência (e valência pelos químicos americanos). Em 1857, August Kekulé propôs valências fixas para muitos elementos, como 4 para o carbono, e as usou para propor fórmulas estruturais para muitas moléculas orgânicas , que ainda são aceitas hoje.
A maioria dos químicos do século 19 definiu a valência de um elemento como o número de suas ligações, sem distinguir diferentes tipos de valência ou ligação. No entanto, em 1893 Alfred Werner descreveu complexos de coordenação de metal de transição , como [Co (NH 3 ) 6 ] Cl 3 , em que ele distinguiu valências principais e subsidiárias (alemão: 'Hauptvalenz' e 'Nebenvalenz'), correspondendo aos conceitos modernos de estado de oxidação e número de coordenação, respectivamente.
Para os elementos do grupo principal , em 1904, Richard Abegg considerou valências positivas e negativas (estados de oxidação máximo e mínimo) e propôs a regra de Abegg no sentido de que sua diferença é frequentemente 8.
Elétrons e valência
O modelo de Rutherford do átomo nuclear (1911) mostrou que o exterior de um átomo é ocupado por elétrons , o que sugere que os elétrons são responsáveis pela interação dos átomos e pela formação de ligações químicas. Em 1916, Gilbert N. Lewis explicou a valência e as ligações químicas em termos de uma tendência dos átomos (do grupo principal) de atingir um octeto estável de 8 elétrons da camada de valência. De acordo com Lewis, a ligação covalente leva a octetos pelo compartilhamento de elétrons, e a ligação iônica leva a octetos pela transferência de elétrons de um átomo para outro. O termo covalência é atribuído a Irving Langmuir , que afirmou em 1919 que "o número de pares de elétrons que qualquer átomo compartilha com os átomos adjacentes é chamado de covalência desse átomo". O prefixo co- significa "junto", de modo que uma ligação co-valente significa que os átomos compartilham uma valência. Posteriormente a isso, agora é mais comum falar de ligações covalentes em vez de valência , que caiu em desuso no trabalho de nível superior com os avanços na teoria da ligação química, mas ainda é amplamente utilizado em estudos elementares, onde fornece uma introdução heurística ao assunto.
Na década de 1930, Linus Pauling propôs que também existem ligações covalentes polares , que são intermediárias entre covalentes e iônicas, e que o grau de caráter iônico depende da diferença de eletronegatividade dos dois átomos ligados.
Pauling também considerou as moléculas hipervalentes , nas quais os elementos do grupo principal têm valências aparentes maiores do que o máximo de 4 permitido pela regra do octeto. Por exemplo, na molécula de hexafluoreto de enxofre (SF 6 ), Pauling considerou que o enxofre forma 6 verdadeiras ligações de dois elétrons usando orbitais atômicos híbridos sp 3 d 2 , que combinam um orbital s, três p e dois d. No entanto, mais recentemente, cálculos de mecânica quântica nesta e em moléculas semelhantes mostraram que o papel dos orbitais d na ligação é mínimo, e que a molécula de SF 6 deve ser descrita como tendo 6 ligações covalentes polares (parcialmente iônicas) feitas de apenas quatro orbitais no enxofre (um se três p) de acordo com a regra do octeto, junto com seis orbitais nos flúores. Cálculos semelhantes em moléculas de metal de transição mostram que o papel dos orbitais p é menor, de modo que um orbital se cinco orbitais d no metal são suficientes para descrever a ligação.
Valências comuns
Para elementos nos grupos principais da tabela periódica , a valência pode variar entre 1 e 7.
| Grupo | Valence 1 | Valence 2 | Valence 3 | Valence 4 | Valence 5 | Valence 6 | Valence 7 | Valence 8 | Valências típicas |
|---|---|---|---|---|---|---|---|---|---|
| 1 (I) | NaCl | 1 | |||||||
| 2 (II) | MgCl 2 | 2 | |||||||
| 13 (III) |
BCl 3 AlCl 3 Al 2 O 3 |
3 | |||||||
| 14 (IV) | CO | CH 4 | 4 | ||||||
| 15 (V) | NÃO |
NH 3 PH 3 As 2 O 3 |
NO 2 |
N 2 O 5 PCl 5 |
3 e 5 | ||||
| 16 (VI) |
H 2 O H 2 S |
SO 2 | SO 3 | 2 e 6 | |||||
| 17 (VII) | HCl | HClO 2 | ClO 2 | HClO 3 | Cl 2 O 7 | 1 e 7 | |||
| 18 (VIII) | XeO 4 | 8 |
Muitos elementos têm uma valência comum relacionada à sua posição na tabela periódica, e atualmente isso é racionalizado pela regra do octeto . Os prefixos numéricos gregos / latinos (mono- / uni-, di- / bi-, tri- / ter- e assim por diante) são usados para descrever íons nos estados de carga 1, 2, 3 e assim por diante, respectivamente. A polivalência ou multivalência refere-se a espécies que não estão restritas a um número específico de ligações de valência . As espécies com uma única carga são univalentes (monovalentes). Por exemplo, o cátion Cs + é um cátion univalente ou monovalente, enquanto o cátion Ca 2+ é um cátion divalente, e o cátion Fe 3+ é um cátion trivalente. Ao contrário do Cs e do Ca, o Fe também pode existir em outros estados de carga, notavelmente 2+ e 4+, e é, portanto, conhecido como íon multivalente (polivalente). Os metais de transição e os metais à direita são tipicamente multivalentes, mas não há um padrão simples que prediz sua valência.
| Valência | Adjetivo mais comum ‡ | Adjetivo sinônimo menos comum ‡ § |
|---|---|---|
| 0-valente | zerovalente | não valente |
| 1 valente | monovalente | univalente |
| 2 valente | divalente | bivalente |
| 3 valente | trivalente | tervalente |
| 4 valente | tetravalente | quadrivalente |
| 5 valente | pentavalente | quinquevalent /pentavalente |
| 6 valente | hexavalente | sexivalente |
| 7 valente | heptavalente | septivalente |
| 8 valente | octavalente | - |
| 9 valente | não valente | - |
| 10 valente | decavalente | - |
| múltiplo / muitos / variável | polivalente | multivalente |
| juntos | covalente | - |
| Não juntos | não covalente | - |
† Os mesmos adjetivos também são usados na medicina para se referir à valência da vacina, com a ligeira diferença de que, neste último sentido, quadri- é mais comum do que tetra- .
‡ Conforme demonstrado pela contagem de acessos na pesquisa na web do Google e nos corpora de pesquisa do Google Livros (acessado em 2017).
§ Algumas outras formas podem ser encontradas em grandes corpora em inglês (por exemplo, * quintavalente, * quintivalente, * decivalente ), mas não são as formas convencionalmente estabelecidas em inglês e, portanto, não são inseridas nos principais dicionários.
Valência versus estado de oxidação
Devido à ambigüidade do termo valência, outras notações são atualmente preferidas. Ao lado do sistema de estados de oxidação (também chamados de números de oxidação ), conforme usado na nomenclatura de estoque para compostos de coordenação , e a notação lambda, conforme usado na nomenclatura IUPAC de química inorgânica , o estado de oxidação é uma indicação mais clara do estado eletrônico dos átomos em uma molécula.
O estado de oxidação de um átomo em uma molécula fornece o número de elétrons de valência que ganhou ou perdeu. Em contraste com o número de valência, o estado de oxidação pode ser positivo (para um átomo eletropositivo) ou negativo (para um átomo eletronegativo ).
Os elementos em um estado de alta oxidação podem ter uma valência superior a quatro. Por exemplo, em percloratos , o cloro tem sete ligações de valência; o rutênio , no estado de oxidação +8 no tetróxido de rutênio , tem oito ligações de valência.
Exemplos
| Composto | Fórmula | Valência | Estado de oxidação |
|---|---|---|---|
| Cloreto de hidrogênio | HCl | H = 1 Cl = 1 | H = +1 Cl = −1 |
| Ácido perclórico * | HClO 4 | H = 1 Cl = 7 O = 2 | H = +1 Cl = +7 O = −2 |
| Hidreto de sódio | NaH | Na = 1 H = 1 | Na = +1 H = −1 |
| Óxido ferroso ** | FeO | Fe = 2 O = 2 | Fe = +2 O = −2 |
| Óxido férrico ** | Fe 2 O 3 | Fe = 3 O = 2 | Fe = +3 O = −2 |
* O íon perclorato univalente ( ClO-
4) tem valência 1.
** O óxido de ferro aparece em uma estrutura de cristal , portanto, nenhuma molécula típica pode ser identificada.
No óxido ferroso, o Fe apresenta estado de oxidação II; no óxido férrico, estado de oxidação III.
| Composto | Fórmula | Valência | Estado de oxidação |
|---|---|---|---|
| Cloro | Cl 2 | Cl = 1 | Cl = 0 |
| Peróxido de hidrogênio | H 2 O 2 | H = 1 O = 2 | H = +1 O = −1 |
| Acetileno | C 2 H 2 | C = 4 H = 1 | C = −1 H = +1 |
| Cloreto de mercúrio (I) | Hg 2 Cl 2 | Hg = 2 Cl = 1 | Hg = +1 Cl = −1 |
As valências também podem ser diferentes dos valores absolutos dos estados de oxidação devido à polaridade diferente das ligações. Por exemplo, em diclorometano , CH 2 Cl 2 , o carbono tem valência 4, mas estado de oxidação 0.
Definição de "número máximo de títulos"
Frankland considerou que a valência (ele usou o termo "atomicidade") de um elemento era um único valor que correspondia ao valor máximo observado. O número de valências não utilizadas em átomos do que agora são chamados de elementos do bloco p é geralmente par, e Frankland sugeriu que as valências não utilizadas saturaram umas às outras. Por exemplo, o nitrogênio tem uma valência máxima de 5; na formação da amônia, duas valências são deixadas soltas; o enxofre tem uma valência máxima de 6; na formação do sulfeto de hidrogênio, quatro valências são deixadas soltas.
A União Internacional de Química Pura e Aplicada (IUPAC) fez várias tentativas para chegar a uma definição inequívoca de valência. A versão atual, adotada em 1994:
- O número máximo de átomos univalentes (originalmente átomos de hidrogênio ou cloro) que podem se combinar com um átomo do elemento em consideração, ou com um fragmento, ou para o qual um átomo deste elemento pode ser substituído.
Hidrogênio e cloro foram originalmente usados como exemplos de átomos univalentes, devido à sua natureza de formar apenas uma ligação simples. O hidrogênio tem apenas um elétron de valência e pode formar apenas uma ligação com um átomo que possui uma camada externa incompleta . O cloro tem sete elétrons de valência e pode formar apenas uma ligação com um átomo que doa um elétron de valência para completar a camada externa do cloro. No entanto, o cloro também pode ter estados de oxidação de +1 a +7 e pode formar mais de uma ligação ao doar elétrons de valência .
O hidrogênio tem apenas um elétron de valência, mas pode formar ligações com mais de um átomo. No íon bifluoreto ( [HF
2]-
), por exemplo, forma uma ligação de quatro elétrons de três centros com dois átomos de flúor:
- [F – HF - ↔ F - H – F]
Outro exemplo é a ligação de dois elétrons de três centros em diborano (B 2 H 6 ).
Valências máximas dos elementos
Valências máximas para os elementos são baseadas nos dados da lista de estados de oxidação dos elementos .
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Grupo → | |||||||||||||||||||||
| ↓ Período | |||||||||||||||||||||
| 1 | 1 H |
2 Ele |
|||||||||||||||||||
| 2 | 3 Li |
4 Ser |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
|||||||||||||
| 3 | 11 N / D |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
|||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 Como |
34 Se |
35 Br |
36 Kr |
|||
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 CD |
49 No |
50 Sn |
51 Sb |
52 Te |
53 eu |
54 Xe |
|||
| 6 | 55 Cs |
56 BA |
|
71 Lu |
72 Hf |
73 Ta |
74 C |
75 Ré |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 No |
86 Rn |
||
| 7 | 87 Fr |
88 Ra |
|
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og |
||
|
|
57 La |
58 Ce |
59 Pr |
60 WL |
61 PM |
62 Sm |
63 Eu |
64 D'us |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
|||||||
|
|
89 Ac |
90 º |
91 Pa |
92 você |
93 Np |
94 Pu |
95 Sou |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 Não |
|||||||
| Valências máximas são baseadas na lista de estados de oxidação dos elementos | |||||||||||||||||||||
|
0 1 2 3 4 5 6 7 8 9 Desconhecido A cor de fundo mostra valência máxima do elemento químico |
|||||||||||||||||||||

